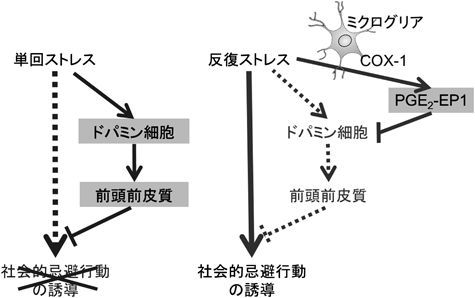
2) Goshen, I., Kreisel, T., Ben-Menachem-Zidon, O., Licht, T., Weidenfeld, J., Ben-Hur, T., & Yirmiya, R. (2008) Mol. Psychiatry, 13, 717–728.
3) Barik, J., Marti, F., Morel, C., Fernandez, S.P., Lanteri, C., Godeheu, G., Tassin, J.P., Mombereau, C., Faure, P., & Tronche, F. (2013) Science, 339, 332–335.
4) Tanaka, K., Furuyashiki, T., Kitaoka, S., Senzai, Y., Imoto, Y., Segi-Nishida, E., Deguchi, Y., Breyer, R.M., Breyer, M.D., & Narumiya, S. (2012) J. Neurosci., 32, 4319–4329.
7) Lammel, S., Ion, D.I., Roeper, J., & Malenka, R.C. (2011) Neuron, 70, 855–862.
9) Chaudhury, D., Walsh, J.J., Friedman, A.K., Juarez, B., Ku, S.M., Koo, J.W., Ferguson, D., Tsai, H.C., Pomeranz, L., Christoffel, D.J., Nectow, A.R., Ekstrand, M., Domingos, A., Mazei-Robison, M.S., Mouzon, E., Lobo, M.K., Neve, R.L., Friedman, J.M., Russo, S.J., Deisseroth, K., Nestler, E.J., & Han, M.H. (2013) Nature, 493, 532–536.
11) Butts, K.A., Weinberg, J., Young, A.H., & Phillips, A.G. (2011) Proc. Natl. Acad. Sci. USA, 108, 18459–18564.
12) Refojo, D., Schweizer, M., Kuehne, C., Ehrenberg, S., Thoeringer, C., Vogl, A.M., Dedic, N., Schumacher, M., von Wolff, G., Avrabos, C., Touma, C., Engblom, D., Schütz, G., Nave, K.A., Eder, M., Wotjak, C.T., Sillaber, I., Holsboer, F., Wurst, W., & Deussing, J.M. (2011) Science, 333, 1903–1907.
13) Nomura, D.K., Morrison, B.E., Blankman, J.L., Long, J.Z., Kinsey, S.G., Marcondes, M.C., Ward, A.M., Hahn, Y.K., Lichtman, A.H., Conti, B., & Cravatt, B.F. (2011) Science, 334, 809–813.
14) Müller, N., Schwarz, M.J., Dehning, S., Douhe, A., Cerovecki, A., Goldstein-Müller, B., Spellmann, I., Hetzel, G., Maino, K., Kleindienst, N., Möller, H.J., Arolt, V., & Riedel, M. (2006) Mol. Psychiatry, 11, 680–684.