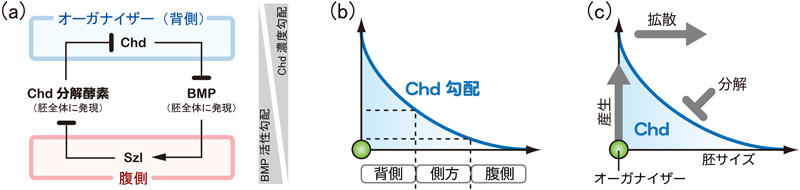
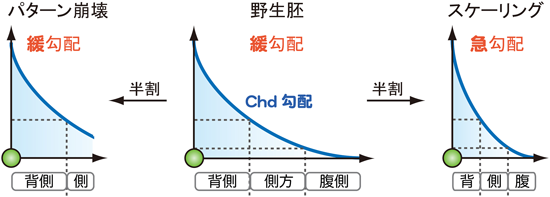
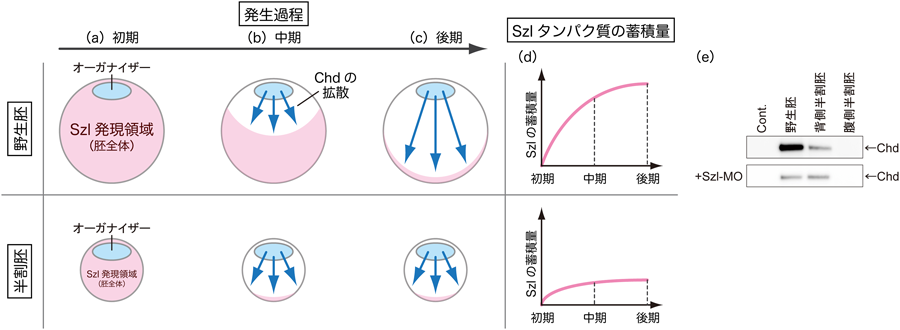
生物の相似性を保証する濃度勾配のスケーリングScaling of Dorsal-Ventral patterning by Embryo size
1 独立行政法人理化学研究所多細胞システム形成研究センター体軸動態研究チームLaboratory for Axial Pattern Dynamics Team, Center for Developmental Biology, RIKEN ◇ 〒650-0047 兵庫県神戸市中央区港島南町2-2-32-2-3 Minatojima-Minami-machi, Chuo-ku, Kobe-shi, Hyogo 650-0047, Japan
2 独立行政法人科学技術振興機構さきがけ「細胞機能の構成的な理解と制御」研究領域Research Area ‘Design and Control of Cellular Functions’, Precursory Research for Embryonic Science and Technology (PRESTO), Japan Science and Technology Agency (JST)