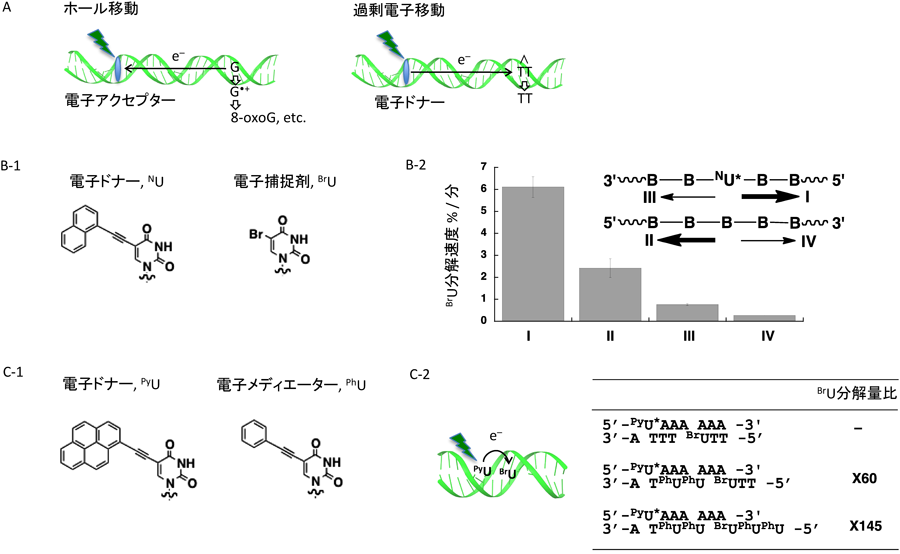
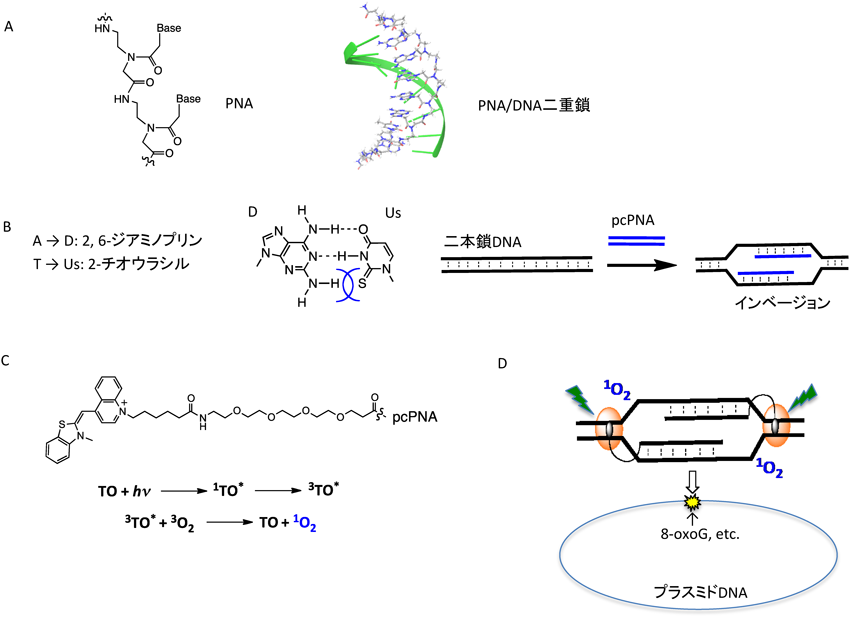
人工核酸を用いたDNA内電荷移動とDNA光損傷DNA-mediated charge transfer and DNA photodamage by artificial nucleic acids
筑波大学生命領域学際研究センター小宮山プロジェクトKomiyama Project, Life Science Center of Tsukuba Advanced Research Alliance, University of Tsukuba ◇ 〒305-8577 茨城県つくば市天王台一丁目1番1号1-1-1 Tennodai, Tsukuba-shi, Ibaraki 305-8577, Japan