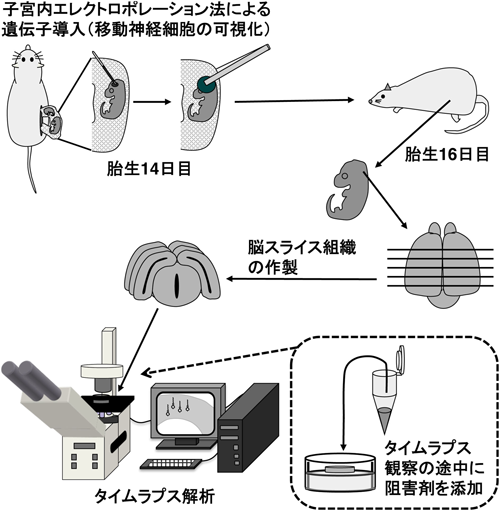
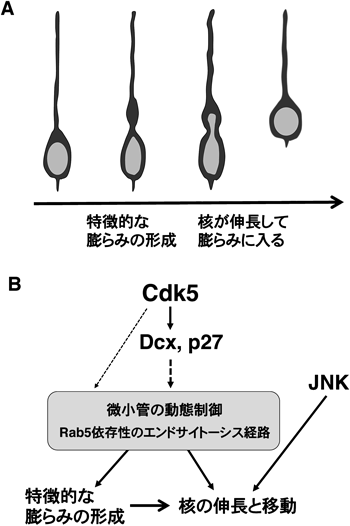
Cdk5およびp27kip1による大脳皮質形成の制御機構:増殖停止細胞における細胞周期関連分子の役割Beyond the cell cycle regulation: Novel functions of cell cycle-related proteins in brain development
1 公益財団法人先端医療振興財団先端医療センター研究所医薬品研究開発部医薬品開発研究グループDrug Development Group, Department of Molecular Life Science, Institute of Biomedical Research and Innovation Laboratory, Foundation for Biomedical Research and Innovation ◇ 〒650-0047 兵庫県神戸市中央区港島南町二丁目2番2-2 Minatojima-Minami-machi, Chuo-ku, Kobe-shi, Hyogo 650-0047, Japan
2 慶應義塾大学医学部生理学教室Department of Physiology, School of Medicine, Keio University ◇ 〒160-8582 東京都新宿区信濃町35番地35 Shinano-machi, Shinjuku-ku, Tokyo 160-8582, Japan