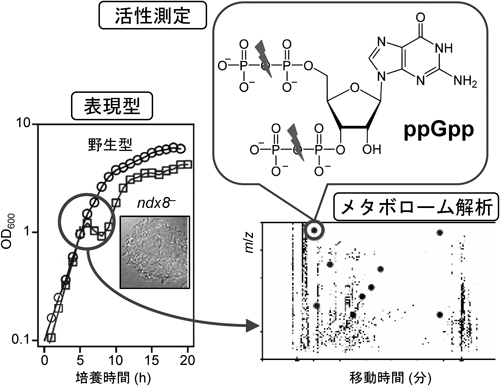
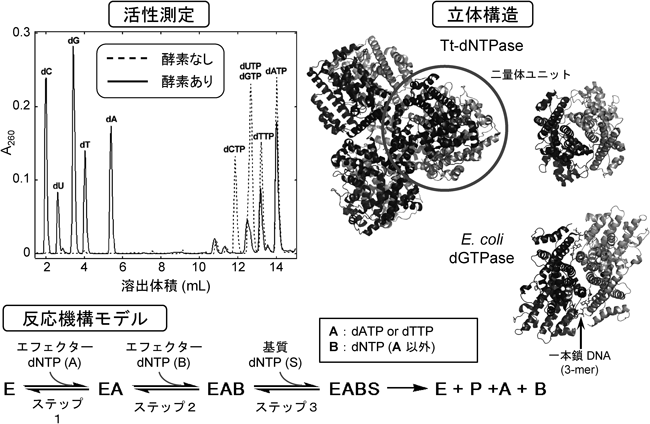
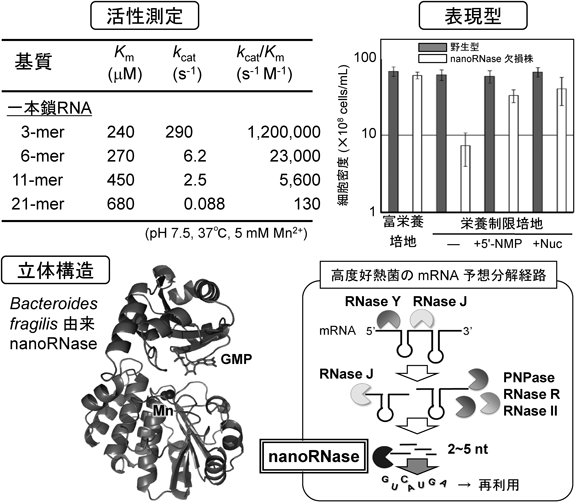
1) Ooga, T., Ohashi, Y., Kuramitsu, S., Koyama, Y., Tomita, M., Soga, T., & Masui, R. (2009) J. Biol. Chem., 284, 15549–15556.
3) Kondo, N., Nakagawa, N., Ebihara, A., Chen, L., Liu, Z.J., Wang, B.C., Yokoyama, S., Kuramitsu, S., & Masui, R. (2007) Acta Crystallogr. D Biol. Crystallogr., 63, 230–239.
4) Vorontsov, I.I., Minasov, G., Kiryukhina, O., Brunzelle, J.S., Shuvalova, L., & Anderson, W.F. (2011) J. Biol. Chem., 286, 33158–33166.
5) Singh, D., Gawel, D., Itsko, M., Hochkoeppler, A., Krahn, J.M., London, R.E., & Schaaper, R.M. (2015) J. Biol. Chem., 290, 10418–10429.
6) Goldstone, D.C., Ennis-Adeniran, V., Hedden, J.J., Groom, H.C., Rice, G.I., Christodoulou, E., Walker, P.A., Kelly, G., Haire, L.F., Yap, M.W., de Carvalho, L.P., Stoye, J.P., Crow, Y.J., Taylor, I.A., & Webb, M. (2011) Nature, 480, 379–382.
7) Lahouassa, H., Daddacha, W., Hofmann, H., Ayinde, D., Logue, E.C., Dragin, L., Bloch, N., Maudet, C., Bertrand, M., Gramberg, T., Pancino, G., Priet, S., Canard, B., Laguette, N., Benkirane, M., Transy, C., Landau, N.R., Kim, B., & Margottin-Goguet, F. (2012) Nat. Immunol., 13, 223–228.
8) Ryoo, J., Choi, J., Oh, C., Kim, S., Seo, M., Kim, S.Y., Seo, D., Kim, J., White, T.E., Brandariz-Nunez, A., Diaz-Griffero, F., Yun, C.H., Hollenbaugh, J.A., Kim, B., Baek, D., & Ahn, K. (2014) Nat. Med., 20, 936–941.
9) Wakamatsu, T., Kim, K., Uemura, Y., Nakagawa, N., Kuramitsu, S., & Masui, R. (2011) J. Biol. Chem., 286, 2807–2816.
10) Uemura, Y., Nakagawa, N., Wakamatsu, T., Kim, K., Montelione, G.T., Hunt, J.F., Kuramitsu, S., & Masui, R. (2013) FEBS Lett., 587, 2669–2674.