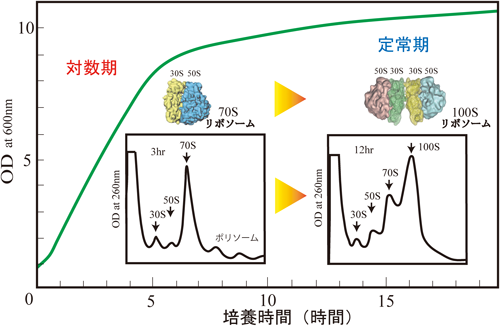
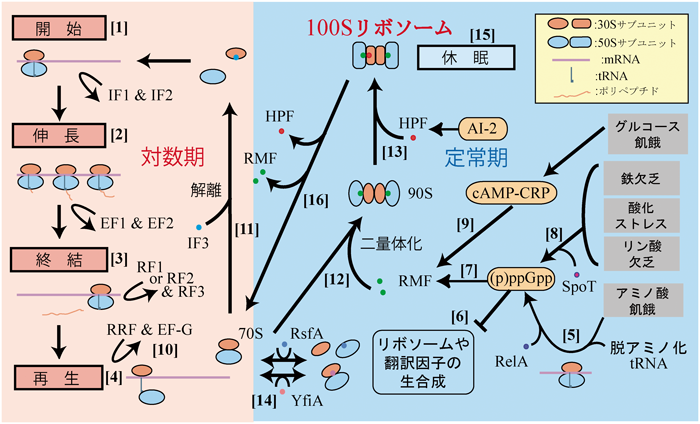
100Sリボソーム形成による翻訳制御とリボソームサイクルThe ribosome cycle and translational regulation by the formation of 100S ribosome
1 大阪医科大学医学部総合教育講座物理学教室Department of Physics, Osaka Medical College ◇ 〒569–8686 大阪府高槻市大学町2–7 ◇ Daigakumachi 2–7, Takatsuki, Osaka 569–8686, Japan
2 株式会社吉田生物研究所バイオ情報研究部門Bio-informatics section, Yoshida Biological Laboratory ◇ 〒607–8081 京都市山科区竹鼻外田町11–1 ◇ Takebanasotoda-cho 11–1, Yamashina-ku, Kyoto 607–8081, Japan