1995~2015年の20年間で,脳が合成する神経ステロイド(男性・女性ホルモンが代表的)の作用研究は大きく進展した.脳海馬が合成する男性・女性ホルモンの作用に関しては,動物実験のみならず,高齢者の増加に伴い臨床的に重要なヒトのデータも集まりつつある.分子論的には,古典的な核内受容体を介した遺伝子転写経路(genomic経路)とは異なる,神経シナプスに存在する(膜上)ステロイド受容体を介したnon-genomic作用でキナーゼを駆動する速い作用経路を明らかにしたことに意義がある.以前は「性ホルモンのnon-genomic経路の詳細を明らかにする」という申請書を書くと,「過去30年間にわたりnon-genomic経路は何度も提唱されたが,実態がいまだに不明であり,この提案は却下すべきである」とされたりして,悔しい思いをしたこともある.しかし今や性ホルモンのnon-genomic作用に関する確固たる分子基盤がわかってきた.2014年に相次いで企画された複数のSpecial Issueに招待論文を書いたが,それらSpecial Issueの編集まえがきにはたとえば「10年前と比べるとエストラジオールの作用研究の進歩により,神経シナプスのモジュレーターであるという新しい概念を生んだ」と明確に述べられている1, 2).Journal of Endocrinology誌は“60 years of Neuroendocrinology”という特集を組んでこの分野の進歩を後押ししている3).
筆者はこの分野を長年研究してきたが,2015年に東京大学を定年になったのを機会にこれまでの研究をまとめ,将来の方向を展望してみたい.内容は川戸研で行ってきたラット・マウスの研究成果に基づいているが,世界の潮流と対比して論じる.なお本稿では以下特にことわりなく,T(テストステロン),DHT(ジヒドロテストステロン),E2(エストラジオール),ER(エストロゲン受容体),AR(アンドロゲン受容体),LTP(長期増強),LTD(長期抑制)などを略語で表記する.また本稿では,「女性ホルモン」はほとんどの場合エストラジオール(E2)のことを指す.
女性ホルモン(エストロゲン)補充療法が,更年期以降の女性の記憶・認知機能の劣化(アルツハイマー病など)の改善に有効であることは,世界中で1000万人にものぼる対象者の治療によって明らかになり,この分子機構を神経科学的に説明するために膨大な研究が積み重ねられてきた.2000年以降15年の間に,“Brain and Estrogen”や“Estrogen and Cognition”という題名をつけた特別号が有名なジャーナルからたびたび出版されている1, 4–9).
初期は,E2による脳神経の保護作用(慢性的ステロイド作用,数日~数週間かかる)が研究の中心だった.また視床下部–下垂体–性腺軸での生殖系の制御が老化により異常になる現象(更年期症状)に関するものも多かった.ところが2005年以降は,記憶中枢である海馬において,E2による神経シナプスのモジュレーション作用が記憶能力を改善するという論文が多くなってきて,この分野が確立してきた.このようなE2の神経作用はメスのラット・マウスの海馬だけでなくオスの海馬でもよく研究されている.オスでは海馬内でいったんTがE2に変換されて作用するので,E2作用が研究されているわけである.
2005年ごろまでは,E2がシナプスなどの神経回路を変化させるためには,12~28時間の長い時間を必要とする古典的経路(genomic process)だけが考えられてきた.それは「女性ホルモン受容体(エストロゲン受容体;ER)や男性ホルモン受容体(アンドロゲン受容体;AR)が細胞質に存在し,E2がERに,T, DHTがARに結合すると,ホルモン—受容体複合体は核内に移動し,遺伝子転写とタンパク質合成が起こり,シナプスが変化する」という経路である.これに対して我々は20~120分で速く作用する,「神経シナプスの細胞膜上に局在する受容体ERやARにE2やTが結合すると,下流のタンパク質キナーゼを活性化し,神経シナプスが増加したり,LTPやLTDが増強されたりする」という経路(non-genomic process)が働いていることを示した.この発見は長い間の常識を覆すものである10–12).
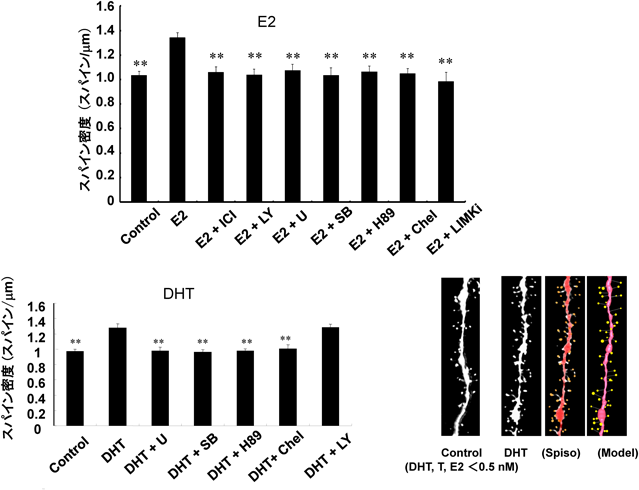
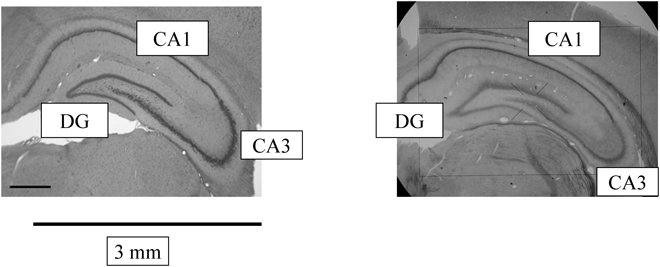
記憶の仕組みを分子レベルで研究するために,グルタミン酸神経シナプスの構造を可視化して調べる方法がある.(オスでもメスでも)E2は,神経スパイン(spine,シナプス後部)の密度を変化させることによっても,海馬の神経可塑性を制御している10, 13).スパインはシナプス前部と一緒になって記憶を蓄える最小部位シナプスを構成する.神経に蛍光色素を注入して共焦点顕微鏡で3次元画像を撮影して個々のスパインを可視化し,E2の作用を検討したところ,海馬スライスに1~10 nM E2を2時間作用させると,空間認知をつかさどるCA1部位でスパイン密度が増加する10, 14)(図1).スパイン頭部の直径は0.2~1.0 µmの分布を持つが,特に小型スパイン(0.2~0.4 µm)の増加が目立つ.中型スパイン(0.4~0.5 µm)や大型スパイン(0.5~1.0 µm)では変化が少ない.この頭部直径の解析は,我々がBioinformaticsプロジェクトで開発したスパインの数理解析プログラムSpiso-3Dで可能になった14).
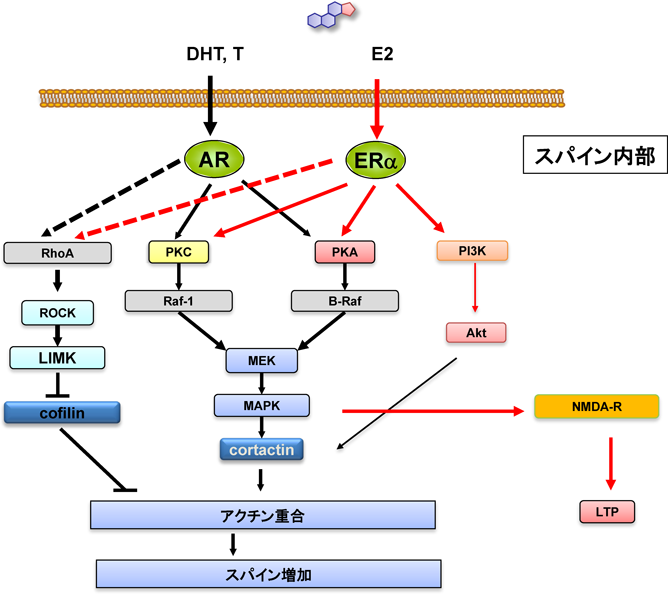
このスパイン作用を媒介する情報伝達は,「E2がスパイン内の受容体ERαに結合するとMAPK, PKA, PKC, PI3K, LIMKが活性化されてアクチンを制御するタンパク質のリン酸化が起こり,アクチンの重合を引き起こしてスパインが増加」するとまとめられる(図1, 2)6, 11).スパイン(シナプス後部)局在のERαがキナーゼを活性化するnon-genomic信号系を,キナーゼ阻害剤を使用して見いだした点が筆者らの新機軸である.non-genomic信号系の実態証明は,「スパインの内部か膜上にエストロゲン受容体が存在するか?(ERαではない新しい受容体?)」と,「キナーゼなどの速い信号系が動くか?」の2点が明らかにならない限り現実的ではないとみなされていた.
4. 速い作用を生み出すシナプスのエストロゲン受容体
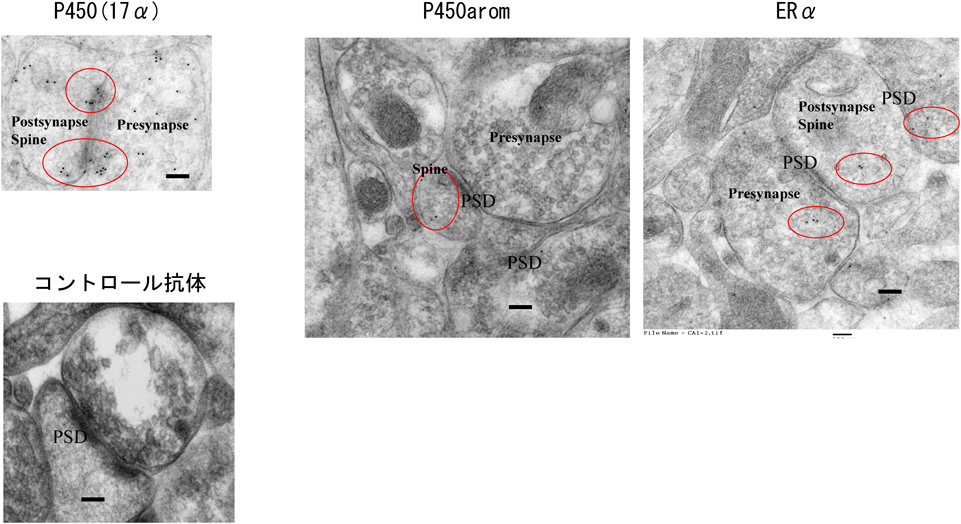
当時世界で五つくらいの大型プロジェクトが進んでいたが,いずれも脳でERαではない新しい受容体を発見できていなかった.他のプロジェクト代表との議論も参考にして,新しい可能性として,ERα自身が海馬の神経細胞や神経シナプスにも局在しているのではないか,と考えて調べることにした.ウエスタンブロットで市販の多くの抗ERα抗体を試したが,海馬試料ではERαの57 kDaバンドに結合するものはまったく存在しなかった.そこで,広島大の小南教授・山崎教授らがERαのC末端19ペプチドに対するポリクローナル抗体RC-19を作製し精製したものを使うと,海馬試料でERαの57 kDaバンドに結合するものが得られた.このRC-19を持参し,ニューヨークのMt.Sinai医大のMorrison研において金コロイド免疫電子顕微鏡解析を行った.その結果,ERαが海馬のグルタミン酸神経に発現していること,細胞体や核のみならず,神経シナプス後部(スパイン)・前部にもERαが局在していることを発見した(図3,図7参照)10).
以前に本誌ミニレビューを書いた2003年時点では,海馬でのE2受容体の検出(組織染色やin situハイブリダイゼーション)は核受容体ERαに関しても困難をきわめていた.ERαは海馬にはほとんど存在しないという報告が多かった.あるいは,新生仔期の生後10日齢ではERαが発現するが,成獣になるとほとんどなくなってしまうとか,介在神経(GABA神経)にしか発現がないなどともいわれていた.ER-Xとかいう新型受容体があるという説も出たが,現在は誤りだということになっている15).混乱の一因は世界中で,ERαのC末端20ペプチドに対する抗体として販売し使用されているMC20, HC20などが,海馬のERαの57 kDaバンドには結合せず,まったく異なるバンドに結合することにあり,ERαの発現が少ない海馬での解析には不向きな抗体であったことによる16).有名なRockefeller大のMcEwen研やKarolinska大のGustafsson研でも市販品の抗体を使っていて,抗体を自作し精製する研究室はほぼ皆無だった.Gustafsson研のMargaret Warner教授に至っては,「ウエスタンブロットによって脳のERαが検出されるはずがない,卵巣でも理論上検出されないはずだ」,と言うので大口論になった.「If I am wrong, I should leave Karolinska tomorrow」とまで言っていた.内分泌器官ではERαの発現量が多いので,多少感度や精製度の低い抗体を用いても正しい57 kDaのウエスタンバンドが得られるが,海馬・皮質・小脳のようにERαの発現量が少ない場所では,時に,57 kDaとはまったく異なる正しくないウエスタンバンドが出てしまうのだと考えた.
さらに決定的なことに,ERαがないはずのノックアウトマウスの海馬でもMC20はしっかりしたシグナルを示し,解析の結果,MC20には52 kDaの不明なタンパク質を認識する抗体が混在していることがわかった10).悩ましいのは,これらの精製度の低い市販抗体であっても,ERα量の多い脳の視床下部や卵巣では綺麗に57 kDaバンドのシグナルを示すことである.注意すべきはERα抗原が少ない脳ではモノクローナル抗体を使用しても他の類似ペプチド配列を持つタンパク質に結合してしまうことがあり,染色結果を信用できないということである.このことを理解している人は少ないが,核受容体の分子生物学の創始者で有名なフランスStrasburg大のChambon教授(ラスカー賞受賞者)と3日間話し込んだとき,「そうだそうだ,monoclonal antibody is not always monoclonal」と意見が一致して,学問的な確信を得た.彼からはERαノックアウトマウス,ERβノックアウトマウスをいただいて,ERαをノックアウトするとE2を加えてもスパインが増加しないことを確かめることができた17).一方,ERβノックアウトではスパイン増加は止まらなかった.さらにChambon教授の説明によると,当時Korach教授らが作製し実験に供していた,ERαをネオマイシン誘導性に欠損させるERαノックアウトマウスでは,N末端の欠けた活性ERαが残存するためにE2作用が残っており,完全なノックアウトマウスではないので,未発見のエストロゲン受容体を想定する論文は根拠がないと判明した18, 19).
海馬組織におけるERβの免疫組織染色では,いまだに世界中で間違いが蔓延している.すべての組織染色論文でERβのウエスタンブロットが示されていないが,筆者の経験では,市販の抗体を用いてウエスタンブロットすると,分子量のまったく異なるバンドが検出されてしまう.広島大の小南研において,ERβのC末端ペプチドに対する抗体を何種類も作製・精製して,これを用いてERβ発現細胞で反応性を調べたが,ウエスタンブロットでの判定を満たす抗体は得られなかった.ERβにはスプライシングバリアントが存在するので,うまく抗体ができないのかもしれない.ERα, ERβ以外の新規エストロゲン受容体を見つける競争は激しかったが,ミクロソーム膜上にGPR30が見いだされた20).しかし,実験してみるとE2の結合も非常に低く,E2作用がうまく検出されないので(石井,私信),まだ本当の膜上受容体とはいい切れないのではないだろうか21).GPR30はアゴニストG-1の刺激でJunキナーゼ(JNK)を活性化して海馬空間記憶を強化するが,E2刺激はGPR30を経由せず,ERα, ERβを経由してMAPKを活性化する信号系であり,両者は大きく異なることもわかってきた22).ERα自身の一部も膜に結合して存在してGタンパク質を活性化させるので,こちらの方が速い情報伝達を担っている可能性が高いと筆者は思っている23, 24).ERαのスプライシングバリアントERα41, ERα36などもいろいろと見つかっており,これらがnon-genomic機構を担う新規ERである可能性もある.
オスなら男性ホルモンT, DHTがそのまま海馬に作用してもおかしくないはずである.最近,男性ホルモンTやDHTが直接働いて神経シナプスを増やすことがわかってきた25).海馬への注入実験で,TやDHTには抗不安作用(勇敢にする作用)があることがわかっていた.我々の実験では,TやDHTを海馬神経スパインに2時間作用させると,CA1, CA3領域で急激にスパイン密度が増加した(図1)12, 14, 25).「T, DHTがスパイン内の受容体ARに結合し,LIMK, MAPK, PKA, PKCが活性化し,アクチン制御タンパク質のリン酸化を引き起こし,アクチンの重合が起きた結果,スパインが増加する」という作用経路がわかった(図2).E2作用経路と似ているが,PI3Kは関与しない点がE2とは異なっていた.男性ホルモン受容体に関してはCA1シナプスにも核と同じアンドロゲン受容体ARが見いだされており,このARを介して下流のキナーゼ群を駆動しているという結果である.ARはその発現がCA1≫CA3~DGとCA1に発現が偏っているのがERと違う特徴である.TとDHTを比較すると,作用は似ているがDHTの方がTより作用力が強い.
TとDHTが海馬神経のスパイン-シナプス(シナプス形成したスパイン)を急性的に増加させるという一連の研究もある26, 27).この仕事ではAR阻害剤フルタミドによる阻害効果がないことから,nonAR型の受容体が働いていると説明されている.しかしこのnonARは15年たっても分子が同定されていないのが大きな弱点である.sex-steroid binding globulin(SHBG)に結合したDHTが受容体megalinに結合し,cAMPを上昇させてPKAを活性化する経路が報告されているが,そうだとすると,TとDHTの膜上受容体はmegalinといえるかもしれない.
大学生と雑談をすると,脳の男性ホルモンは攻撃性と欲望を担っているという誤った思い込みがあるようである.実際,「優秀な株のトレーダーは血中・唾液のテストステロン値が高い」という神経経済学の本が売れている.これもTの攻撃性の発現だと思っているのではないか.ヒト脳内のテストステロン値は測れていないが,ラット海馬内のT値は血中の120%であり,精巣摘出をすると20%まで低下するから,トレーダーの脳のT値は血中Tと強い相関があるだろう.しかしながら,実はやる気の中枢は海馬だとされているので,攻撃性よりやる気が高いだけともいえる(前述のとおりTは抗不安作用を持つので).海馬での男性ホルモン受容体の探索はERの探索と比較してあまり注目されていないが,これは男性ホルモンが記憶と関係あるはずがない,という思い込みがあるせいだろうか.
TやDHTの記憶への作用に関する研究はE2と比べるとずっと少なく,高次脳機能におけるT, DHTの作用はよくわかっていない.これは男性の更年期が女性の更年期に比べてあまり研究されてないことにもよる.男性でも更年期や加齢により脳内のTやDHTが低下し,その結果,スパイン数が減少して記憶機能が低下し,認知症やアルツハイマー病が発生すると思われる.対処法として男性患者に対するテストステロン補充療法(注射・塗り薬など)が行われているが(米国ではなんと対象者が500万人),現在のところ日本では,女性に対する女性ホルモン補充療法ほど一般化していない.しかし近い将来は一般化することを強く期待する.男性の末梢にE2を補充すると体への副作用が問題となるので,むしろTを注射して(日本の厚生労働省は注射のみを認可している)脳の内部でE2とDHTに変換したほうがよいと考える.ちなみに2014年,80歳でエベレスト登頂に成功した三浦雄一郎さんは,テストステロン注射で,トレーニングをやる気が回復したという話をしている28).
メスラットではE2がnon-genomicに血管の弛緩を引き起こすが,オスではTがnon-genomic経路で,ARを介してPI3KやAktを活性化し,eNOSをリン酸化してNOを発生させて,血管を広げて高血圧を予防する29, 30).これが海馬の血管性の老化・認知症を抑えるわけである.血中にE2が少ないオスにとって,これは非常にありがたい機構である.
現在記憶のアンチエイジングは世界の最大関心事である.我々はここ5年間,この点に集中して研究を行ってきた.1995年までは,老化すると脳の神経細胞は死んでゆくと論文に書いてあった.ところが1995年以降,正常老化の場合,海馬の神経細胞は死なず委縮もしないということが立証された.そうすると正常老化ではどうやって記憶力が低下するのだろう? 我々は最近,正常な加齢により海馬内のTやE2が低下することでスパイン数が減少し,その結果,シナプスも減少するため記憶機能が低下するというデータを得ている.女性ホルモン補充療法でE2を送り込むと海馬の記憶能力を活性化できる理由は,スパイン密度の回復効果にあると考えている.一方,正常老化ではないアルツハイマー病モデルマウスでは,月齢が18か月を越えると,加齢とともに神経細胞が死んで数が低下し,スパイン密度が急激に減少することが報告されている.ちなみに小脳や大脳皮質では,正常老化であっても神経細胞が減少する.部位によって状況が大いに異なることに注意すべきである.
7. 神経シナプスの長期増強(LTP)と長期抑圧(LTD)
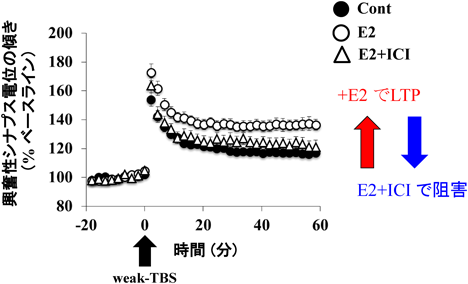
オス・メスに関わらずE2が海馬において,グルタミン酸神経のシナプス情報伝達の長期増強(long-term potentiation:LTP)や長期抑圧(long-term depression:LTD)を強化することが,電気生理学的実験によってわかってきた.LTPは記憶の書き込み現象であり,これまでに世界中で膨大な研究結果がある.多くの人は,脳由来神経栄養因子(brain-derived neurotrophic factor:BDNF)やE2がLTPを正にモジュレート(修飾)することを期待する.しかし測定条件によってはそうではない場合もあって,複雑な結果が得られている.LTPを成立させる標準的な実験では,シナプス前部を高頻度電気刺激(high frequency stimulation:HFS)して,興奮性シナプス後電位(excitatory postsynaptic potential:EPSP)を1.5~2倍増大させる(LTP成立).ラットが成獣に達しない発達期や思春期前期(2~4週齢)までにおいては(神経回路が完成していないこともあり),単純に神経栄養因子E2, BDNFの灌流によって,EPSPベースラインが急性的に上昇し,またLTP値も上昇する31, 32).しかし神経回路が完成した成獣(3か月)かそれ以後では(18~20か月の老齢まで),E2の灌流でEPSPベースライン上昇がみられず,LTPも変化しない33, 34).このことは10年間大きな論争となっていた.我々は,成獣(3か月)以後LTP値の上昇がみられないのは,HFS電気刺激が強すぎて,それ以上LTPを強化する力がないためであることを見いだした.E2でEPSPベースラインが急性的に上昇するかしないかは,神経シナプスが未熟なのか成熟しているのかに依存しているのであろう.一般的なHFSとしてはθバースト刺激(TBS, 200ミリ秒の間に100 Hzで5パルスを10回繰り返す刺激)か,テタヌス刺激(100 Hzで1秒刺激)が使われてきた.我々は弱い閾値以下のTBS刺激を作り出して(weak-TBS, 3回のみ繰り返し),E2灌流下のweak-TBS刺激によりLTP成立(E2-LTP)に成功し,ようやく神経栄養因子効果を見いだせたのである(図4)11).ここで閾値以下のTBS刺激のみではLTPは成立しない.
この結果E2-LTP成立における信号伝達系は,「E2がスパインERα/ERβに結合し,MAPK, PKA, PKCの活性化によるNMDA受容体のリン酸化によってCa2+流入量の増加が起こり,CaMKIIが活性化しE2-LTPが成立」というものである.我々の工夫はスパイン(シナプス後部)局在のERα/ERβがキナーゼを活性化するnon-genomic信号系を,キナーゼ阻害剤を使用して見いだした点にある.
イタリアのPettorossi, Grassi研では阻害剤レトロゾールで海馬スライスのP450aromをわずか20分阻害しE2産生を止めただけでCA1のLTPが小さくなることを見いだした35, 36).我々も追試してこれを確かめたが,わずか20分の間TからのE2合成を止めただけでLTPが阻害されるということは,スライスでの局所E2合成がLPTの誘導に有効であることを示した点で画期的である.我々を含めて他のグループはみな外からE2を灌流などで加えて急性効果を調べていたので,局所合成のE2作用を直接測定していたとはいいがたいからである.またDHT, TがE2と反対にLTPを抑える方向に働くことがわかってきた11, 36).DHT, TはE2による過剰興奮性を抑えているのであろうか? これからの重要課題になりそうである.
名古屋大の曽我部研究室は,Tの上流のデヒドロエピアンドロステロン(DHEA),プレグネノロン(PREG)の海馬における急性作用を研究してきた.DG領域でP450sccを阻害してPREG合成を止めると直ちにEPSPが減少し,LTPが小さくなる.DHEAを灌流するとLTPが復活する37).DHEAは性ホルモンより副作用が少ない薬になる可能性があるが,いまだにDHEA受容体が同定されていないのが弱点である.
LTDは低頻度刺激(low frequency stimulation)または低濃度NMDA刺激により引き起こされて,EPSPが80%程度に低下する.LTDは誤ったシナプス記憶を消す作用であり,この作用がないと,全体として正しい記憶を形成できない.我々は通常,最初は大雑把に記憶するが,その半分程度は誤った記憶であり,その後反復して正しい記憶に修正している.LTDが生じない遺伝子改変マウスでは神経行動テストの成績が悪くなる.ラットの海馬スライスで1~10 nMのE2を灌流すると,EPSPが80%から60%になりE2によってLTDが強化される5, 10, 38).
ここまで論じてきた性ホルモン作用は,精巣・卵巣が合成するTやE2が血流に乗り脳に流入して慢性的に作用する,いわゆる内分泌作用ではなく,脳の神経細胞自身が合成してその近傍の細胞(組織)で働くTやE2の作用だと捉えるべきである.つまり局所合成・局所作用である.なぜならば,この20年間で,記憶中枢の海馬が独自に男性ホルモン(T, DHT)や女性ホルモン(E2)を合成していることが確かめられたためである(オス・メス両方とも)39–43).海馬内での男性・女性ホルモン濃度を測定すると,血中をめぐっているTやE2濃度より高いことがわかり(メスでは100倍にもなる)43, 44),海馬合成のT, E2は脇役ではなく主役であることがわかった.
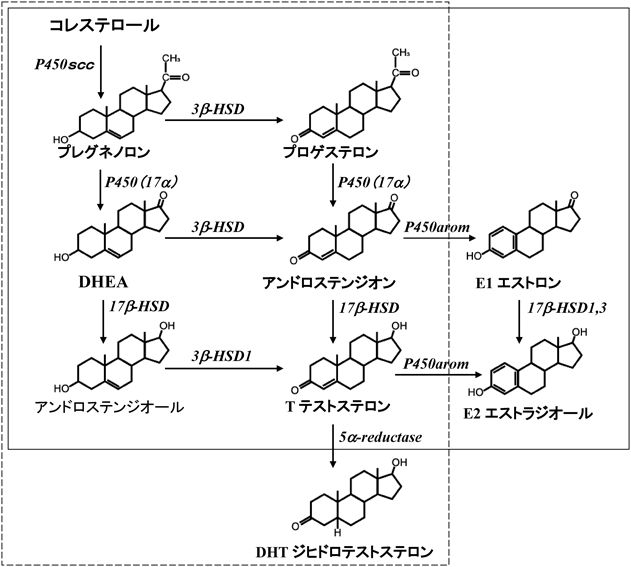
我々の研究を含む,2000~2015年の研究の結果判明した,海馬(ラットとマウス)での神経細胞中のステロイドの生合成経路を図5に示す.コレステロールから始まり,PREG(P450sccが合成),DHEA(P450(17α)が合成),T(17β-HSDが合成)と変換されたのち,DHT(5α-reductaseが合成)か,E2(P450aromが合成)になる,という経路である.この経路を証明する上で最も難題であったのは,P450(17α)がmRNAでもタンパク質でも脳には存在しないという数多くの論文報告を覆して,P450(17α)とDHEA, T, E2合成を発見することであった.この分野の開拓者であるパリの国立保健医学研究機構(INSERM)のBaulieu教授が,PREGやプロゲステロン(PROG)までが神経ステロイドであって,その先のステロイド合成系は脳には存在しない,つまり,どんな実験からもP450(17α)は存在しないし,DHEAやTも合成されないという論文をPNAS誌などに繰り返し書いており,これが大きな壁であった45–47).「DHEAよりも下流の性ステロイドは,卵巣・精巣のみで合成され,血中をめぐり脳に到達して作用する」というのが,今に至る常識であった.精巣摘出を行うと2日以内に確かに脳内のTは,従来のラジオイムノアッセイや質量分析の技術では検出できない程度にまで,大きく減少する.しかし検出感度を100~1000倍上げることで,ようやく脳内合成されるTを捉えることができるようになった40, 41).
振り返ると,1990年代後半には分子生物学が発展して微量のmRNAが測定できるようになり,脳内の多くのP450や3β-HSDなどのmRNAは卵巣や副腎皮質の1/100以下であるということが国際会議でどんどん報告されて,ほとんどのP450生化学者は,脳でのP450の働きには重要性がないと考え,研究から撤退していった.しかし私は脳P450のステロイド合成を目標としてきたし,今さら諦めたくない,脳の新しい情報伝達物質として脳内ステロイド学を発展させてみたいと決意して研究を進めた.「脳以外の内臓や末梢ではステロイドホルモンもペプチドホルモンも,情報伝達物質として勢力を二分しているのに,脳ではステロイドホルモンが合成されないとされているのは,間違いではないか」と私は考えていた.脳が精巣や卵巣の支配下にあるというのは本末転倒ではないか⁉ 成果がなかなか出ない時期が続いたが,10年間かけて抽出法や測定法の検出感度を1000倍上げることで,ようやく脳内ステロイドの実態を捉えることができるようになった.対象として神経内分泌学でよく使われる生殖中枢の視床下部ではなく,記憶中枢の海馬を使用した理由は,記憶の研究がやりたかったからだが,これが神経ステロイド作用を特定するのに適していた.神経内分泌学で多用される視床下部は,脳血液関門がゆるく,実験結果の解釈において血中に由来するT, E2, DHEAの影響が排除できないので,局所合成の実験には向いていなかった.
アフィニティーカラムや硫酸アンモニウム分画などで徹底的に精製した選択性の高いP450抗体(小南教授,山崎教授,原田教授の作製)を用いて海馬スライスを抗体染色し,P450scc, P450(17α),P450aromが神経にきれいに発現していることを発見した39–41, 48).性ホルモン合成に必要な他の酵素(17β-HSD type 1~4, 3β-HSD, 5α-reductaseなど)もすべて検出できた.mRNAやウエスタンブロットから,これらの濃度は精巣・卵巣などと比べて1/200~1/5000と大変低かったが,がっかりしなかった.なぜなら神経細胞は小さく,海馬の体積は0.1 mL程度で血管体積20 mLの1/200程度である.海馬は全身にステロイドを配達する内分泌器官でなく,海馬では地産地消なのでこれで十分なはずである.
3H標識した酵素の基質を海馬スライスとインキュベートして代謝させ,生成物をHPLCで精製して計測する合成解析を行い,T, DHT, E2などの合成経路を決定した.海馬の合成系の特徴は,精巣・卵巣の合成系の融合型であり,オスとメスの間で顕著な差がみられず,オスの脳でもE2が,そしてメスの脳でもT, DHTが合成される点である.これは,精巣・卵巣の性ステロイドは文字どおり生殖機能の調節を担っているが,脳合成の性ステロイドは性別であまり違わない神経伝達・神経可塑性の制御を行っていることを示していると考えている.
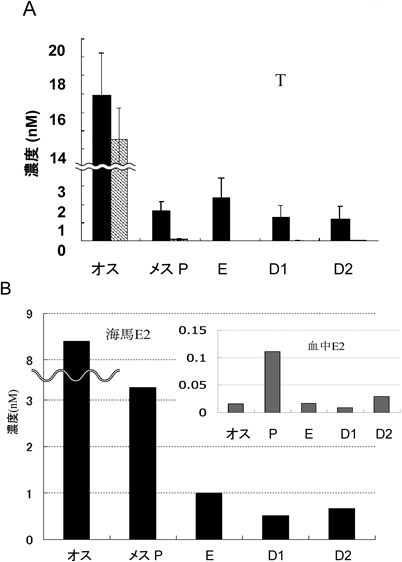
さらに,有機溶媒抽出後,順相HPLCで分画したステロイドを誘導体化して,高感度質量分析LC/MS/MSを行い,海馬中での性ホルモンの濃度を厳密に測定することに成功した44).その結果,成獣オスラットの海馬での濃度は,T(17 nM),DHT(7 nM),E2(8 nM)であった(図6).ここで血中から海馬に入ってくるTの寄与を除くために,精巣摘出したラットの実験を行って比較した結果,TからのDHTの合成経路では海馬内のTの8割は血中から供給され,2割は海馬内で合成されることがわかった.一方,海馬のDHT(7 nM)は血中のDHT(0.6 nM)より10倍多いことがわかった.面白いことに,メスでは海馬のE2(1 nM)は血中(0.1~0.01 nM)より10倍以上も高く,メスでも血中から海馬に入るE2の寄与は非常に低く,海馬内合成が主であることがわかった(図6).またE2はオスの方がメスより8倍も多く,性腺や血中での常識とは反対であった.メスの卵巣摘出ではE2はD1に近い値になる.
海馬における合成経路は,精巣・卵巣の融合型であり,オスとメスの間で顕著な差がみられず,オスの脳でもE2が,そしてメスの脳でもT, DHTが合成されるという,面白い現象が展開している.精巣・卵巣のような生殖機能の調節を担う部位と異なり,海馬合成の性ステロイドは性によらない神経伝達・神経可塑性の制御を行っているからではないかと考えている.さらに,P450(17α)とP450aromは神経細胞のミクロソームのみならず,シナプス後部(スパイン)内やシナプス後肥厚(PSD)にも存在することが免疫電子顕微鏡観察によって明らかとなった(図7)41).これはすなわち,E2が細胞体のみならずシナプスにおいても局所的に合成されていること(シナプス分泌)を示唆し,E2が神経シナプス伝達を短時間のうちにも制御可能であることを支持する.
海馬におけるE2の合成については,ドイツHamburg大のRune教授がたくさんの論文を発表している49–52).発達期の培養海馬スライスを使用して,海馬のE2産生がP450arom阻害剤の添加で24時間後に低下する事実から局所合成を見いだしている.最近はメス海馬ではE2産生があるが,オス海馬ではE2産生がないという不思議な結果を展開していて,我々と対立している.どちらが正しいかは乞うご期待であるが,これまで日本の複数の研究室がオスの海馬でE2産生を見いだしているので53),我々に分があるとみている.
小脳では発達期のプルキンエ細胞にもPROG, E2合成系があるという早大・筒井研の研究もある54).ところが成獣や老化ラットを調べたところ,小脳ではほぼP450aromがなくなるので,Tまでは合成するがE2合成能はほぼ存在しないと思われる42, 55).大脳皮質でも成獣以降ではP450aromの発現量は非常に少なかった.海馬と視床下部では成獣以降でもP450aromはしっかりと発現しているので,大きな差である.
男性ホルモンに関しては,面白い結果を得ている.若いラットに適度な運動を2週間させると,「海馬の男性ホルモンDHT合成が増加し,受容体ARを介して歯状回DGの神経新生が増える」のである56)(New York Times紙に紹介記事掲載).精巣を摘出したラットでも同様のDHT増加と神経新生増加の効果がある.これは海馬で合成される男性ホルモンが神経効果を示す新しい展開である.海馬ではE2は増えないし,ERα阻害剤での抑制効果もない.性ホルモン補充療法でなくても,運動すれば記憶力が良くなるのが事実であれば,老人の認知症予防には朗報になるであろう.
メスの海馬で,性周期に同期してスパイン密度が振動することは,McEwen研が見いだし,Principles in Neuroscienceにも図が載っている有名な現象である.彼らは血中から来るE2, PROGの濃度振動に誘導されると説明していたが,我々の測定によるとメス海馬のE2は血中の約30~100倍もあるので(図6)43),この説明は破綻している.メス海馬におけるPROGからE2を合成する酵素のmRNA発現量は性周期でまったく変動しなかった.したがって血中から供給されるPROGの濃度振動が海馬合成系に上乗せされて,海馬でのPROG, E2振動を引き起こしていることになる.これが海馬の作り出す性周期であり,これに同期してスパイン密度は,卵胞期(P)で高く,排卵期(E)で低下し,黄体期(D1)で上昇し,黄体期(D2)で低下し,Pで上昇する,…というように増減振動を示した43).これがメスで記憶能力(感情に依存する記憶能力)の性周期振動を引き起こすメカニズムであると考えている.
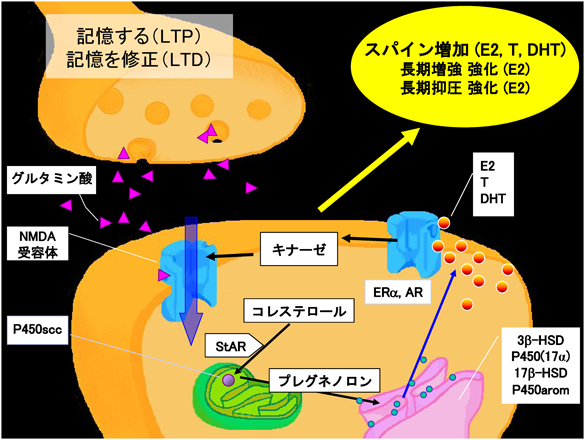
ここまでの話をまとめた男性女性ホルモンの局所合成と作用のモデルを図8に示す.
海馬のストレスセンサー機能においては,コルチコステロン(CORT,ストレス・ステロイド)が重要な影響を及ぼす.うつ病を引き起こすストレスの海馬神経作用分野では,Rockefeller大のMcEwen研をはじめとして非常に膨大な研究がある.海馬はCORT受容体GR(glucocorticoid receptor)が多いため,ストレスのセンサーでありかつ標的でもある.ストレスを受けると視床下部から脳下垂体に信号が伝わり,副腎皮質刺激ホルモンが分泌されて,副腎皮質でCORTが合成され,500 nM程度の高濃度CORTが血中に分泌されて脳に流入し,海馬や視床下部の機能抑制を起こすという回路で海馬の記憶機能が抑制される.おおよそ3週間の長期ストレスを受け続けるとうつ病になり,グルタミン酸神経が委縮する.ところが,うつ病研究以外の急性ストレスの研究は少ない57).我々は,意外なことに急性ストレス(1時間の高濃度500~1000 nM CORT作用)で,海馬のスパインは減少せず,むしろ増加することを見いだした58–60).このストレスは試験や会議の発表などの一時的なストレスに相当する.このような状況で,神経活動が抑制されず上昇することの説明には都合がよい.近年,体内時計の研究が爆発的に進んでいるが,低濃度30 nMの副腎皮質CORTは生体時計からの起床の出力信号であると考えられる.海馬神経スパインの24時間の睡眠覚醒リズムを調べたところ,起床時に大型スパインが増え,その後徐々に減少し,睡眠時にスパイン密度が最低になった61).この起床時のスパイン上昇は3時間以内に起こるのでnon-genomic経路でないと説明ができない.我々は海馬スライスを用いた実験によって「CORTがスパイン内受容体GRに結合し,LIMK, MAPK, PKA, PKCを活性化し,アクチン制御タンパク質をリン酸化して,アクチンの重合が起こり,スパインが増加」するというnon-genomic経路を見いだした59, 61).
我々は長年の努力の末に,海馬がCORTも合成していることの証明にようやく成功した62).P450c21が存在して,PROGからデオキシコルチコステロン(DOC)を経てCORTが生成する反応が進むことを見いだしたのである.P450c21のmRNA量は副腎皮質の約1/20,000と極端に少ないので,自由エネルギー計算を用いた最適プライマーの設計などの技法を開発してやっと,他の研究室が見いだせなかったmRNAを検出した42, 62).
脳はアルドステロンを合成するがCORTは合成しないという論文も出ていたが,これはELISA法という感度的に低い検出法を用いていた63).我々は副腎皮質摘出によって血中CORTをなくしたラットを用いて,順相HPLCなどで脂肪などのコンタミネーションを徹底的に除いた後に質量分析で測定した結果,海馬自身が7 nM CORTを産生していることを見いだした.これは性ステロイドと同じ程度の濃度である.このような低濃度のCORTが神経シナプスに作用するという研究は世界的になかったが,我々の実験では海馬スライスに添加するCORTの濃度を1 nMから10~30 nMへと上昇させると1時間で海馬スパイン密度が増加した.つまりCORTは神経ステロイドとしてシナプスの密度を維持する神経栄養因子であることがわかったのである.海馬合成CORTは副腎皮質CORTとは異なり,ストレス時には合成が上昇しないようである.なお,CORTは筋肉や精巣でも局所合成されており,その役割の解明が待たれる64).
中国の第二軍医大学・神経生物学研究所のY. Chen教授は我々より先にCORTの急性作用の研究に着手していた.講演のために訪問した際に,あえてこの先端的研究に取り組んだ動機を尋ねたところ,「戦場で兵士は大変な急性ストレスにさらされている.だからこの研究は大変重要なものだ」と,真面目に答えてくれた.McEwen研や他の大学でも最近はCORTの急性作用の研究が広がりを見せている.
内臓脂肪での局所ステロイド合成の例をあげる.内臓脂肪は男性・女性ホルモンを合成する重要な組織であることがわかってきた65).これは質量分析法の確立に関して我々と共同研究を行ってきたあすか製薬メディカル本間氏らの研究成果である.アディポネクチンと同様に,内臓脂肪由来の局所ステロイドが老化を防ぎ高血圧を防ぐ機能を示す長寿ホルモンといえるか興味深い.京都府立医大・河田研究室が行ってきた視床下部や海馬の性ホルモンの研究も寄与が大きい.
ここで,神経ステロイド研究勃興期の1980~2000年の状況をまとめておく.
神経ステロイドの命名者はパリの医学衛生学研究機構(INSERM)のBaulieu教授である(1989年ラスカー賞を受賞)46).Baulieu氏は,ラット・マウスの研究から,神経ステロイド(PREG, PROG)は脳内のグリアで合成されていて,血中から脳血液関門を透過して脳内に流入してくるものとは独立であると提唱した46, 66).しかし下流のDHEAは脳内の方が血中より濃度が高いにもかかわらず,合成酵素のP450(17α)が脳内に存在しないしDHEAも合成されないことから,DHEAの下流の男性・女性ホルモンは脳では合成されていないと主張した47).精巣摘出を行うと1日でTが脳から消えてしまうことも大きな理由であった47).脳内で作用する神経ステロイドとして硫酸プレグネノロン(PREGS)を取り上げ,これが非常に重要な神経ステロイドであり,記憶の活性化に働くという多くの論文がBaulieu研から発表されていた46, 47, 67).世界中でPREGSの存在を前提として,多くの作用に関する論文が発表された.PREGSを海馬に低濃度注入しただけで,脚の電気ショックを逃避する記憶・学習テストの成績が向上するとの結果68),海馬PREGS量は加齢とともに低下するが,老化したマウスにPREGSを投与すると空間学習能が回復する69)という結果,などである.しかし2004年になり,「PREGSが脳には存在しなかった」と,発見者であるBaulieu氏自身が報告して大騒動になった.それまでは加水分解後にプレグネノロンを測る間接的な検出法だったのが,質量分析でPREGSを直接測定すると,存在しなかったのである70–72).こうして「PREGS仮説」は崩壊してしまった.こうした混乱もあり,2005年のKarolinska大での私のセミナーの前置きで,Gustafsson教授は,“Neurosteroid is still a somewhat ambiguous field”といっていたくらいである73).Baulieu研の大きな発見は,アロプレグナノロンである.アロプレグナノロンは脳内で合成され,GABA受容体を強化してGABA神経の出力を上げて,脳機能を向上させる.さらにアロプレグナノロンはいろいろな場面で強い神経保護作用を示す.メスラットの方がオスよりずっと多くアロプレグナノロンを合成する74).
DHEA, T, DHT, E2が中枢の神経細胞で合成されているという確たる証拠は2000年までは得られておらず,これらはグリア細胞(アストログリアやオリゴデンドログリア)で合成され66, 75, 76),末梢神経が合成するPROGはミエリン形成に効いている,という論文が多かった77, 78).当時,培養し増やすことのできる脳細胞は生誕後すぐの初代培養のグリア細胞だけであったこと,神経細胞は分裂・増加しないので取り扱いが難しかったことなどが,一連の不明瞭な研究結果の原因であろう.グリア内合成は正しいが,神経内合成が見いだされた現在では,こちらの考え方が主流になっている.
14. ヒトの脳が合成する性ホルモンの働きを考える
さて,動物の話を続けてきたが,「ヒトの記憶における男性・女性ホルモンの機能も同じか?」と,講演後によく質問される.その答えは中国などの「宦官(かんがん)」から得られるのではないか.史記を書いた司馬遷,紙を発明した蔡倫,大航海をなしとげた鄭和,後宮から政治を牛耳った宦官などが歴史上有名な宦官である.宦官は,精巣の男性ホルモンがなくとも,海馬の男性ホルモンが発揮する知力で偉業をなしとげ政治を動かした.下層階級出身者においては出世するための人気職業でもあった.宦官は,後宮で権力を振るい政治をダメにするような負のイメージが強いが,これは権力抗争相手の官僚が悪口を一方的に書いているためである.実際には,官僚と同じく頭の切れる優秀な人たちが多い.中国に限らず,世界中に宦官は存在した.キリスト教国の東ローマ帝国の高位高官には大勢の宦官が登用されていた.これは一族を生産できない一代限りの官僚を登用することで,高級官僚の世襲を防ぎ,皇帝の権力が安定するからであった.70歳を越えれば,ヒトやラットの精巣での男性ホルモンの合成は大きく低下するが,精巣の合成能がなくなった高齢でも,ラット脳には性ホルモンの合成能が存在するので55),頑張れば海馬の性ホルモン機能は中年の状態を保てるかもしれない.現在「老化したラット海馬の神経スパインが男性ホルモン補充で回復する」という論文・総説を書いている.今の世の中,認知症とアンチエイジングが重要なトピックだが,老化しても海馬の記憶力を維持できるかどうかが大きな課題である.順天堂大と帝京大の大学病院の外来では,加齢男性の性腺機能低下症候群(LOH症候群)の方々にテストステロン補充療法が行われており,これら患者さんの認知能力の改善を観察するのも課題の一つになっている.テストステロン補充療法が男性認知症の効果的な治療法になることも期待している.
謝辞Acknowledgments
以上の研究は,川戸研の学生や研究員であった,北條・畑中・長谷川・向井・村上・石井・肥後・大石・三橋・小松崎・荻上・釣木澤・木本・棟朝・高橋・岡本の各博士や,小南・池田・服部・井上・堀田・加藤・小島をはじめとする大勢の修士が中心となって進めたものです.科学技術振興機構のCREST, Bioinformatics, 科学技術振興調整費のプロジェクトに支えられた成果でもある.2000年ごろに社会をゆるがせた環境ホルモン問題のおかげで,脳のエストロゲン作用の研究は大きく進展した.本稿の詳しい資料は,川戸研ウェブサイトhttp://kawato-glia.sakura.ne.jpにある.
引用文献References
1) Luine, V. & Frankfurt, M. (2015) Horm. Behav., 74, 1–3.
2) Lynch, G. & Baudry, M. (2015) Brain Res., 1621, 1–4.
3) Coen, C.W. (2015) J. Endocrinol., 226, E3–E6.
4) Casadesus, G. & Gustafsson, J.-Å. (2010) Biochim. Biophys. Acta, 1800, 1029.
5) Mukai, H., Kimoto, T., Hojo, Y., Kawato, S., Murakami, G., Higo, S., Hatanaka, Y., & Ogiue-Ikeda, M. (2010) Biochim. Biophys. Acta, 1800, 1030–1044.
6) Hojo, Y., Munetomo, A., Mukai, H., Ikeda, M., Sato, R., Hatanaka, Y., Murakami, G., Komatsuzaki, Y., Kimoto, T., & Kawato, S. (2015) Horm. Behav., 74, 149–156.
7) Hojo, Y., Murakami, G., Mukai, H., Higo, S., Hatanaka, Y., Ogiue-Ikeda, M., Ishii, H., Kimoto, T., & Kawato, S. (2008) Mol. Cell. Endocrinol., 290, 31–43.
8) Hojo, Y., Higo, S., Kawato, S., Hatanaka, Y., Ooishi, Y., Murakami, G., Ishii, H., Komatsuzaki, Y., Ogiue-Ikeda, M., Mukai, H., & Kimoto, T. (2011) Front. Endocrinol. (Lausanne), 2, 43.
9) Mukai, H., Takata, N., Ishii, H.T., Tanabe, N., Hojo, Y., Furukawa, A., Kimoto, T., & Kawato, S. (2006) Neuroscience, 138, 757–764.
10) Mukai, H., Tsurugizawa, T., Murakami, G., Kominami, S., Ishii, H., Ogiue-Ikeda, M., Takata, N., Tanabe, N., Furukawa, A., Hojo, Y., Ooishi, Y., Morrison, J.H., Janssen, W.G., Rose, J.A., Chambon, P., Kato, S., Izumi, S., Yamazaki, T., Kimoto, T., & Kawato, S. (2007) J. Neurochem., 100, 950–967.
11) Hasegawa, Y., Hojo, Y., Kojima, H., Ikeda, M., Hotta, K., Sato, R., Ooishi, Y., Yoshiya, M., Chung, B.C., Yamazaki, T., & Kawato, S. (2015) Brain Res., 1621, 147–161.
12) Hatanaka, Y., Hojo, Y., Mukai, H., Murakami, G., Komatsuzaki, Y., Kim, J., Ikeda, M., Hiragushi, A., Kimoto, T., & Kawato, S. (2015) Brain Res., 1621, 121–132.
13) Tsurugizawa, T., Mukai, H., Tanabe, N., Murakami, G., Hojo, Y., Kominami, S., Mitsuhashi, K., Komatsuzaki, Y., Morrison, J.H., Janssen, W.G., Kimoto, T., & Kawato, S. (2005) Biochem. Biophys. Res. Commun., 337, 1345–1352.
14) Mukai, H., Hatanaka, Y., Mitsuhashi, K., Hojo, Y., Komatsuzaki, Y., Sato, R., Murakami, G., Kimoto, T., & Kawato, S. (2011) Cereb. Cortex, 21, 2704–2711.
15) Toran-Allerand, C.D., Guan, X., MacLusky, N.J., Horvath, T.L., Diano, S., Singh, M., Connolly, E.S. Jr., Nethrapalli, I.S., & Tinnikov, A.A. (2002) J. Neurosci., 22, 8391–8401.
16) Hart, S.A., Patton, J.D., & Woolley, C.S. (2001) J. Comp. Neurol., 440, 144–155.
17) Murakami, G., Hojo, Y., Ogiue-Ikeda, M., Mukai, H., Chambon, P., Nakajima, K., Ooishi, Y., Kimoto, T., & Kawato, S. (2015) Brain Res., 1621, 133–146.
18) Gu, Q., Korach, K.S., & Moss, R.L. (1999) Endocrinology, 140, 660–666.
19) Kos, M., Denger, S., Reid, G., Korach, K.S., & Gannon, F. (2002) J. Mol. Endocrinol., 29, 281–286.
20) Revankar, C.M., Cimino, D.F., Sklar, L.A., Arterburn, J.B., & Prossnitz, E.R. (2005) Science, 307, 1625–1630.
21) Otto, C., Fuchs, I., Kauselmann, G., Kern, H., Zevnik, B., Andreasen, P., Schwarz, G., Altmann, H., Klewer, M., Schoor, M., Vonk, R., & Fritzemeier, K.H. (2009) Biol. Reprod., 80, 34–41.
22) Kim, J., Szinte, J.S., Boulware, M.I., & Frick, K.M. (2016) J. Neurosci., 36, 3309–3321.
23) Razandi, M., Pedram, A., Greene, G.L., & Levin, E.R. (1999) Mol. Endocrinol., 13, 307–319.
24) Razandi, M., Alton, G., Pedram, A., Ghonshani, S., Webb, P., & Levin, E.R. (2003) Mol. Cell. Biol., 23, 1633–1646.
25) Hatanaka, Y., Mukai, H., Mitsuhashi, K., Hojo, Y., Murakami, G., Komatsuzaki, Y., Sato, R., & Kawato, S. (2009) Biochem. Biophys. Res. Commun., 381, 728–732.
26) MacLusky, N.J., Hajszan, T., & Leranth, C. (2004) Endocrinology, 145, 4154–4161.
27) Leranth, C., Hajszan, T., & MacLusky, N.J. (2004) J. Neurosci., 24, 495–499.
28) Kumamoto, E. (2015)日本Men’s Health医学会News Letter, 13, 5–8.
29) Yu, J., Akishita, M., Eto, M., Ogawa, S., Son, B.K., Kato, S., Ouchi, Y., & Okabe, T. (2010) Endocrinology, 151, 1822–1828.
30) Ota, H., Akishita, M., Akiyoshi, T., Kahyo, T., Setou, M., Ogawa, S., Iijima, K., Eto, M., & Ouchi, Y. (2012) PLoS ONE, 7, e29598.
31) Foy, M.R., Xu, J., Xie, X., Brinton, R.D., Thompson, R.F., & Berger, T.W. (1999) J. Neurophysiol., 81, 925–929.
32) Kramar, E.A., Chen, L.Y., Brandon, N.J., Rex, C.S., Liu, F., Gall, C.M., & Lynch, G. (2009) J. Neurosci., 29, 12982–12993.
33) Ito, K., Skinkle, K.L., & Hicks, T.P. (1999) J. Physiol., 515, 209–220.
34) Ooishi, Y., Mukai, H., Hojo, Y., Murakami, G., Hasegawa, Y., Shindo, T., Morrison, J.H., Kimoto, T., & Kawato, S. (2012) Cereb. Cortex, 22, 926–936.
35) Grassi, S., Tozzi, A., Costa, C., Tantucci, M., Colcelli, E., Scarduzio, M., Calabresi, P., & Pettorossi, V.E. (2011) Neuroscience, 192, 67–73.
36) Pettorossi, V.E., Di Mauro, M., Scarduzio, M., Panichi, R., Tozzi, A., Calabresi, P., & Grassi, S. (2013) Physiol. Rep., 1, e00185.
37) Tanaka, M. & Sokabe, M. (2012) Neuropharmacology, 62, 2373–2387.
38) Ishii, H., Tsurugizawa, T., Ogiue-Ikeda, M., Asashima, M., Mukai, H., Murakami, G., Hojo, Y., Kimoto, T., & Kawato, S. (2007) Neuroscientist, 13, 323–334.
39) Kimoto, T., Tsurugizawa, T., Ohta, Y., Makino, J., Tamura, H., Hojo, Y., Takata, N., & Kawato, S. (2001) Endocrinology, 142, 3578–3589.
40) Kawato, S., Hojo, Y., & Kimoto, T. (2002) Methods Enzymol., 357, 241–249.
41) Hojo, Y., Hattori, T.A., Enami, T., Furukawa, A., Suzuki, K., Ishii, H.T., Mukai, H., Morrison, J.H., Janssen, W.G., Kominami, S., Harada, N., Kimoto, T., & Kawato, S. (2004) Proc. Natl. Acad. Sci. USA, 101, 865–870.
42) Kimoto, T., Ishii, H., Higo, S., Hojo, Y., & Kawato, S. (2010) Endocrinology, 151, 5795–5806.
43) Kato, A., Hojo, Y., Higo, S., Komatsuzaki, Y., Murakami, G., Yoshino, H., Uebayashi, M., & Kawato, S. (2013) Front. Neural Circuits, 7, 149.
44) Hojo, Y., Higo, S., Ishii, H., Ooishi, Y., Mukai, H., Murakami, G., Kominami, T., Kimoto, T., Honma, S., Poirier, D., & Kawato, S. (2009) Endocrinology, 150, 5106–5112.
45) Le Goascogne, C., Sananes, N., Gouezou, M., Takemori, S., Kominami, S., Baulieu, E.E., & Robel, P. (1991) J. Reprod. Fertil., 93, 609–622.
46) Baulieu, E.E. (1997) Recent Prog. Horm. Res., 52, 1–32.
47) Baulieu, E.E. & Robel, P. (1998) Proc. Natl. Acad. Sci. USA, 95, 4089–4091.
48) Shibuya, K., Takata, N., Hojo, Y., Furukawa, A., Yasumatsu, N., Kimoto, T., Enami, T., Suzuki, K., Tanabe, N., Ishii, H., Mukai, H., Takahashi, T., Hattori, T.A., & Kawato, S. (2003) Biochim. Biophys. Acta, 1619, 301–316.
49) Prange-Kiel, J., Wehrenberg, U., Jarry, H., & Rune, G.M. (2003) Hippocampus, 13, 226–234.
50) Kretz, O., Fester, L., Wehrenberg, U., Zhou, L., Brauckmann, S., Zhao, S., Prange-Kiel, J., Naumann, T., Jarry, H., Frotscher, M., & Rune, G.M. (2004) J. Neurosci., 24, 5913–5921.
51) Prange-Kiel, J., Fester, L., Zhou, L., Lauke, H., Carretero, J., & Rune, G.M. (2006) Hippocampus, 16, 464–471.
52) Vierk, R., Glassmeier, G., Zhou, L., Brandt, N., Fester, L., Dudzinski, D., Wilkars, W., Bender, R.A., Lewerenz, M., Gloger, S., Graser, L., Schwarz, J., & Rune, G.M. (2012) J. Neurosci., 32, 8116–8126.
53) Munetsuna, E., Hojo, Y., Hattori, M., Ishii, H., Kawato, S., Ishida, A., Kominami, S.A., & Yamazaki, T. (2009) Endocrinology, 150, 4260–4269.
54) Sakamoto, H., Ukena, K., & Tsutsui, K. (2001) J. Neurosci., 21, 6221–6232.
55) Munetomo, A., Hojo, Y., Higo, S., Kato, A., Yoshida, K., Shirasawa, T., Shimizu, T., Barron, A., Kimoto, T., & Kawato, S. (2015) J. Physiol. Sci., 65, 253–263.
56) Okamoto, M., Hojo, Y., Inoue, K., Matsui, T., Kawato, S., McEwen, B.S., & Soya, H. (2012) Proc. Natl. Acad. Sci. USA, 109, 13100–13105.
57) Takahashi, T., Kimoto, T., Tanabe, N., Hattori, T.A., Yasumatsu, N., & Kawato, S. (2002) J. Neurochem., 83, 1441–1451.
58) Komatsuzaki, Y., Murakami, G., Tsurugizawa, T., Mukai, H., Tanabe, N., Mitsuhashi, K., Kawata, M., Kimoto, T., Ooishi, Y., & Kawato, S.R. (2005) Biochem. Biophys. Res. Commun., 335, 1002–1007.
59) Komatsuzaki, Y., Hatanaka, Y., Murakami, G., Mukai, H., Hojo, Y., Saito, M., Kimoto, T., & Kawato, S. (2012) PLoS ONE, 7, e34124.
60) Yoshiya, M., Komatsuzaki, Y., Hojo, Y., Ikeda, M., Mukai, H., Hatanaka, Y., Murakami, G., Kawata, M., Kimoto, T., & Kawato, S. (2013) Front. Neural Circuits, 69, 1031–1055.
61) Ikeda, M., Hojo, Y., Komatsuzaki, Y., Okamoto, M., Kato, A., Takeda, T., & Kawato, S. (2015) J. Endocrinol., 226, M13–M27.
62) Higo, S., Hojo, Y., Ishii, H., Komatsuzaki, Y., Ooishi, Y., Murakami, G., Mukai, H., Yamazaki, T., Nakahara, D., Barron, A., Kimoto, T., & Kawato, S. (2011) PLoS ONE, 6, e21631.
63) Gomez-Sanchez, E.P., Ahmad, N., Romero, D.G., & Gomez-Sanchez, C.E. (2005) Am. J. Physiol. Endocrinol. Metab., 288, E342–E346.
64) Maeda, N., Tanaka, E., Suzuki, T., Okumura, K., Nomura, S., Miyasho, T., Haeno, S., & Yokota, H. (2013) J. Biochem., 153, 63–71.
65) Kinoshita, T., Honma, S., Shibata, Y., Yamashita, K., Watanabe, Y., Maekubo, H., Okuyama, M., Takashima, A., & Takeshita, N. (2014) J. Clin. Endocrinol. Metab., 99, 1339–1347.
66) Jung-Testas, I., Hu, Z.Y., Baulieu, E.E., & Robel, P. (1989) Endocrinology, 125, 2083–2091.
67) Corpechot, C., Robel, P., Axelson, M., Sjovall, J., & Baulieu, E.E. (1981) Proc. Natl. Acad. Sci. USA, 78, 4704–4707.
68) Flood, J.F., Morley, J.E., & Roberts, E. (1995) Proc. Natl. Acad. Sci. USA, 92, 10806–10810.
69) Vallee, M., Mayo, W., Darnaudery, M., Corpechot, C., Young, J., Koehl, M., Le Moal, M., Baulieu, E.E., Robel, P., & Simon, H. (1997) Proc. Natl. Acad. Sci. USA, 94, 14865–14870.
70) Liu, S., Sjovall, J., & Griffiths, W.J. (2003) Anal. Chem., 75, 5835–5846.
71) Liere, P., Pianos, A., Eychenne, B., Cambourg, A., Liu, S., Griffiths, W., Schumacher, M., Sjovall, J., & Baulieu, E.E. (2004) J. Lipid Res., 45, 2287–2302.
72) Higashi, T., Sugitani, H., Yagi, T., & Shimada, K. (2003) Biol. Pharm. Bull., 26, 709–711.
73) Warner, M. & Gustafsson, J.A. (2006) Steroids, 71, 91–95.
74) Hojo, Y., Okamoto, M., Kato, A., Higo, S., Sakai, F., Soya, H., Yamazaki, T., & Kawato, S. (2014) J. Steroids Horm. Sci., Article S4.
75) Zwain, I.H. & Yen, S.S. (1999) Endocrinology, 140, 880–887.
76) Zwain, I.H. & Yen, S.S. (1999) Endocrinology, 140, 3843–3852.
77) Koenig, H.L., Schumacher, M., Ferzaz, B., Thi, A.N., Ressouches, A., Guennoun, R., Jung-Testas, I., Robel, P., Akwa, Y., & Baulieu, E.E. (1995) Science, 268, 1500–1503.
78) Schumacher, M., Guennoun, R., Robert, F., Carelli, C., Gago, N., Ghoumari, A., Gonzalez Deniselle, M.C., Gonzalez, S.L., Ibanez, C., Labombarda, F., Coirini, H., Baulieu, E.E., & De Nicola, A.F. (2004) Growth Horm. IGF Res., 14(Suppl A), S18–S33.
著者紹介Author Profile
 川戸 佳(かわと すぐる)
川戸 佳(かわと すぐる)順天堂大学大学院医学研究科泌尿器外科学客員教授.理博.
略歴1969年京都大学入学.74年京都大学理学部物理学科卒業.同年東京大学大学院理学系研究科物理学専攻入学.79年同博士課程修了(理学博士).同年スイス,チュ−リッヒ工科大学生化学科助手.84年東京大学教養学部物理学教室助教授.92年東京大学大学院総合文化研究科広域科学専攻教授(大学院理学系研究科物理学専攻教授兼担).2015年東京大学定年退職(名誉教授).同年順天堂大学大学院医学研究科.
研究テーマと抱負自分の意志(勉強・運動)で,海馬の男性・女性ホルモンを合成する機構の解明.男性ホルモン補充療法による,記憶能力のアンチエイジング法・認知症を改善する方法の解明.
ウェブサイトhttp://kawato-glia.sakura.ne.jp/