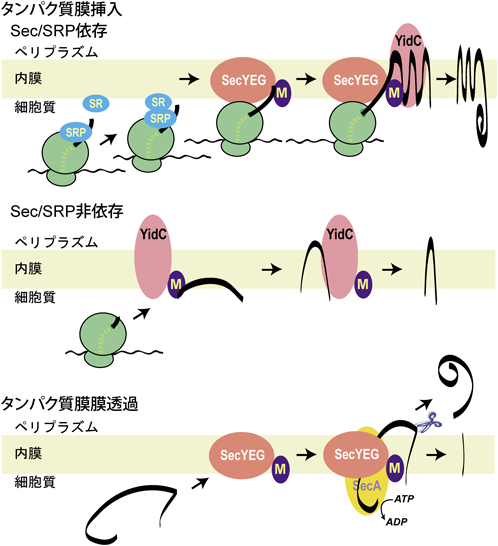
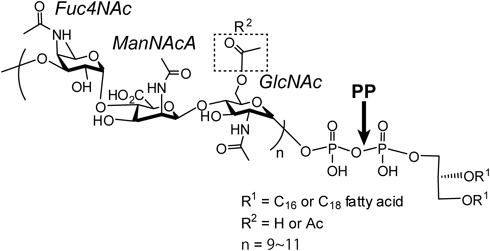
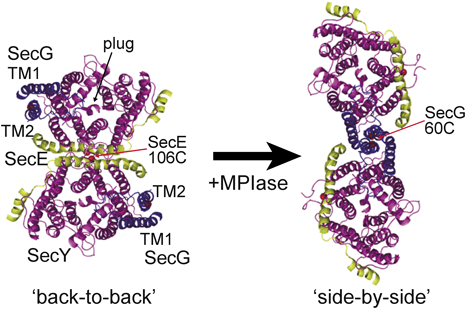
1) Endo, Y. & Nishiyama, K. (2015) Med. Res. Archives, 2, 1–24.
3) Denks, K., Vogt, A., Sachelaru, I., Petriman, N.A., Kudva, R., & Koch, H.G. (2014) Mol. Membr. Biol., 31, 58–84.
5) Geller, B.L. & Wickner, W. (1985) J. Biol. Chem., 260, 13281–13285.
6) Nishiyama, K., Ikegami, A., Moser, M., Schiltz, E., Tokuda, H., & Muller, M. (2006) J. Biol. Chem., 281, 35667–35676.
7) Kawashima, Y., Miyazaki, E., Muller, M., Tokuda, H., & Nishiyama, K. (2008) J. Biol. Chem., 283, 24489–24496.
8) Serek, J., Bauer-Manz, G., Struhalla, G., van den Berg, L., Kiefer, D., Dalbey, R., & Kuhn, A. (2004) EMBO J., 23, 294–301.
9) Nishiyama, K., Maeda, M., Abe, M., Kanamori, T., Shimamoto, K., Kusumoto, S., Ueda, T., & Tokuda, H. (2010) Biochem. Biophys. Res. Commun., 394, 733–736.
10) Nishiyama, K., Maeda, M., Yanagisawa, K., Nagase, R., Komura, H., Iwashita, T., Yamagaki, T., Kusumoto, S., Tokuda, H., & Shimamoto, K. (2012) Nat. Commun., 3, 1260.
11) Welte, T., Kudva, R., Kuhn, P., Sturm, L., Braig, D., Muller, M., Warscheid, B., Drepper, F., & Koch, H.G. (2012) Mol. Biol. Cell, 23, 464–479.
12) Moser, M., Nagamori, S., Huber, M., Tokuda, H., & Nishiyama, K. (2013) Proc. Natl. Acad. Sci. USA, 110, 9734–9739.
14) Nishiyama, K., Mizushima, S., & Tokuda, H. (1993) EMBO J., 12, 3409–3415.
15) Kumazaki, K., Chiba, S., Takemoto, M., Furukawa, A., Nishiyama, K., Sugano, Y., Mori, T., Dohmae, N., Hirata, K., Nakada-Nakura, Y., Maturana, A.D., Tanaka, Y., Mori, H., Sugita, Y., Arisaka, F., Ito, K., Ishitani, R., Tsukazaki, T., & Nureki, O. (2014) Nature, 509, 516–520.