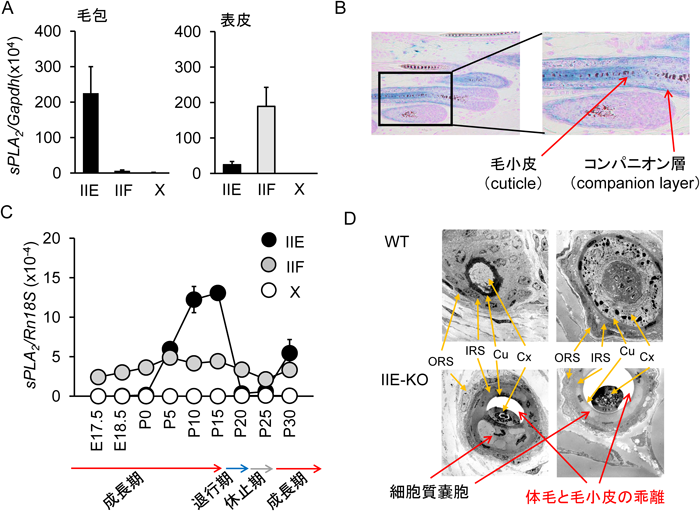
1) Murakami, M., Sato, H., Miki, Y., Yamamoto, K., & Taketomi, Y. (2015) J. Lipid Res., 56, 1248–1261.
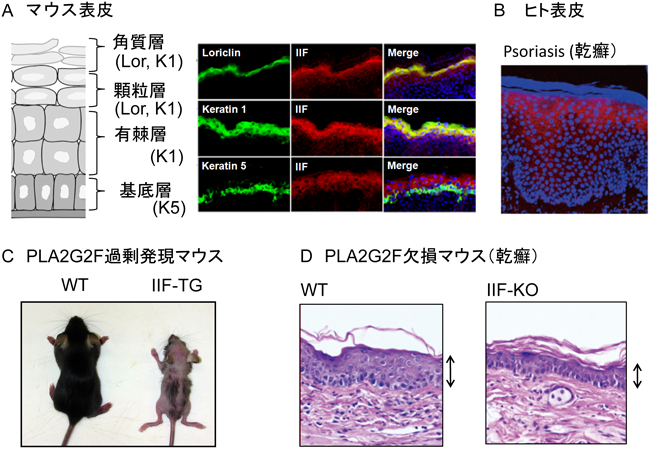
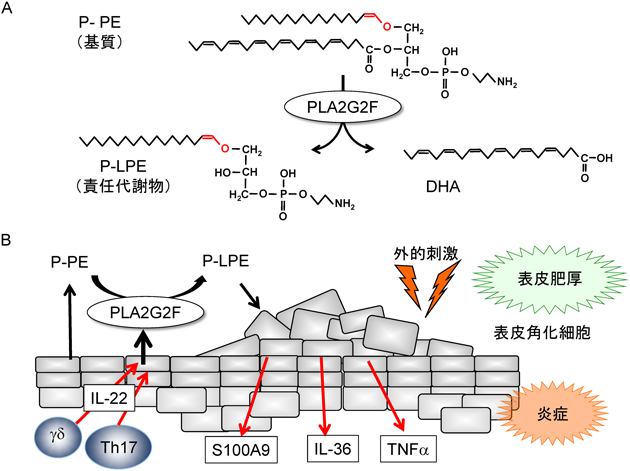
2) Yamamoto, K., Miki, Y., Sato, M., Taketomi, Y., Nishito, Y., Taya, C., Muramatsu, K., Ikeda, K., Nakanishi, H., Taguchi, R., Kambe, N., Kabashima, K., Lambeau, G., Gelb, M.H., & Murakami, M. (2015) J. Exp. Med., 212, 1901–1919.
3) Yamamoto, K., Miki, Y., Sato, H., Nishito, Y., Gelb, M.H., Taketomi, Y., & Murakami, M. (2016) J. Biol. Chem., 291, 15602–15613.
4) Fluhr, J.W., Mao-Qiang, M., Brown, B.E., Hachem, J.P., Moskowitz, D.G., Demerjiam, M., Haftek, M., Serre, G., Crumrine, D., Mauro, T.M., Elias, P.M., & Feingold, K.R. (2004) J. Invest. Dermatol., 123, 140–151.
5) Yamamoto, K., Taketomi, Y., Isogai, Y., Miki, Y., Sato, H., Masuda, S., Nishito, Y., Morioka, K., Ishimoto, Y., Suzuki, N., Yokoya, Y., Hanasaki, K., Ishikawa, Y., Ishii, T., Kobayashi, T., Fukami, K., Ikeda, K., Nakanishi, H., Taguchi, R., & Murakami, M. (2011) J. Biol. Chem., 286, 11616–11631.
6) Grass, D.S., Felkner, R.H., Chiang, M.Y., Wallace, R.E., Navelainen, T.J., Bennett, C.F., & Swanson, M.E. (1996) J. Clin. Invest., 97, 2233–2241.
7) Tortola, L., Rosenwald, E., Abel, B., Blumberg, H., Schafer, M., Coyle, A.J., Renauld, J.C., Werner, S., Kisielow, J., & Kopf, M. (2012) J. Clin. Invest., 122, 3965–3976.
8) Miki, Y., Yamamoto, K., Taketomi, Y., Sato, H., Shimo, K., Kobayashi, T., Ishikawa, Y., Ishii, T., Nakanishi, H., Ikeda, K., Taguchi, R., Kabashima, K., Arita, M., Arai, H., Lambeau, G., Bollinger, J.M., Hara, S., Gelb, M.H., & Murakami, M. (2012) J. Exp. Med., 210, 1217–1234.
9) Modi, B.G., Neustadter, J., Binda, E., Lewis, J., Filler, R.B., Roberts, S.J., Kwong, B.Y., Reddy, S., Overton, J.D., Galan, A., Tigelaar, R., Cai, L., Fu, P., Shlomchik, M., Kaplan, D.H., Hayday, A., & Girardi, M. (2012) Science, 335, 104–108.
11) Sato, H., Taketomi, Y., Ushida, A., Isogai, Y., Kojima, T., Hirabayashi, T., Miki, Y., Yamamoto, K., Nishito, Y., Kobayashi, T., Ikeda, K., Taguchi, R., Hara, S., Ida, S., Miyamoto, Y., Watanabe, M., Baba, H., Miyata, K., Oike, Y., Gelb, M.H., & Murakami, M. (2014) Cell Metab., 20, 119–132.
12) MacPhee, M., Chepenik, K.P., Liddell, R.A., Nelson, K.K., Siracusa, L.D., & Buchberg, A.M. (1995) Cell, 81, 957–966.