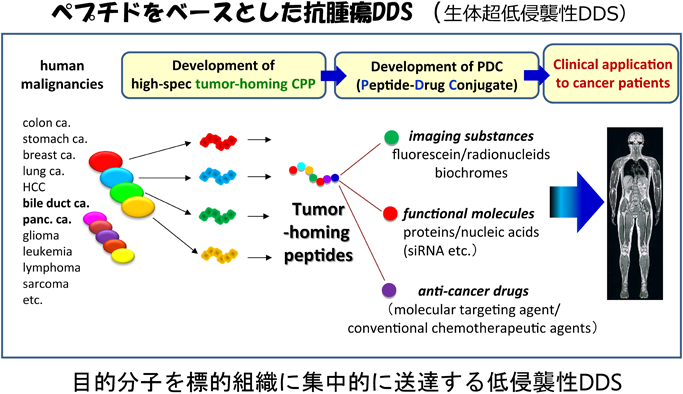
テイラード・アプリケーションを目指したがん細胞選択的吸収性ペプチドの開発Development of tumor-lineage homing peptide for their tailored application to diverse malignancies
新潟大学大学院医歯学総合研究科・分子細胞病理学Division of Molecular and Cellular Pathology, Niigata University Graduate School of Medical and Dental Sciences ◇ 951–8510 新潟市中央区旭町通1–757 ◇ 1–757 Asahimachi-dori, Chuo-ku, Niigata 951–8510, Japan