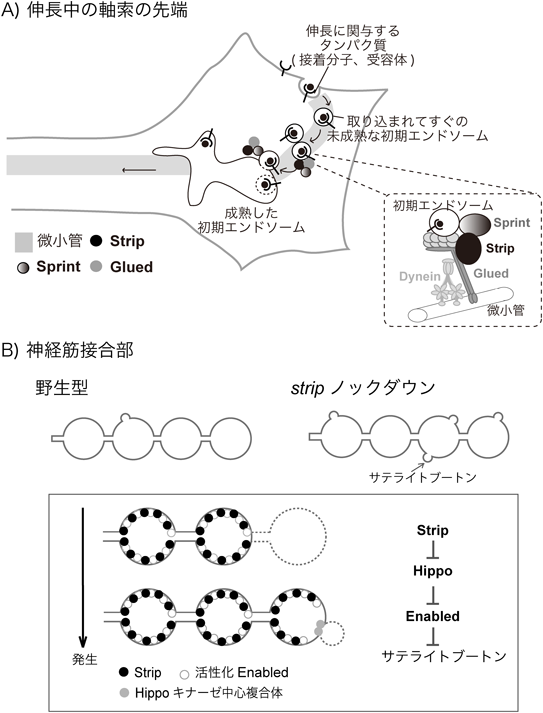
小胞輸送・微小管安定性・Hippoシグナル経路に関わるハブタンパク質StripStrip, a hub protein in giant protein complex, regulates vesicle transport, microtubule stability and hippo signaling during neural development
1 東京慈恵会医科大学熱帯医学講座Department of Tropical Medicine, The Jikei University School of Medicine ◇ 〒105–8461 東京都港区西新橋3–25–8 ◇ 3–25–8 Nishi-Shimbashi, Minato-ku, Tokyo, 105–8461, Japan
2 広島大学大学院理学研究科生物科学専攻細胞生物学研究室Department of Biological Science, Graduate School of Science, Hiroshima University ◇ 〒739–8526 東広島市鏡山1–3–1 ◇ 1–3–1 Kagamiyama, Higashi-Hiroshima, Hiroshima 739–8526, Japan