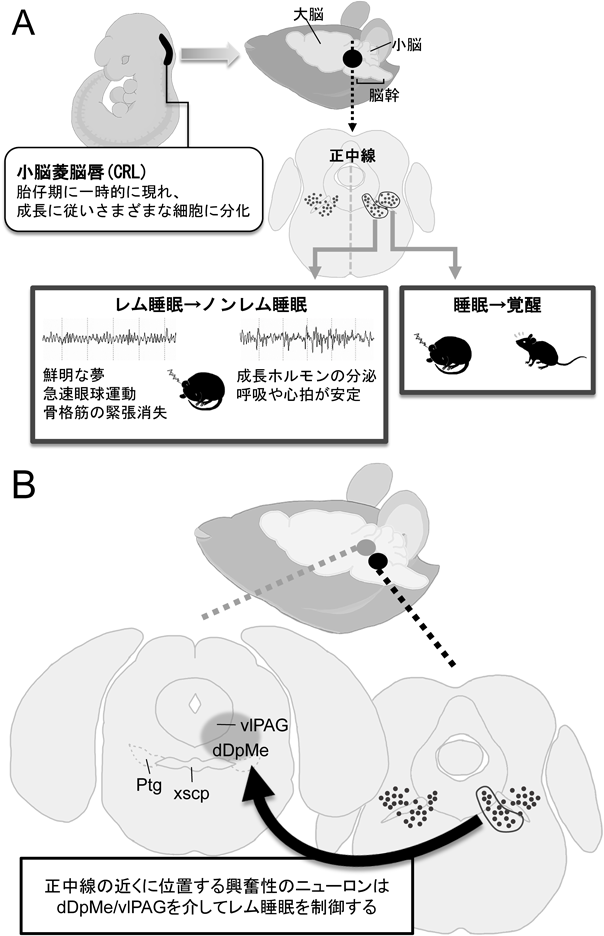
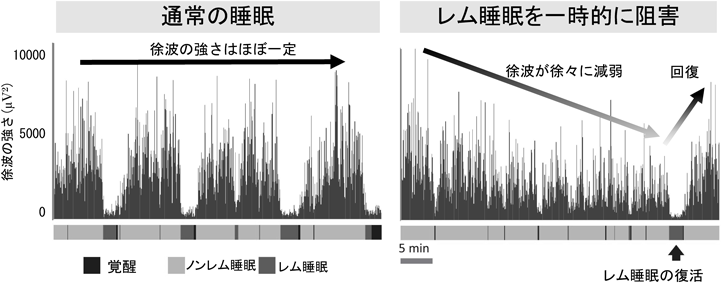
レム睡眠のメカニズムと生理的意義The function and mechanisms of REM sleep
1 筑波大学国際統合睡眠医科学研究機構(WPI-IIIS)International Institute for Integrative Sleep Medicine (WPI-IIIS), University of Tsukuba ◇ 〒305–8575 茨城県つくば市天王台1–1–1 筑波大学睡眠医科学研究棟 ◇ International Institute for Integrative Sleep Medicine (WPI-IIIS), University of Tsukuba; 1–1–1 Tennodai, Tsukuba, Ibaraki, 305–8575, Japan
2 筑波大学人間総合科学研究科フロンティア医科学専攻Master’s Program of Medical Science, Graduate School of Comprehensive Human Sciences, University of Tsukuba ◇ 〒305–8575 茨城県つくば市天王台1–1–1 ◇ University of Tsukuba; 1–1–1 Tennodai, Tsukuba, Ibaraki, 305–8575, Japan