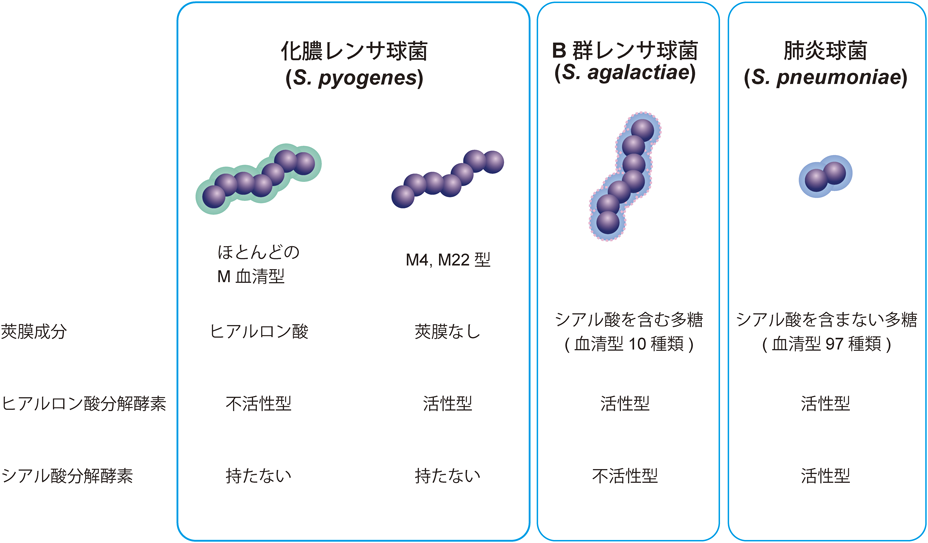
病原レンサ球菌の感染過程における莢膜糖鎖と糖鎖分解酵素の役割Role of streptococcal polysaccharide capsules and glycosidases in the pathogenesis
大阪大学大学院歯学研究科口腔細菌学教室Oral and Molecular Microbiology, Osaka University, Graduate School of Dentistry ◇ 〒565–0871 大阪府吹田市山田丘1–8 ◇ 1–8, Yamadaoka, Suita, Osaka 565–0871, Japan