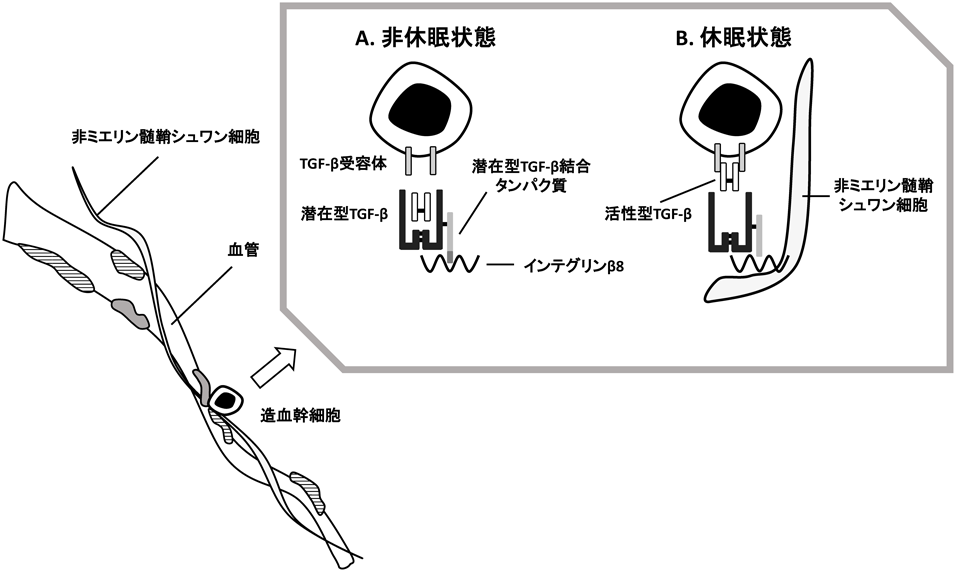
造血幹細胞の維持と誘導The hematopoietic stem cell and its niche
1 東京大学医科学研究所幹細胞治療研究センター幹細胞治療部門Center for Stem Cell Biology and Regenerative Medicine, The Institute of Medical Science, The University of Tokyo ◇ 〒108–8639 東京都港区白金台4–6–1 ◇ 4–6–1 Shirokanedai, Minato-ku, Tokyo 108–8639, Japan
2 東京大学医科学研究所先端医療研究センター分子療法分野Division of Molecular Therapy, Advanced Clinical Research Center, The Institute of Medical Science, The University of Tokyo ◇ 〒108–8639 東京都港区白金台4–6–1 ◇ 4–6–1 Shirokanedai, Minato-ku, Tokyo 108–8639, Japan