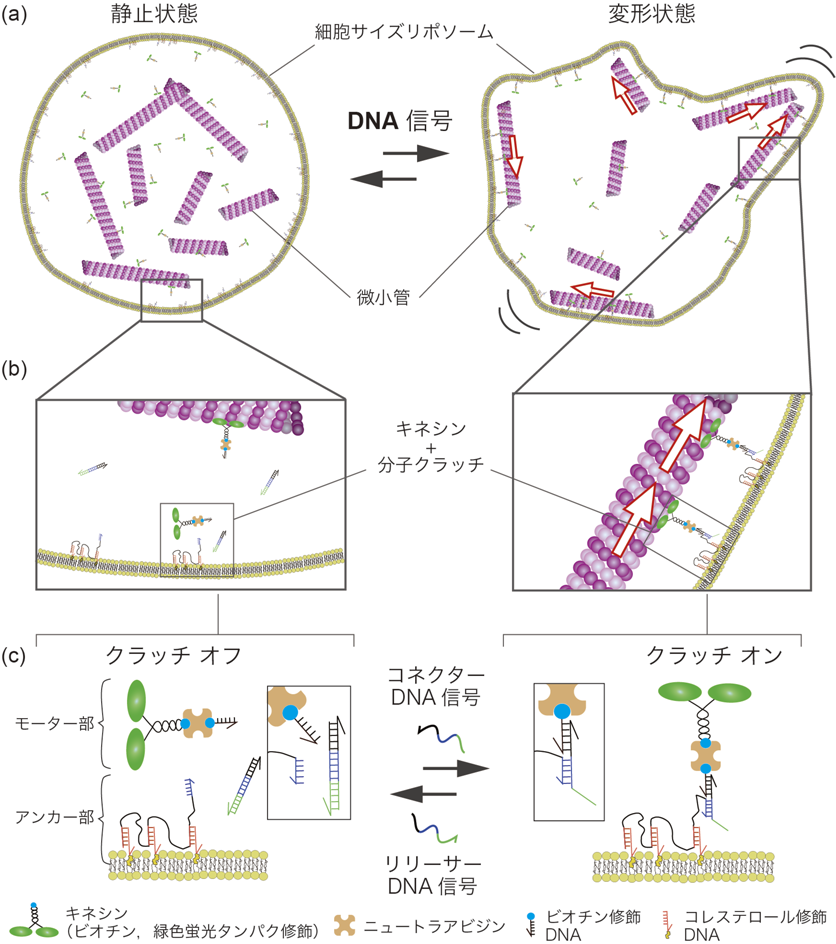
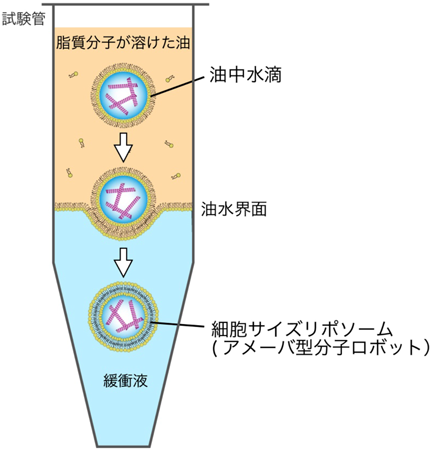
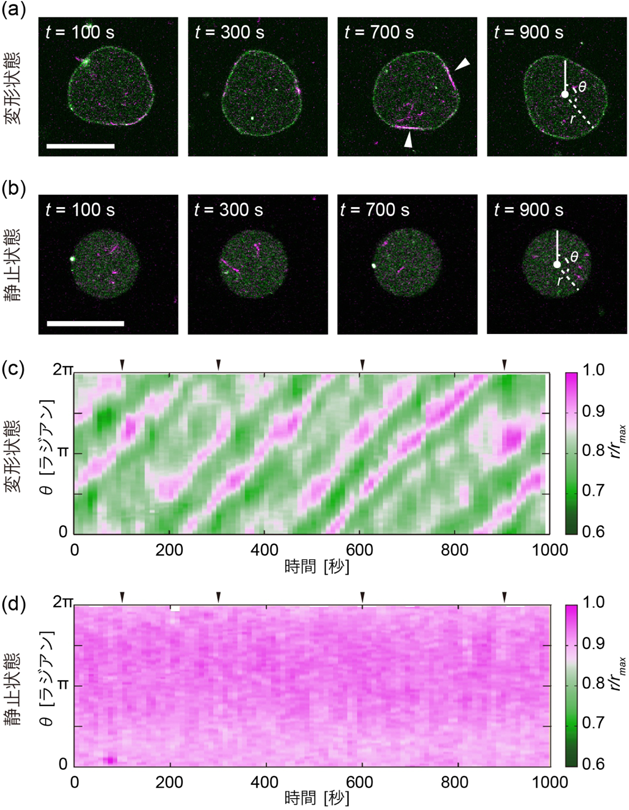
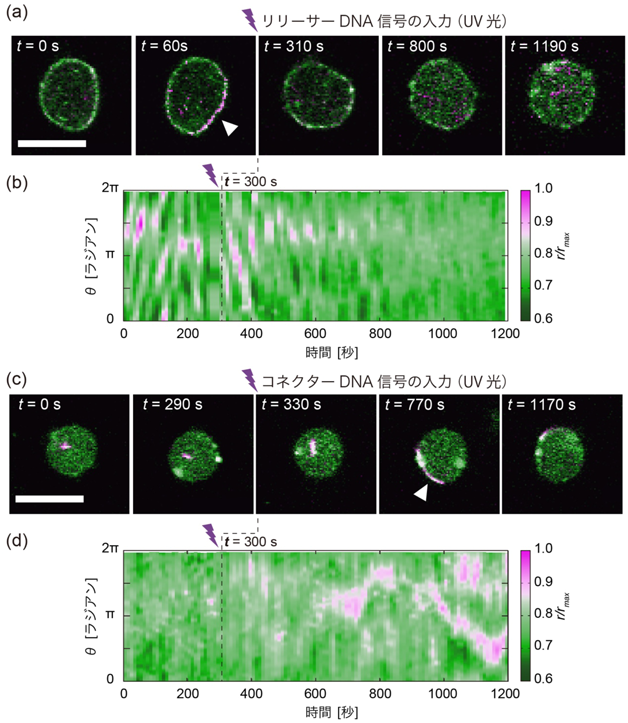
分子ロボティクス:アメーバ型分子ロボットの開発Molecular Robotics: Development of amoeba-type molecular robot
東北大学大学院工学研究科ロボティクス専攻Department of Robotics, Graduate school of Engineering, Tohoku University ◇ 〒980–8579 仙台市青葉区荒巻字青葉 6–6–01 ◇ 6–6–01 Aramaki Aza-Aoba, Aoba-ku, Sendai, 980–8579, Japan