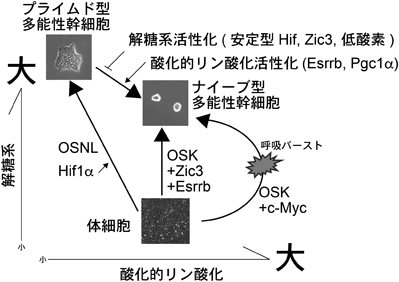
分化多能性の獲得・維持と代謝Metabolism controls acquisition and maintenance of pluripotency
1 京都大学iPS細胞研究所(CiRA)未来生命科学開拓部門Department of Life Science Frontiers, Center for iPS Cell Research and Application (CiRA), Kyoto University ◇ 〒606–8507 京都市左京区聖護院川原町53 ◇ 53 Kawahara-cho, shogoin Sakyo-ku, Kyoto 606–8507, Japan
2 国立研究開発法人日本医療機構,AMED-CRESTAMED-CREST, AMED ◇ 〒100–0004 東京都千代田区大手町1–7–1 ◇ 1–7–1, Otemachi, Chiyoda-ku, Tokyo 100–0004, Japan