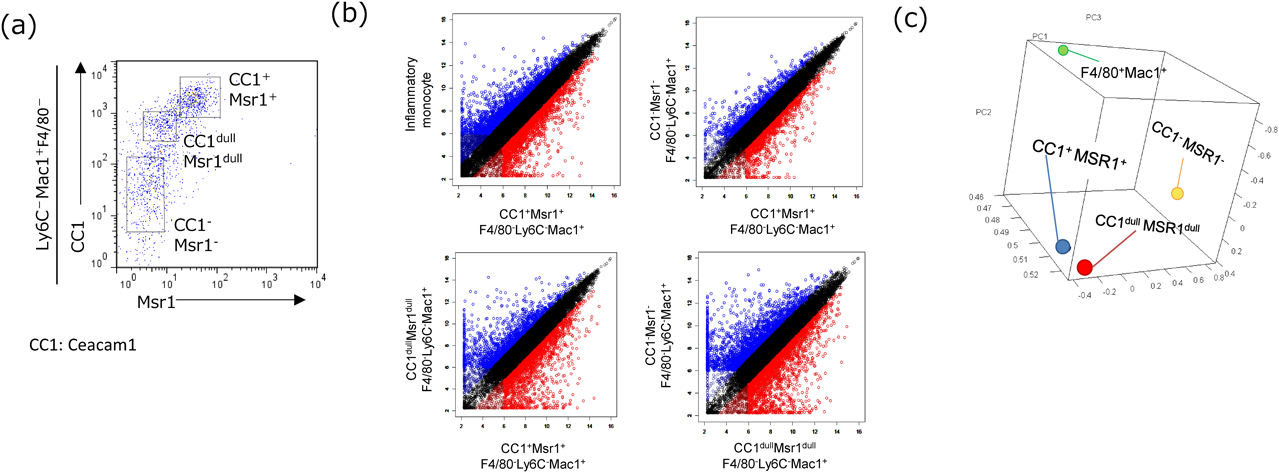
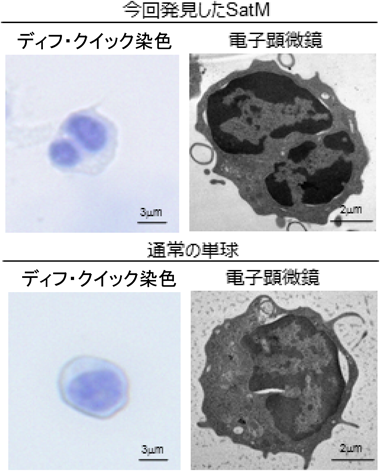
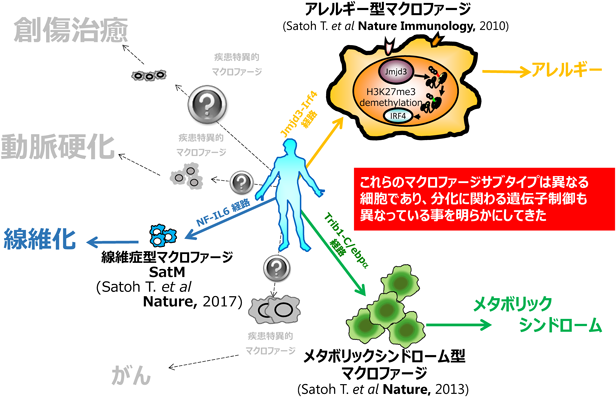
疾患特異的マクロファージの機能的多様性Functional diversity for disorder-specific macrophage subtype
1 大阪大学免疫学フロンティア研究センター自然免疫学Laboratory of Host Defense, Immunology Frontier Research Center, Osaka University ◇ 〒565–0871大阪府吹田市山田丘3–1 ◇ 3–1 Yamada-oka, Suita, Osaka, 565–0871
2 大阪大学微生物病研究所自然免疫学Laboratory of Host Defense, Research institute for Microbial diseases, Osaka University ◇ 〒565–0871 大阪府吹田市山田丘3–1 ◇ 3–1 Yamada-oka, Suita, Osaka 565–0871, Japan