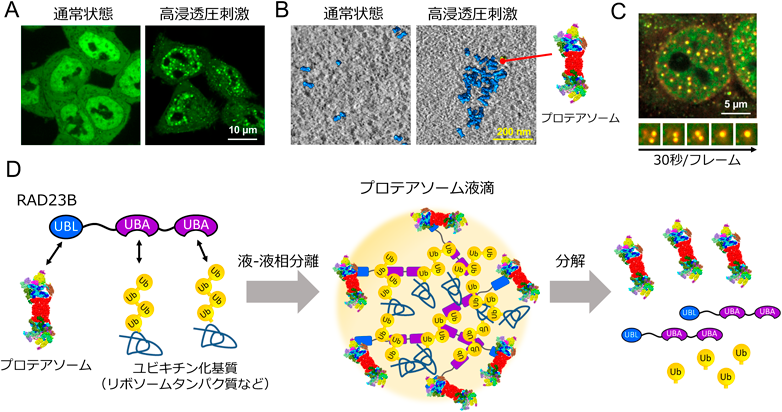
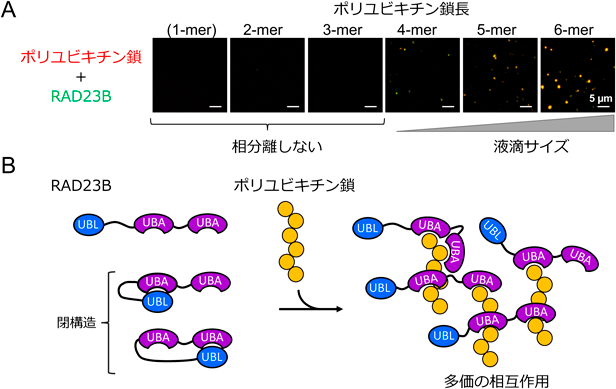
ストレスとユビキチンに依存したプロテアソームの液–液相分離Proteasome phase separation for degradation
公益財団法人東京都医学総合研究所 蛋白質代謝プロジェクトProtein Metabolism Project, Tokyo Metropolitan Institute of Medical Science ◇ 〒156–8506 世田谷区上北沢2–1–6 ◇ 2–1–6 Kamikitazawa, Setagaya-ku, Tokyo 156–8506, Japan