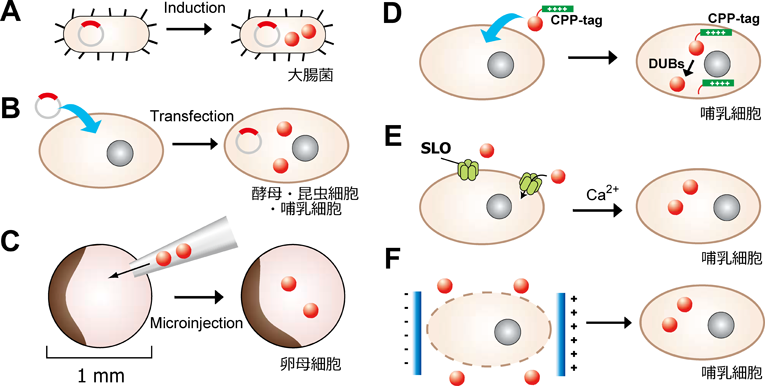
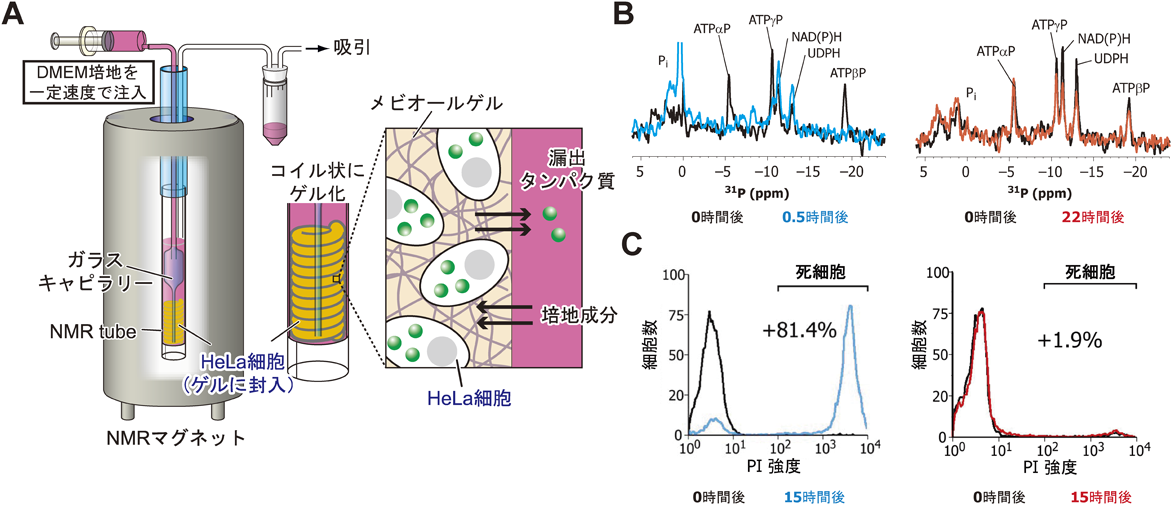
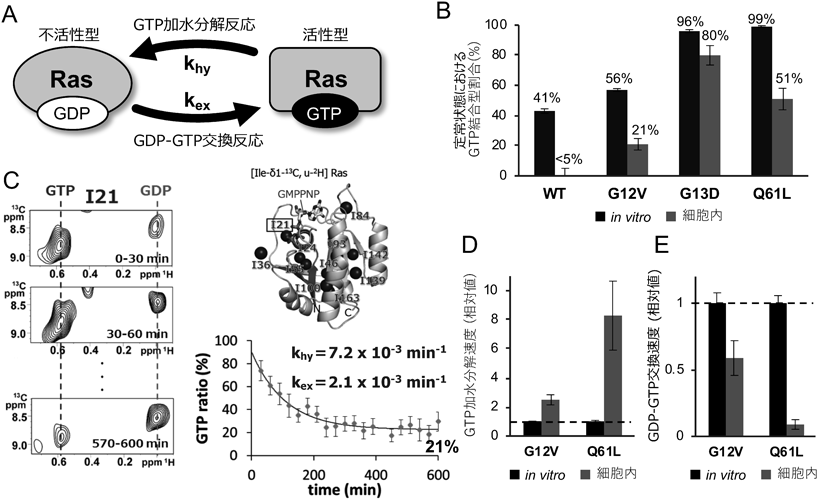
バイオリアクター型in-cell NMR法の開発とRasの活性状態の観測への応用Development of in-cell NMR bioreactor system for real-time monitoring of the activation status of Ras
千葉大学大学院薬学研究院Graduate School of Pharmaceutical Sciences, Chiba University ◇ 〒260–8675 千葉県千葉市中央区亥鼻1–8–1 ◇ 1–8–1 Inohana, Chuo-ku, Chiba 260–8675, Japan