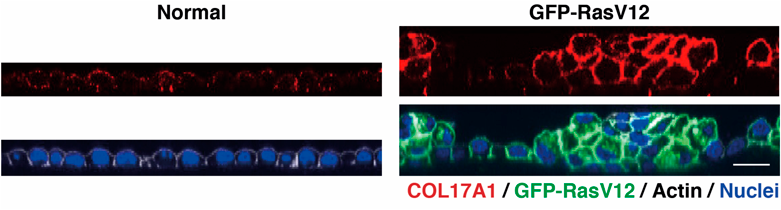
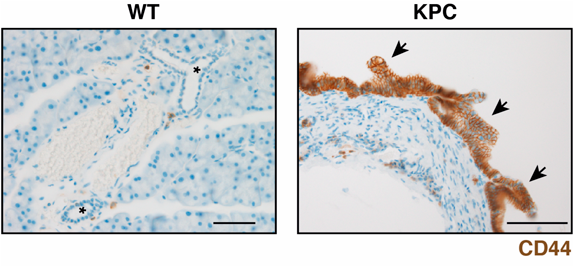
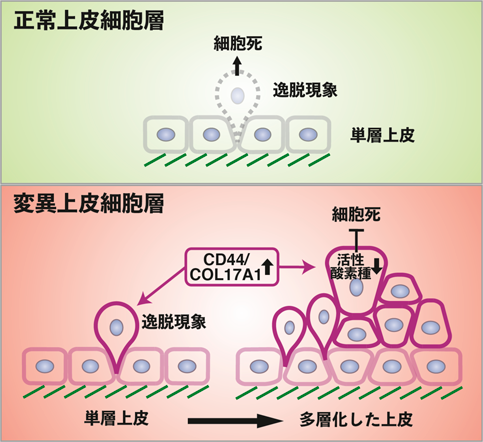
CD44/COL17A1経路はがん原性変異により引き起こされる多層上皮構造の形成を促進させるThe CD44/COL17A1 pathway promotes the formation of multilayered, transformed epithelia
京都大学大学院医学研究科分子生体統御学講座分子腫瘍学Department of Molecular Oncology, Kyoto University Graduate School of Medicine ◇ 〒606–8501 京都市左京区吉田近衛町 ◇ Sakyo-ku, Yoshida-Konoe-Cho, Kyoto 606–8501, Japan