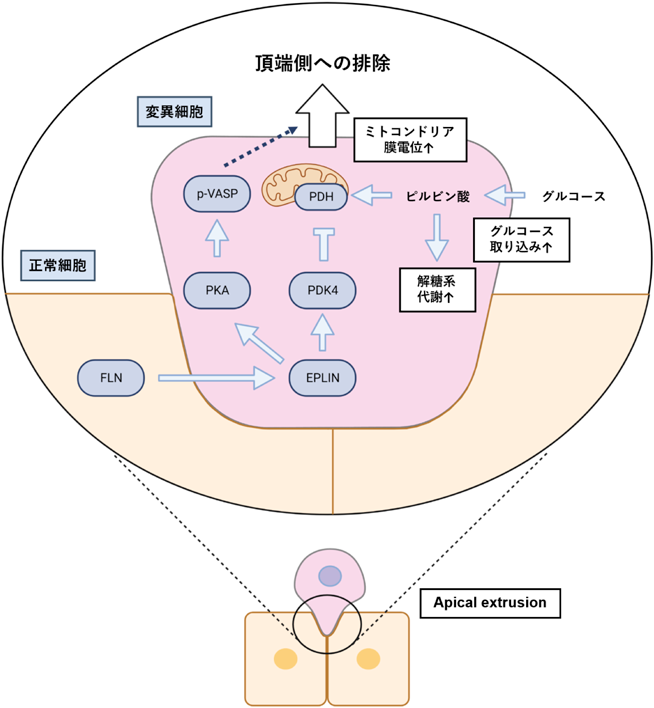
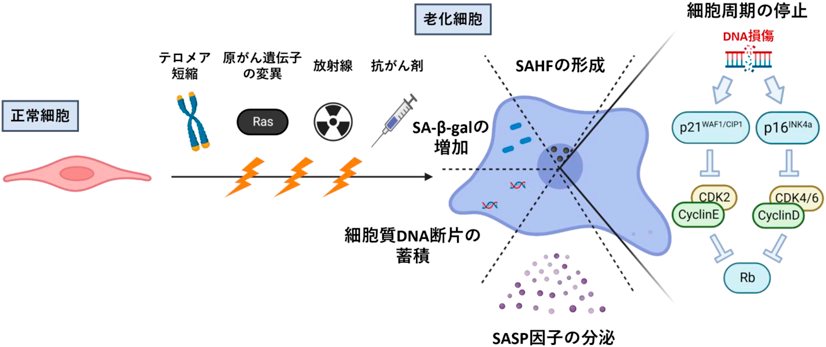
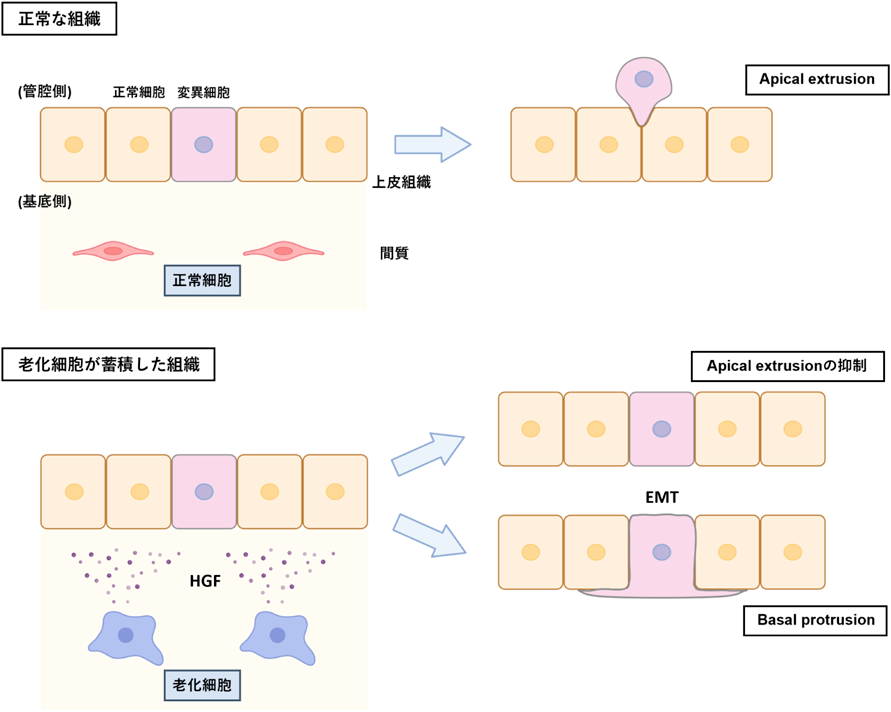
老化細胞が分泌するSASP因子による細胞競合阻害作用Inhibition of cell competition by SASP factors derived from senescent cells
公益財団法人がん研究会がん研究所細胞老化研究部Division of Cellular Senescence, Cancer Institute, Japanese Foundation for Cancer Research ◇ 〒135–8550 東京都江東区有明3–8–31 ◇ 3–8–31 Ariake, Koto-ku, Tokyo 135–8550, Japan