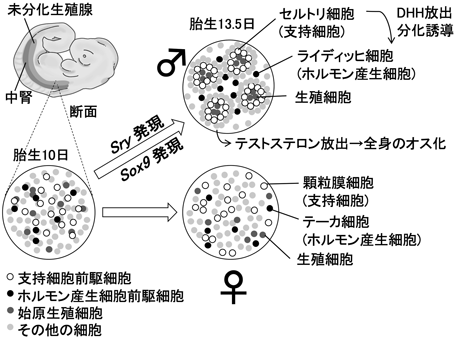
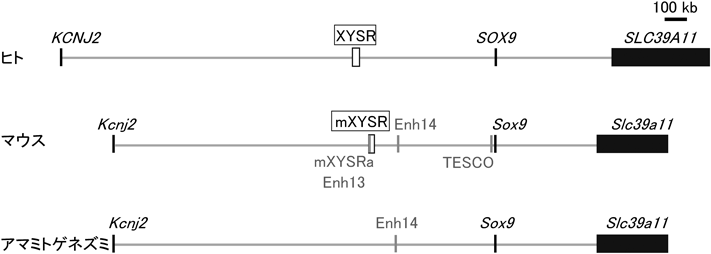
哺乳類の性決定におけるSox9のエンハンサーによる発現制御Regulation of Sox9 expression by enhancers in mammalian sex determination
国立研究開発法人国立成育医療研究センター研究所システム発生・再生医学研究部National Research Institute for Child Health and Development ◇ 〒157–8535 東京都世田谷区大蔵2–10–1 ◇ 2–10–1 Okura, Setagaya, Tokyo 157–8535, Japan