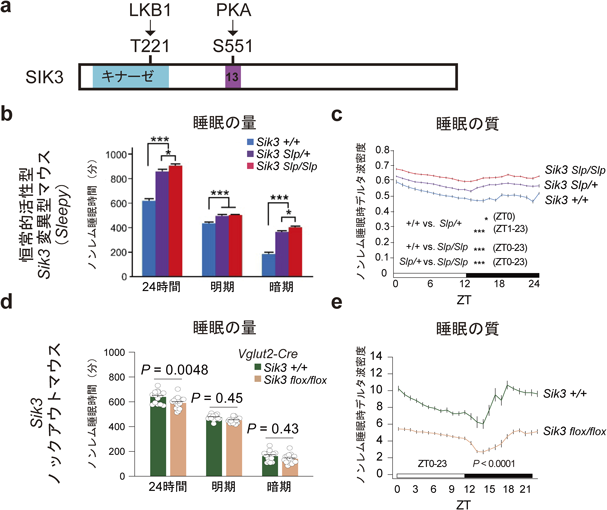
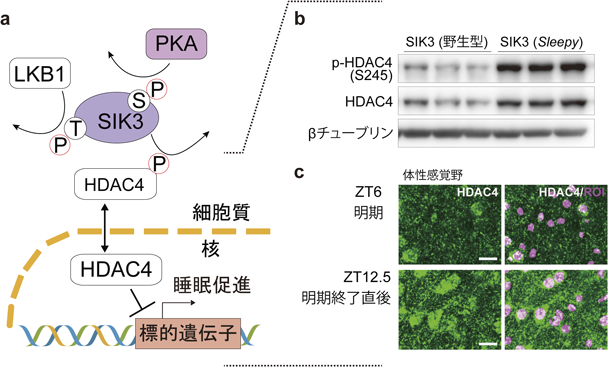
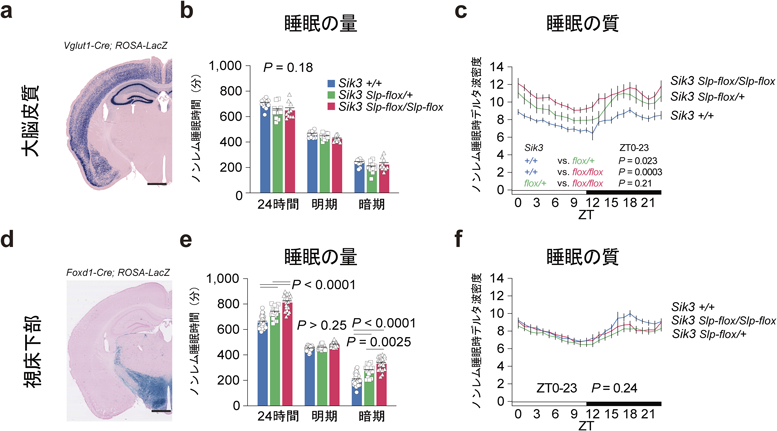
睡眠の質と量をつかさどる,興奮性ニューロン内LKB1-SIK3-HDAC4シグナル経路The LKB1-SIK3-HDAC4 signaling pathway in excitatory neurons regulates sleep quality and quantity
筑波大学国際統合睡眠医科学研究機構(WPI-IIIS)The international Institute for Integrative Sleep Medicine (WPI-IIIS), University of Tsukuba ◇ 〒305–0005 茨城県つくば市天王台1–1–1 ◇ 1–1–1 Tennodai, Tsukuba, Ibaraki 305–00005, Japan