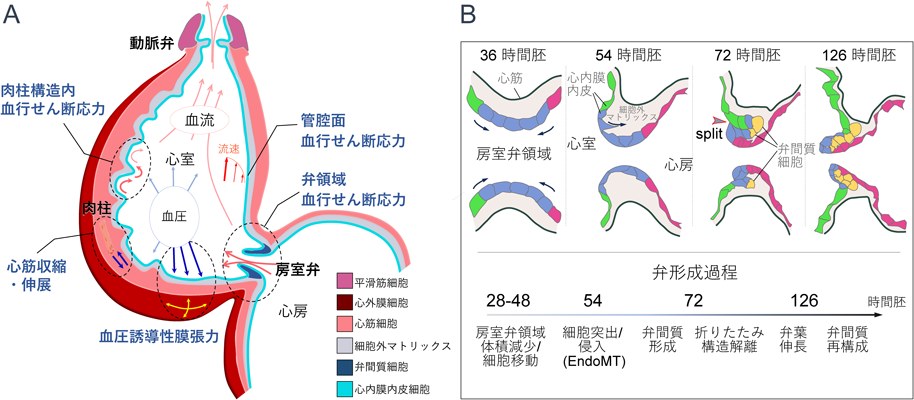
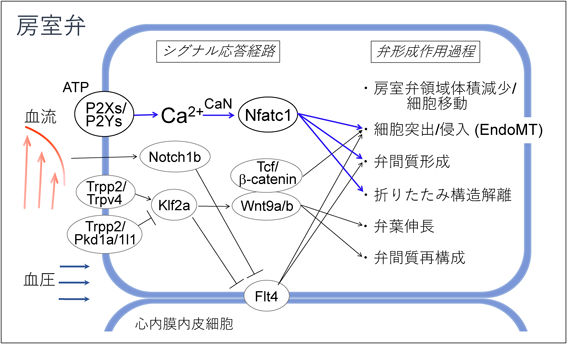
「力」により心臓管腔形成を調節する機構Tissue mechanics and signaling in cardiac lumen morphogenesis
徳島大学先端酵素学研究所生体力学シグナル分野Division of Biomechanics and Signaling, Institute of Advanced Medical Sciences, Tokushima University ◇ 〒770–8503 徳島市蔵本町3–18–15 ◇ 3–18–15 Kuramoto-cho, Tokushima 770–8503, Japan