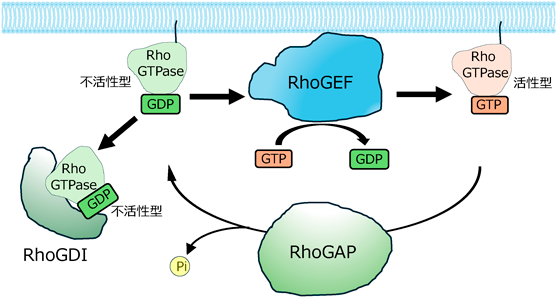
Rasスーパーファミリー低分子量タンパク質の一種であるRho GTPaseは,RhoA, Rac1, Cdc42を含む23種類から構成されており,その多くは細胞内で不活性なGDP結合状態と活性なGTP結合状態の間でサイクルが制御されることにより,細胞内分子スイッチとして機能する.その中には,恒常的に活性型で存在するRnd3やRhoD,ミトコンドリアで機能するMiro1等も含まれる1, 2).各種Rho GTPaseの異なったグアニンヌクレオチド結合状態への変化を制御するため,細胞内では,Rho GTPaseに特異的に作用する三つの分子群が主に機能している3).すなわち,GDP結合状態からGTP結合状態へ促進する働きを持つグアニンヌクレオチド交換因子(RhoGEF),GTP結合状態からGDP結合状態にするためRho GTPaseが持つGTP加水分解活性を上昇させる働きを持つGTPase活性化タンパク質(RhoGAP),細胞膜上の不活性型Rho GTPaseと相互作用することにより阻害するグアニンヌクレオチド解離阻害因子(RhoGDI)である(図1).
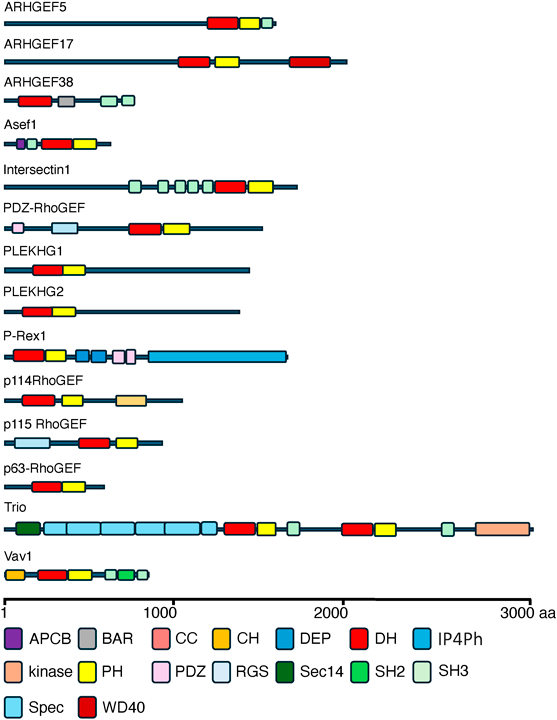
Rho GTPaseの活性化因子であるRhoGEFは,主に二つのファミリーで構成されている.一つは,diffuse B-cell lymphoma(Dbl)ホモロジー(DH)ドメインを持つDblファミリーRhoGEFであり,もう一つは,dedicator of cytokinesis(Dock)ホモロジー領域を持つDOCKファミリーRhoGEFである4, 5).DblファミリーRhoGEFのほとんどは,Rhoに対するグアニンヌクレオチド交換促進活性を持つDHドメインと,RhoGEFの細胞膜との相互作用を担うPleckstrinホモロジー(PH)ドメインがタンデムに存在する構造を持つ.それに対して,ARHGEF37やARHGEF38のようにPHドメインとは異なる脂質結合ドメインであるBin/Amphiphysin/Rvs(BAR)ドメインを持つRhoGEFも存在する(図2).さらに,DblファミリーRhoGEFの多くは,DHドメインやPHドメイン以外に,タンパク質の持つプロリンリッチ(PR)モチーフを認識し相互作用するSrc homology 3(SH3)ドメインや,タンパク質のC末端に存在するPSD95/Dlg/ZO-1(PDZ)ドメイン結合モチーフを認識し相互作用するPDZドメイン等の特定の機能を持つタンパク質ドメインを持つことにより,細胞内のほかの生体分子との相互作用等を介して,時空間的に制御されると考えられている.ヒト遺伝子中に,RhoGEFとして機能すると推測されるものは71種類存在する.一方,DOCKファミリーRhoGEFは,Dockホモロジー領域2(DHR-2, DOCKERやCZH2とも呼ばれる)を持ち,ヒト遺伝子中に11種類が存在する.一般的に,DOCKファミリーRhoGEFは,RacやCdc42に対して作用することが知られている6).
DblファミリーRhoGEFに関する総説は,これまでいくつか発表されているので,そちらも参照されるとよいと考える4–8).DblファミリーRhoGEFはさまざまな刺激により制御されることが知られているが,本稿では特に,三量体GTP結合タンパク質(Gタンパク質)共役型受容体(G-protein-coupled receptor:GPCR)刺激を介して遊離される各種Gタンパク質サブユニットによるDblファミリーRhoGEFの制御機構と,DblファミリーRhoGEFのPRモチーフとSH3ドメインを介したタンパク質間相互作用を介した制御機構について最新の知見を含め解説する.
2. 各種Gタンパク質サブユニットによるDblファミリーRhoGEFの制御
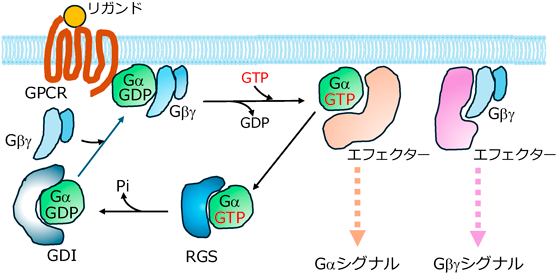
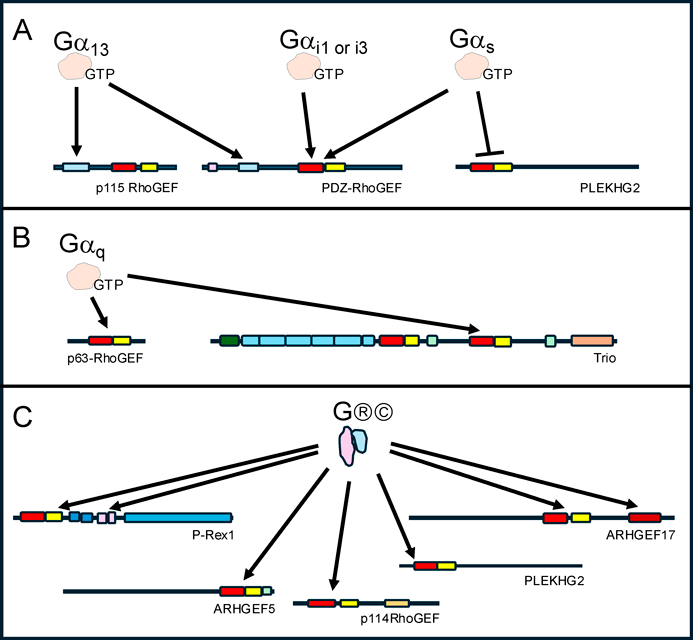
種々のGPCR刺激により,細胞はさまざまな形態変化を起こす.その際,それぞれのGPCRに共役するGタンパク質が活性型となり,それらが種々のRhoGEFの活性化を介して,Rho GTPaseを活性化することにより,細胞形態変化が誘導される.Gタンパク質は,Gα, Gβ, Gγの三つのサブユニットで構成され,細胞外リガンドが細胞膜上のGPCRに結合すると,細胞内で,GαサブユニットがGTP型に変換され活性型となり,活性型GαサブユニットとGβγサブユニット複合体に遊離し,それぞれが,下流のエフェクタータンパク質に作用する(図3).Gαサブユニットは,ヒト遺伝子中に16種類存在し,構造,機能から四つのサブファミリーに大別される.それぞれは,Gαi1, Gαi2, Gαi3等を含むGαiファミリー,Gαs, Gαolf等を含むGαsファミリー,Gαq, Gα11, Gα14等を含むGαqファミリー,Gα12とGα13を含むGα12ファミリーに分類される.また,Gβサブユニットは5種類,Gγサブユニットは12種類の遺伝子がそれぞれ存在する.これらの組合わせは,各細胞における遺伝子の発現量により異なると考えられる9–12).DblファミリーRhoGEFについては,1998年に,Gα12ファミリーによりp115 RhoGEFが直接的な制御を受けるという報告があって以来,Gタンパク質の活性型各サブユニットによる制御機構に関する報告が出されてきた13, 14)(図4).
1)Gα12/13により制御されるDblファミリーRhoGEF
活性型Gαsサブユニットに対してはアデニル酸シクラーゼが,活性型Gαqサブユニットに対してはホスホリパーゼCがエフェクターとして知られているが,活性型Gα12/13サブユニットのエフェクター分子については不明であった.しかし,リゾホスファチジン酸によるアクチンストレスファイバー形成に,活性型Gα12/13サブユニットと,その下流のRhoAが関与することが明らかになり,活性型Gα12/13サブユニットによるRhoGEFの活性化が注目された15).その後,上述したように,活性型Gα12/13サブユニットにより直接活性化されるDblファミリーRhoGEFとして,p115 RhoGEFが報告された13, 14).p115 RhoGEFはGタンパク質のGTPase活性を亢進させる働きを持つregulator of G protein signaling(RGS)ドメインを持ち,活性型Gα12/13がこのドメインと相互作用することを介してp115 RhoGEFが活性化され,下流のRhoAを活性化する16).このRGSドメインを持つDblファミリーRhoGEFとして,PDZ-RhoGEF17)や,LARG18)が同定されており,これらもRhoAを活性化させるDblファミリーRhoGEFである(図4A).
2)Gαqサブユニットにより制御されるDblファミリーRhoGEF
活性型Gαqサブユニットとの相互作用により活性化されるDblファミリーRhoGEFとして,p63RhoGEF/GEFTとTrioが報告されている19, 20).活性型Gαqサブユニットが,p63RhoGEFのPHドメインおよびTriple functional domain protein(Trio)の二つあるDHドメインとPHドメインのC末端側に存在するPHドメインのC末端アミノ酸配列に結合することにより,これらのRhoGEFが活性化される.また,この保存されたPHドメインのC末端アミノ酸配列はKalirinにも存在し,Kalirinも同様な制御を受けると考えられる19).このように,現在では,Gqシグナルによる細胞応答に関して,ホスホリパーゼC経路とDblファミリーRhoGEF経路の二つの下流シグナルに関して考える必要がある(図4B).
3)Gαsサブユニットにより制御されるDblファミリーRhoGEF
活性型Gαsサブユニットにより,アデニル酸シクラーゼが活性化され,細胞内cAMP量の増加に伴い,プロテインキナーゼA(PKA)が活性化されることがよく知られている.このことに関連し,DblファミリーRhoGEFの一種であるphosphatidylinositol 3,4,5-trisphosphate-dependent Rac exchanger 1(P-Rex1)が,PKAのリン酸化により阻害されるなどの報告がある21).一方,活性型Gαsサブユニットの直接相互作用によるDblファミリーRhoGEFへの効果については,活性型Gαsサブユニットが,pleckstrin homology and RhoGEF domain containing G2(PLEKHG2)のDHドメイン付近と相互作用することにより,その活性が抑制されることが報告されている22).その一方,Gα13サブユニットにより活性化されRhoAを活性化することが報告されているPDZ-RhoGEFが,活性型Gαsサブユニットと相互作用し,Cdc42を活性化するという報告もある23).これらの報告は,同じGαサブユニットが異なるDblファミリーRhoGEFに対して異なる制御を行うことができると同時に,同じDblファミリーRhoGEFが異なるGαサブユニットにより異なるRho GTPaseに対する特異性を示すことを意味する.これは非常に興味深い知見であり,今後の詳細な研究が待たれる(図4A).
4)Gαiサブユニットにより制御されるDblファミリーRhoGEF
Gαiファミリーはアデニル酸シクラーゼ活性を阻害するGαサブユニットであると同時に,GPCR刺激時に遊離するGβγサブユニットの主たる供給源がGiであるとも考えられてきた.そのため,これまでGαiファミリーにより直接的な制御を受けるDblファミリーRhoGEFに関する報告はほとんどなかった.その一方で,各種活性型GαiファミリーによるRho GTPaseの活性化について,いくつかの報告はあった24, 25).最近,近位依存性ビオチン化酵素によるタンパク質間相互作用解析技術を用い,活性型Gαi相互作用タンパク質が同定された26, 27).その結果,Gα13により活性化されRhoAを活性化するPDZ-RhoGEFが,活性型Gαi1とGαi3により活性化されるDblファミリーRhoGEFとして同定された.さらに,この活性化は,相同性が85%以上あるにもかかわらず,活性型Gαi2より活性型Gαi1とGαi3により特異性があることも明らかにされた.このことは,それぞれのGαサブユニットファミリーにおいて,相同性にあまり差がないサブユニット間で,DblファミリーRhoGEFに対する効果が大きく異なることを示唆している.今後,この点に着目し,それぞれのGαサブユニットに特異性のあるDblファミリーRhoGEFの同定が進む可能性があると考えられる(図4A).
5)Gβγサブユニットにより制御されるDblファミリーRhoGEF
GPCR刺激を受けて遊離されるGβγサブユニットにより活性化されるDblファミリーRhoGEFは,過去いくつか報告されている(図4C).P-Rex1は,初めて報告されたGβγサブユニットにより直接活性化されるDblファミリーRhoGEFである28).P-Rex1の活性化にはGβγサブユニット単独の結合では十分ではなく,リン脂質であるphosphatidylinositol 3,4,5-trisphosphate(PIP3)との結合が必要であり,アイソフォームであるP-Rex2も同様の性質を持っている.これらのDblファミリーRhoGEFは,Racを活性化させる29, 30).Gβγサブユニットと相互作用し活性化することで,RhoAとRac1を活性化されるDblファミリーRhoGEFとして,p114RhoGEF/ARHGEF18の報告もある31).PLEKHG2は,自身が持つDHドメイン付近の構造にGβγサブユニットが結合し活性化する32).P-Rex1とは異なり,PLEKHG2のPHドメインはPIP3との結合力は弱く,phosphatidylinositol 4,5-bisphosphateと強く結合するため,RacおよびCdc42を活性化する33).ARHGEF5/TIMは,siRNAスクリーニングによりケモタキシス(走化性)に関わるDblファミリーRhoGEFとして同定された.ARHGEF5は,Gβγサブユニットと自身が持つPHドメイン付近の構造が結合し活性化する34).P-Rex1やPLEKHG2とは異なり,ARHGEF5はRhoAとRhoBを強く活性化させ,RhoCとRhoGも活性化する.ARHGEF17/p164-RhoGEFは,GβγサブユニットがARHGEF17のC末端領域にまず結合することで構造変化が起こり,その後,GβγサブユニットがPHドメイン付近に結合することで活性化する.ARHGEF17も,ARHGEF5と同様にRhoAを活性化する35).
3. SH3ドメインを介したDblファミリーRhoGEFの制御機構
細胞内シグナルに関わるタンパク質は,リン酸化を含むさまざまな翻訳後修飾を受けることによりその機能が制御される.また,タンパク質間相互作用を介して,時空間的に制御されることも知られている.タンパク質間相互作用において使用されるタンパク質ドメインとして,SH3ドメインはよく知られている.SH3ドメインは,タンパク質中のPXXP配列で代表されるPRモチーフを認識し,相互作用することが知られている36).SH3ドメインを持つDblファミリーRhoGEFは21種類存在し,そのSH3ドメインは分子内におけるDHドメインとの位置関係や含有数も異なっている37).
1)SH3ドメインを介したDblファミリーRhoGEFの自己阻害
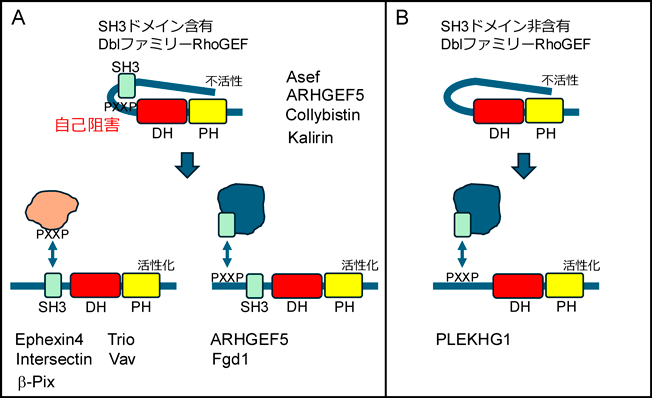
SH3ドメインを持つDblファミリーRhoGEFの中には,分子内のPRモチーフと含有SH3ドメインとが相互作用することにより,RhoGEF活性が自己阻害されている状態で存在するものがいくつか報告されている.この自己阻害は,リン酸化などの翻訳後修飾やほかの生体分子との結合によって解除され,DblファミリーRhoGEFが活性状態になると考えられる(図5A).大腸腺腫症タンパク質(adenomatous polyposis coli protein:APC)は,Wntシグナル伝達経路の負の制御因子であり,β-カテニンのリン酸化と分解を促進することが知られている.このAPCが結合することで活性化することが知られているAPC-stimulated guanine nucleotide exchange factor(Asef)は,自身が持つSH3ドメインとDHドメインが相互作用した抑制型で存在する.APCがAsefのAPC結合ドメインに結合することにより,SH3ドメインとDHドメインの相互作用による自己阻害が解除され,活性化される38–40).Asefと相同性が高いCollybistin/ARHGEF9/Pem-2についても,同様に,自身が持つSH3ドメインとDHドメインが相互作用した抑制型で存在すると考えられている.しかし,この自己阻害解除がどのように行われ,その解除がCollybistinのRhoGEF活性と関わっているのか等,不明な点が多い41).エンドサイトーシスにおいて重要な役割を持つとされるCdc42の活性化に関わるIntersectin1とIntersectin2の二つのアイソフォームを持つIntersectinは,分子内に五つのSH3ドメインを持つ.この五つのSH3ドメインのうち,DHドメインの一番近傍に位置するSH3(E)ドメインが,DHドメインと相互作用することにより自己阻害されていることが報告されている42, 43).この自己阻害は,neuronal Wiskott-Aldrich syndrome protein(N-WASP)などとの結合により解除され,Intersectin1が活性化状態になると考えられている.上述したDblファミリーRhoGEFのSH3ドメインは,各DblファミリーRhoGEFのDHドメインを中心にしてN末端領域に位置している.それに対して,ARHGEF5/TIMの場合,DHドメインよりC末端領域に位置するが,上述したDblファミリーRhoGEFと同様,SH3ドメインとDHドメインが相互作用した抑制型で存在する44).さらに,タンデムに並ぶDHドメインとPHドメインを分子内に2個持つDblファミリーRhoGEFのKalirinも,DHドメインに対して,よりC末端側に位置するSH3ドメインが結合することにより自己阻害されることが報告されている37).
2)SH3ドメインを介したほかのタンパク質との相互作用によるDblファミリーRhoGEFの制御
DblファミリーRhoGEFのSH3ドメインを利用した自己阻害とは別に,SH3ドメインとほかのタンパク質との相互作用に関する報告がいくつかある(図5A).β-PAK-interacting exchange factor(β-Pix)については,RacやCdc42のエフェクターの一つであるp21-activated kinase(PAK)2が,β-PixのSH3ドメインと結合することが知られている45, 46).また,GPCRの一種であるCXCR4を含む受容体の細胞内のソーティング,リサイクル,分解を制御することが知られているE3ユビキチンリガーゼの一種であるatrophin-interacting protein 4(AIP4)と,SH3ドメインを介して結合することも報告されている47).さらに,β-Pixが,Dynamin2とSH3ドメインを介して結合することにより,大腸がんの進行を促進する働きがあることが報告されている48).Vavに関しても自身の持つSH3ドメインを介して,mammalian sterile 20(Ste20)-like kinase 3(MST3)49),Epstein-Barr virus nuclear antigen 1(EBNA1)50),growth factor receptor-binding protein 2(Grb2)51–53)を含むいくつかのタンパク質との相互作用が報告されている.また,Trioに関しても,focal adhesion kinase(FAK)54)や,Myosin X55)との相互作用が,Ephexin4についてもengulfment and cell motility 1(Elmo1)との相互作用が報告されている56).五つのSH3ドメインを持つIntersectinは,エンドサイトーシスの制御機構に深く関わっていると考えられており,エンドサイトーシスに関わる重要なほかのタンパク質であるmammalian Son-of-sevenless(mSOS)57),Cdc42 GTPase-activating protein(CdGAP)58, 59),WASP-interacting protein(WIP)60),Endophilin-A61, 62),Synaptobrevin 263),Dynamin264)などとの相互作用が,SH3ドメインを介して行われることが報告されている.
3)DblファミリーRhoGEFのPRモチーフ等を介した活性制御
SH3ドメインを含まないDblファミリーRhoGEFの活性化もまた,不活性状態からの構造変化には,何らかの翻訳後修飾やタンパク質間相互作用を介した制御が必要と考えられる.その一つとして,ほかのSH3ドメインを含むタンパク質との相互作用を介する制御があげられるが,これに関する詳細な報告はまだあまりない.SH3ドメイン含有タンパク質には,Grb2やNCK2など,SH3ドメインとリン酸化チロシンを認識するSrc homology 2(SH2)ドメインで構成されるアダプタータンパク質や,上述したRhoGEFやSrcやFynを含む非受容体型チロシンキナーゼ等が含まれる.ヒトでは200種類以上のSH3含有タンパク質がある36).これらのSH3ドメイン含有タンパク質がDblファミリーRhoGEF上に存在するPRモチーフを認識することにより,それぞれのタンパク質機能を制御することが考えられる.骨格形成や胚の形態形成に影響を及ぼすX連鎖性ヒト疾患である顔面性器形成異常症(faciogenital dysplasia)の原因遺伝子産物であるCdc42に作用するDblファミリーRhoGEFであるFgd1は,Arp2/3複合体を介してアクチン重合を制御するアクチン結合タンパク質であるcortactinおよびマウスactin-binding protein 1と直接相互作用する65).このとき,cortactinおよびマウスactin-binding protein 1が持つSH3ドメインと,Fdg1のN末端領域にあるPRモチーフが結合し,アクチン骨格制御が行われると考えられる(図5A).また,podosome形成に重要な役割を担うSrcが持つSH3ドメインを用いた質量分析から,SH3ドメイン結合タンパク質としてARHGEF5が見いだされた66).ARHGEF5のどの領域でSrcのSH3ドメインと結合するかは不明であるが,ARHGEF5が多くPRモチーフを持つ点などを含め,今後検討がなされると考えられる(図4A).PLEKHG1/ARHGEF41も同じSrcファミリーチロシンキナーゼの一種であるFynによってチロシンリン酸化されると同時に,FynのもつSH2ドメインとSH3ドメインを介してPLEKHG1に結合し,活性化するとの報告があり,ARHGEF5と同様に,PLEKHG1も多数のPRモチーフを持つことから,これらを利用して相互作用するものと考えられる67)(図5B).