RhoファミリーGタンパク質は,アクチン細胞骨格の制御を介して,細胞の形態形成に重要な役割を果たしている.他のGタンパク質と同じように,不活性状態のGDP結合型と活性化状態のGTP結合型の間を,グアニンヌクレオチド交換因子(guanine nucleotide exchange factor:GEF),GTPase活性化因子(GTPase activating protein:GAP)といった制御タンパク質の作用を受けながら循環し,スイッチ分子として働いている.GEFは,Gタンパク質のGDP/GTP交換反応を促進することにより,Gタンパク質を直接活性化することができる制御因子であり,GEF自体も厳密に制御されている.GEFの恒常的な活性化によるRhoファミリーGタンパク質(RhoA, Rac1, Cdc42など)の調節異常は,がんの悪性化につながることが知られており,したがってこれらのGタンパク質に対するGEFはがんの治療標的になると考えられている1, 2).
哺乳類では,RhoファミリーGタンパク質に対するGEFはこれまでに約80種類が同定されている1, 3).そのうちの約70種類は,Dblホモロジー(DH)と呼ばれる共通の触媒ドメインを持ち,そのほとんどがC末端側に連続したPleckstrinホモロジー(PH)ドメインを持つDH–PHドメイン型のGEFである.一方,DHドメインを持たない非典型的なGEFとしてDOCKファミリー分子が同定されている4, 5).ヒトでは11種類存在するDOCKファミリー分子は,RacとCdc42を活性化し,これらのGタンパク質の活性化を通じて,免疫細胞の遊走,神経軸索の伸長,心血管系の発達,骨代謝などさまざまな生理機能を制御している6–8).また,浸潤がん,アルツハイマー病,骨溶解症などの疾患にも関与している.本稿では,DOCKファミリー分子の構造に焦点を当て,前半でそのユニークなドメインの構造と分子認織のメカニズムを紹介し,後半ではこれまでに明らかになった分子全体における活性制御のメカニズムについて紹介する.
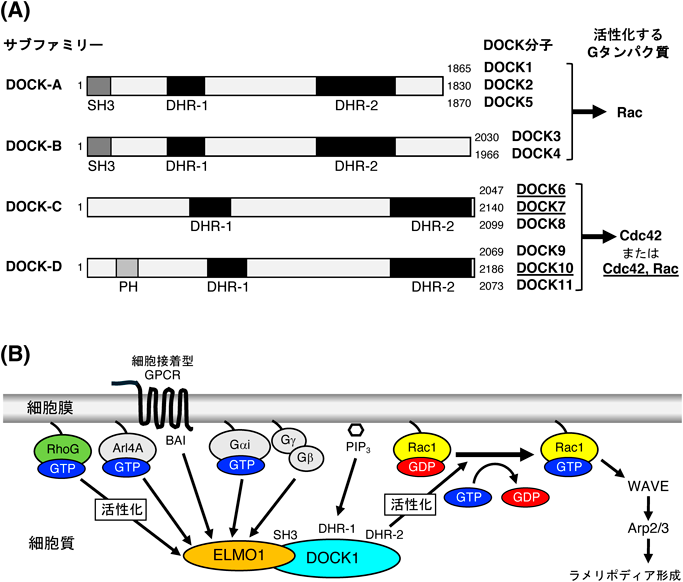
DOCKファミリー分子は,約2000アミノ酸残基からなる大きなマルチドメインタンパク質である(図1A).従来のGEFが持つDH–PHドメインの代わりに,二つのユニークなDOCKホモロジー領域(DHR)を共通に持つ.DHR-1ドメインは,ホスファチジルイノシトールリン酸(PIP)と結合することで,DOCK分子の細胞膜への局在を媒介する9).DHR-2ドメインは,RacまたはCdc42(またはその両方)に結合してGEFとして作用する触媒ドメインである4, 10).DOCKファミリー分子は,一次配列の相同性に基づいて四つのサブファミリーに分類される4).DOCK-A, Bサブファミリーに属するDOCK1~DOCK5は,Racを特異的に活性化する.DOCK-C, Dサブファミリーに属するDOCK6~DOCK11は,主にCdc42を活性化するが,そのうちDOCK6, DOCK7, DOCK10はCdc42とRacを活性化する二重特異性GEFである11–13).二つのDHRドメインに加え,DOCK-A, BサブファミリーはN末端にSH3ドメインを持つという特徴がある.これらの分子では,SH3ドメインとそれに続くヘリックス領域が,ELMO14)と呼ばれる足場タンパク質に結合する15, 16).ELMOは,単独ではGEF機能を持たないが,DOCKと協調して細胞内のRacシグナルを制御する17–19).一方,DOCK-Dサブファミリーは,PHドメインをN末端側に持つ.このサブファミリーに属するDOCK9のPHドメインは,分子の膜結合を媒介することが報告されている20).
細胞内では,RhoファミリーGタンパク質はC末端がゲラニルゲラニル化された状態で存在し,GDP解離阻害因子(GDP dissociation inhibitor:GDI)の作用を受けて細胞質と細胞膜上の間を行き来する21).活性化されたGタンパク質の作用部位は細胞膜であることから,活性化因子であるDOCKファミリー分子も細胞膜上で作用すると考えられる.一方,細胞の静止状態では,DOCKファミリー分子は主に細胞質に存在し,分子活性が抑制されているようである.たとえば,DOCK-AとBサブファミリーにそれぞれ属するDOCK1とDOCK4は,SH3ドメインとDHR-2ドメインの分子内相互作用によって活性が自己阻害される22, 23).ELMOも分子内相互作用によって自己阻害されることから24),DOCKとELMOは互いに結合することで自己阻害を解除していると考えられている6).DOCK-CとDサブファミリーにそれぞれ属するDOCK611)とDOCK920)についても,分子内相互作用による自己阻害が示唆されており,ドメイン構成の異なるDOCK分子がどのように制御されているのか興味深い.
外部刺激によって細胞が活性化されると,一般的にはホスファチジルイノシトール3-キナーゼ(PI3K)の活性化によってPI(3,4,5)P3が産生され,DOCKはDHR-1ドメインを介して細胞膜に移行し,RacやCdc42を活性化する.さらに,DOCK1に代表されるDOCK-A, Bサブファミリーは,結合パートナーのELMOが上流因子に結合することで分子の細胞膜上への移行が促進すると考えられている6)(図1B).具体的には,低分子量Gタンパク質のRhoG25)やArl4A26),ヘテロ三量体Gタンパク質のGαiサブユニット27)やGβγサブユニット28),細胞接着型Gタンパク質共役型受容体(G-protein-coupled receptor:GPCR)のBAI129)やBAI330)などの膜タンパク質が,DOCK–ELMO–Racシグナル伝達経路の上流因子として報告されている.ところが,DOCKの自己阻害とこれらのシグナル伝達因子による活性化の構造的基盤は,後で述べるクライオ電子顕微鏡技術が近年進歩するまで,まったく明らかにされていなかった.
一般に,複数のドメインから構成されるタンパク質は柔軟な構造を持つため,タンパク質全体の構造解析は困難である.DOCKとELMOもその例外ではなく,全体構造が解明される前に,結晶化やNMRによってさまざまな部分構造が決定された(表1).ここでは主要なドメインの構造を紹介する.
表1 DOCKファミリー分子の利用可能な構造情報| 領域 | 分子 | 複合体における結合分子 | 解析手法 | *PDB ID | 分解能(Å) | 公開年 |
|---|
| DHR-1 | DOCK1 | — | X線結晶構造解析 | 3L4C | 2.4 | 2010 |
| DOCK8 | — | X線結晶構造解析 | 7CLX | 1.5 | 2021 |
| — | X線結晶構造解析 | 7CLY | 1.4 | 2021 |
| DHR-2 | DOCK9 | Cdc42 | X線結晶構造解析 | 2WM9 | 2.2 | 2009 |
| Cdc42–GDP | X線結晶構造解析 | 2WMN | 2.4 | 2009 |
| Cdc42–GTP | X線結晶構造解析 | 2WMO | 2.2 | 2009 |
| DOCK2 | Rac1 | X線結晶構造解析 | 2YIN | 2.7 | 2011 |
| Rac1 | X線結晶構造解析 | 3B13 | 3 | 2012 |
| DOCK8 | Cdc42 | X線結晶構造解析 | 3VHL | 2.1 | 2012 |
| DOCK7 | Cdc42 | X線結晶構造解析 | 6AJ4 | 3.3 | 2019 |
| Cdc42 | X線結晶構造解析 | 6AJL | 3.2 | 2019 |
| DOCK10 | Cdc42 | X線結晶構造解析 | 6TKY | 2.6 | 2020 |
| Cdc42–GDP | X線結晶構造解析 | 6TKZ | 2.6 | 2020 |
| Rac3 | X線結晶構造解析 | 6TM1 | 3.7 | 2020 |
| Cdc42 | X線結晶構造解析 | 8I5F | 2.8 | 2023 |
| Rac1 | X線結晶構造解析 | 8I5W | 2.4 | 2023 |
| Rac1 | X線結晶構造解析 | 8I5V | 1.7 | 2023 |
| PH | DOCK9 | — | NMR | 1WG7 | | 2004 |
| SH3 | DOCK1 | — | NMR | 2M0Y | | 2012 |
| DOCK2 | ELMO1 Proリッチ領域 | NMR | 2RQR | | 2010 |
| ELMO1 PH–Proリッチ領域 | X線結晶構造解析 | 3A98 | 2.1 | 2010 |
| 全体 | DOCK2 | ELMO1 | クライオ電顕 | 6TGB | 5.5 | 2020 |
| ELMO1, Rac1 | クライオ電顕 | 6TGC | 4.1 | 2020 |
| DOCK5 | ELMO1, Rac1 | クライオ電顕 | 7DPA | 3.8 | 2021 |
| ELMO1 | クライオ電顕 | 8JHK | 4.8 | 2024 |
| ELMO1, Rac1, RhoG–GTP | クライオ電顕 | 8ZJ2 | 4.7 | 2024 |
| *蛋白質構造データバンク(Protein Data Bank, PDB) |
1)DHR-1ドメインと特異性
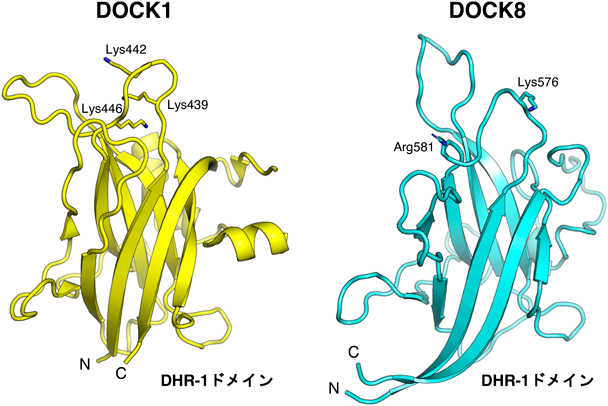
DHR-1ドメインは,プロテインキナーゼC(PKC)を含む多くのタンパク質にみられるC2ドメイン31)と共通の膜結合モジュールである.DOCK1のDHR-1ドメインの結晶構造が報告され,PI(3,4,5)P3を産生する酵素であるPI3KのC2ドメインとよく似た逆並行βサンドイッチ構造であることが明らかにされている32)(図2).分子表面には塩基性ポケットが見いだされ,このポケットを形成する三つのリシン残基がPI(3,4,5)P3との結合に関わることが同定された.
DOCK1にみられる塩基性ポケットのアミノ酸配列はDOCKファミリー内で違いがあるため,すべてのDOCK分子がDOCK1と同じPIP特異性を示すわけではない.プロテオーム解析の結果33),DOCK4, DOCK5, DOCK9は,DOCK1と同様にPI(3,4,5)P3に強く結合するが,興味深いことに,DOCK-Cサブファミリーに属するDOCK7とDOCK8はPI(3,4,5)P3よりもPI(4,5)P2に強く結合するという報告がなされている.筆者らは,DOCK8のDHR-1ドメインの結晶構造を決定し34),DOCK1とは形の異なる塩基性ポケットを見いだした(図2).このポケットを形成するリシン残基とアルギニン残基は,PI(4,5)P2結合残基であることが確認され,DOCK8がPI(3,4,5)P3よりもPI(4,5)P2に高い親和性で結合する構造的根拠が明らかになった.
2)DHR-2ドメインのGEFメカニズム
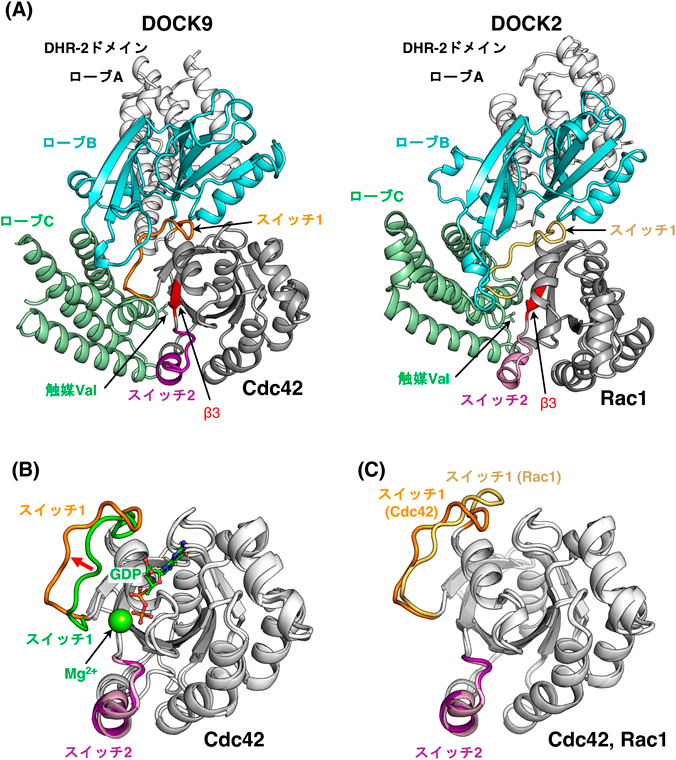
これまでに5種類のDOCKファミリー分子のDHR-2ドメインとGタンパク質との複合体の結晶構造が報告されている(表1).はじめにDOCK9–Cdc42複合体35)とDOCK2–Rac1複合体36)の構造が報告され,これらのDHR-2ドメインが三つの共通した領域(ローブA~Cと命名されている)から構成されることが明らかになった(図3A).このうち,ローブAはペアとなってホモ二量体を形成し,GEF活性には直接は関与しない37).Gタンパク質の結合領域はローブBとローブCで,Gタンパク質の二つのスイッチ領域周辺と広範囲に相互作用している.
GDP結合型のGタンパク質がDHR-2ドメインに結合すると,スイッチ1領域の構造変化が促進される(図3B).DHR-2ドメインのローブC上にあるヌクレオチドセンサーと呼ばれる触媒バリン(Val)残基は,Gタンパク質のGDP結合に必要なマグネシウムイオンの配位を阻害する(図3A).そのため,GDPはGタンパク質から解離し,GTPの結合が可能になり,Gタンパク質が活性化するというメカニズムが提唱されている35).このDHR-2ドメインの構造とそれらから推定されるGEFのメカニズムは,従来知られていたDH–PHドメイン型の交換因子とはまったく異なっている.
3)Gタンパク質特異性
DOCK2とDOCK9がそれぞれRacとCdc42に特異的に結合する構造的根拠は,二つのDHR-2ドメインの構造比較によって調べられた36).Rac1とCdc42は近接分子であり,GDP結合型とGTP結合型のコンホメーションはほとんど同じである.ところが,DHR-2ドメインと結合した状態(グアニンヌクレオチドを含まない状態)の構造を比較すると,スイッチ1のコンホメーションに違いがあることがわかる(図3C).これに対応して,DHR-2ドメイン側では,DOCK2とDOCK9の間でローブBとローブCの配置に違いがみられる(図3A).また,変異実験により,Gタンパク質は主にスイッチ1領域(27位,30位,33位)とβ3(54位,56位)のアミノ酸配列の違いによってDHR-2ドメインに認織されることが明らかになった(図3A).したがって,DOCK2(DOCK-Aサブファミリー)とDOCK9(DOCK-Dサブファミリー)の特異性は,Gタンパク質認識に直接関わるアミノ酸残基の違いと,DHR-2ドメインの構造(ローブBとローブCの配置)の違いの両方によって決定されていると考えられる36, 38).
筆者らは,Cdc42とRacを活性化する二重特異性GEFとして,DOCK7(DOCK-Cサブファミリー),DOCK10(DOCK-Dサブファミリー)の結晶構造を決定した39, 40).Cdc42を特異的に活性化するDOCK841),DOCK935)に比べて,DOCK7–Cdc42複合体39)では,上述のGタンパク質認織部位(スイッチ1領域とβ3)での相互作用が弱いことがわかった.したがって,DOCK7はCdc42に対して特異性が低下し,Racに対して寛容であると予測された.DOCK10については,Cdc42およびRac1との複合体をそれぞれ決定した40).その結果,DOCK10はDOCK9(Cdc42特異的)と同じように強くCdc42と相互作用し,Rac1とはDOCK2(Rac特異的)とは異なる形で相互作用することが示された.さらに,変異実験によって,二重特異性はローブB内のアミノ酸配列によって特徴づけられることが確認された.
このように,さまざまなDOCK分子のドメインを原子レベルの分解能で構造解析することで,分子認識の詳細なメカニズムが明らかになってきた.
5. DOCK–ELMO複合体のクライオ電子顕微鏡単粒子解析
DHR-1およびDHR-2ドメイン以外の領域は,DOCKファミリー分子の機能にどのように関わっているのだろうか.近年,クライオ電子顕微鏡技術によってDOCK2–ELMO1複合体42)とDOCK5–ELMO1複合体43)の全体構造が明らかになり,複数のドメインによる活性制御の理解が大きく前進した.クライオ電子顕微鏡を用いた単粒子解析は,巨大タンパク質の構造スナップショットを捉えるのに適した手法である.ここでは,筆者らのグループによるDOCK5–ELMO1の3種類の複合体の構造解析を中心に紹介する.
1)DOCK5–ELMO1–Rac1複合体の構造
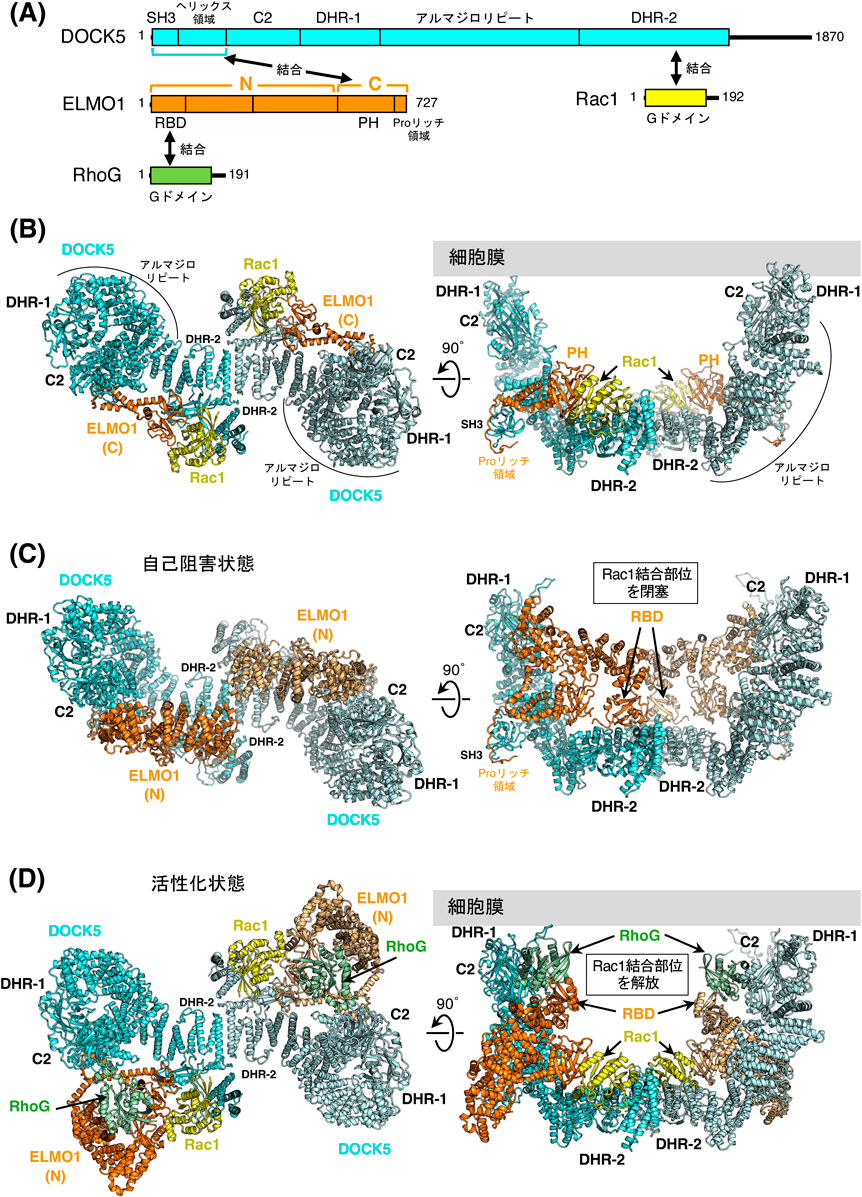
DOCK5はDOCK-Aサブファミリーに属し,細胞内でELMOと結合することでRacを特異的に活性化する.DOCKとELMOがどのように連携してRacを活性化するのかを明らかにするために,DOCK5, ELMO1, Rac1の三者複合体の構造を解析した43)(図4A).DOCK5–ELMO1–Rac1三者複合体は,DOCK5のDHR-2ドメインがペアになってホモ二量体を形成している(図4B).2分子のRac1は,二量体の中央付近にあるDHR-2ドメインの触媒領域(ローブBとC)に結合している.DHR-1ドメインとDHR-2ドメインの間はアルマジロリピートと呼ばれるαヘリックスの超らせん構造でつながっている.DOCK5のN末端(SH3ドメインとヘリックス領域)はELMO1のC末端[PHドメインとプロリン(Pro)リッチ領域]と強固に結合し16),さらにアルマジロリピートとも結合することで,全体として安定した構造を形成している.DHR-1ドメインは二量体の両端にあり,塩基性ポケットは同じ方向に向いていることから,ホモ二量体は細胞膜に安定に結合すると予想される.また,DHR-1ドメインに隣接して,塩基性ポケットを持たないC2ドメインが同定された.このC2ドメインは膜結合には関与しないが,構造の安定化やタンパク質間相互作用(たとえば,後述の自己阻害状態におけるELMO1との相互作用)に関与している.
興味深いことに,ELMO1のC末端側にあるPHドメインは,Rac1とDHR-2ドメイン(ローブB)の両方と相互作用していた.この構造から,ELMO1のPHドメインは,GDP/GTP交換反応におけるDOCK5とRac1の結合を安定化させている可能性が示唆される.実際に,Rac1と相互作用するELMO1のPHドメインのアミノ酸残基に変異を導入すると,精製タンパク質を用いた実験で,Rac1に対するDOCK5–ELMO1複合体のGEF活性が低下することが確認された.
別途報告されたDOCK2–ELMO1–Rac1複合体42)は,DOCK5–ELMO1–Rac1複合体と基本的に同じ構造を示している.ELMO1のPHドメインよりN末端側の領域(図4A)は,筆者らのDOCK5–ELMO1–Rac1複合体では観測されていないが,DOCK2–ELMO1–Rac1複合体では「開いた」コンホメーションとして捉えられており,構造的に柔軟であることがわかる.
2)DOCK5–ELMO1複合体の構造
上述の構造的柔軟性を示すELMO1のN末端側は,複数の上流因子との結合に関与する領域である(図1B).DOCK5–ELMO1複合体においてELMO1のN末端側を欠失させると,精製タンパク質を用いた実験でRac1に対するGEF活性が大きく上昇した42, 43).このことは,ELMO1のN末端側がDOCK5–ELMO1複合体の自己阻害に関与していることを示唆している.そこで次に,Rac1を含まないDOCK5–ELMO1二者複合体のクライオ電子顕微鏡単粒子解析を行ったところ,ELMO1のN末端側とC末端側が分子内相互作用する「閉じた」コンホメーションが確認された44)(図4C).この構造では,ELMO1のN末端にあるRBDドメインとDOCK5のDHR-2ドメインが相互作用している.したがって,Rac1の結合部位がELMO1によって閉塞され,GEF活性が阻害されていることが示唆される.DOCK5–ELMO1複合体の「閉じた」コンホメーションは,別途報告されているDOCK2–ELMO1複合体の構造42)と類似していることから,DOCK–ELMO複合体は共通の自己阻害メカニズムを持つ可能性が高い.
3)RhoG–DOCK5–ELMO1–Rac1複合体の構造
RhoGは,Racに最も近縁なRhoファミリーGタンパク質の一員である.活性化(GTP結合)によってELMO1のRBDドメインに結合し,DOCKを介してRacシグナル伝達を活性化することが報告されている25, 45–47)(図1B).筆者らは,精製タンパク質を用いた実験で,GTP結合型のRhoGをDOCK5–ELMO1複合体に結合させると,Rac1に対するGEF活性が上昇することを見いだした.また,Rac1に対する親和性も上昇することがわかった.この構造基盤を明らかにするため,RhoGとRac1を含むDOCK5–ELMO1複合体(四者)のクライオ電子顕微鏡単粒子解析を行った(図4A).この解析では,RhoGとRac1が結合した「開いた」コンホメーションがとらえられた(図4D)44).前述の「閉じた」コンホメーションと比べると,ELMO1のN末端側は,C末端側に対して約120度回転している.RhoGはスイッチ領域を介して(すなわち,GTP結合に依存して)ELMO1のRBDドメインに結合する42, 48)と同時に,別の領域でDOCK5のC2ドメインと相互作用している.これらの結果は,DOCK5–ELMO1の「開いた」コンホメーションをRhoGが安定化させ,Rac1の結合を促進するという自己阻害解除のメカニズムを示唆している.このように,DOCK–ELMO複合体が上流因子と結合することで活性化するメカニズムの一端が明らかになりつつある.
クライオ電子顕微鏡技術により,これまで結晶構造解析では報告されていなかったDOCK分子全体の構造が明らかになり,さらに,シグナル伝達の過程で形成される一過性の複合体形成の様子も捉えることが可能になってきた.一方,上述のDOCK2とDOCK5の最初のクライオ電子顕微鏡構造が解析された後,AlphaFold(アルファフォールド)プログラムにより,タンパク質の構造を高い精度で予測することが可能になった.今後,クライオ電子顕微鏡技術とAlphaFold予測を組み合わせることで,まだ明らかにされていないDOCKファミリー分子の自己阻害状態と活性化状態の構造解析が進むことが期待される.
一方,柔軟な構造や不均一な相互作用は,たとえ機能的に重要であっても,タンパク質の構造解析では可視化しにくい問題がある.本稿で紹介したクライオ電子顕微鏡単粒子解析では,タンパク質の化学的架橋が試料の安定化に有効であったが,この人工的な影響を排除することはできない.また,単純化された,脂質膜を含まない可溶性系における構造解析であることにも注意を払う必要がある.DOCK分子が細胞膜上でGタンパク質を活性化する際には,コンホメーション変化が起こる可能性が高いことも指摘されている49).このような課題に取り組むため,筆者らのグループは,Gタンパク質とDOCKの複合体を脂質膜上に再構成するなど,より生体内に近い環境での構造解析を実現する技術の開発も進めている.冒頭で述べたように,DOCKファミリー分子はがんやその他の疾患の重要な治療標的であり,そのユニークな構造と制御メカニズムの理解が進めば,将来,DOCKファミリー分子を特異的に阻害(または活性化)する薬剤の開発につながることが期待される.