3. Arfファミリー低分子量GTP結合タンパク質の活性調節と調節分子の結合タンパク質
1)Arf6を活性化する交換因子cytohesinの分類と構造について
1992年,LiuとPohajdakによってヒトcDNAクローンより単離されたB2-1は,ナチュラルキラーT細胞と末梢Tリンパ球に高発現し,酵母の分泌経路に関与するSec7タンパク質と相同性を有する分子であると考えられていた18).その後,ヒトJurkat細胞cDNAライブラリーを用いた酵母ツーハイブリッド法により,B2-1はβ2インテグリンの細胞内ドメインに結合する分子として同定され,インテグリンの細胞接着機能への関与が予測されたことから,cytohesin-1(サイトへジン1)と命名され19),その後の研究により,これが低分子量GTP結合タンパク質Arfファミリーの活性化因子であることが明らかとなった20).
Cytohesinは,cytohesin-1,-2,-3,-4の4種類のサブファミリーに分類される約340から400アミノ酸のタンパク質である21–25).cytohesin-1は脾臓,血球系やリンパ球系に高発現し,cytohesin-2[ARNO(Arf nucleotide-binding site opener)とも呼ばれる]とcytohesin-3[(GRP1(general receptor for phosphoinositides 1)またはARNO3とも呼ばれる]は組織特異性が低くさまざまな部位に発現し,cytohesin-4もブロードな発現を示すが,リンパ球系に比較的多く発現していると考えられている.
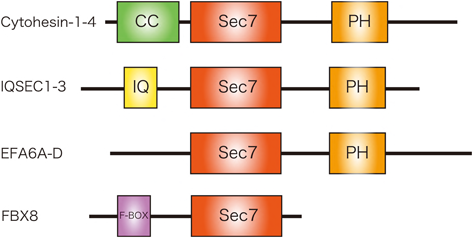
すべてのcytohesinは類似したドメイン構造を有している(図3).N末端側からCoiled-coilドメイン,Sec7ドメイン,Pleckstrin homology(PH)ドメイン,C末端の塩基性アミノ酸に富む領域である.Coiled-coilドメインはタンパク質モチーフの一つで,ロイシンなどの疎水性アミノ酸を含む7アミノ酸残基の繰り返し配列を含んでおり,他のCoiled-coilドメインを有するタンパク質との相互作用に関与している.Arfファミリー活性化に直接関与するグアニンヌクレオチド交換因子(guanine nucleotide exchange factor,以下GEFと略す)活性を触媒するSec7ドメインは,cytohesinの主要な生理学的機能を担う.Sec7ドメインに隣接するPHドメインは,イノシトールリン脂質に結合し,タンパク質の細胞膜への局在に関与する.
現在まで,Sec7ドメインを有する哺乳類のArfGEFは15種類同定されている26, 27).cytohesin-1~4サブファミリーのほかに,BIG1, 2(brefeldin A-inhibited guanine nucleotide-exchange protein 1, 2またはArfgef1, 2)サブファミリー,GBF1(Golgi brefeldin A-resistant factor 1),IQSEC1~3[IQ and Sec7 domain-containingまたはBRAG1~3(brefeldin A-resistant Arf-GEF 1~3)]サブファミリー,EFA6A~D[exchange factor for Arf6 A~DまたはPSD(Pleckstrin and Sec7 domain containing)1, 4, 2, 3]サブファミリー,FBX8(F-box only protein)である.BIG1サブファミリーはArf1, 3に,GBF1はArf1, 3, 5に比較的高い特異性を有するが,その他の交換因子cytohesin, IQSEC, EFA6サブファミリーはArf6に特異性が高いと考えられている.なかでも,cytohesin-1とcytohesin-2はArf6への特異性が非常に高いことが指摘されている(図3).
2)その他のArfGEFサブファミリーと細胞機能
BIG1サブファミリーとGBF1は,細胞内の膜輸送をつかさどっている.BIG1およびBIG2は,trans-ゴルジネットワーク(TGN)とエンドソームに局在し,主にエンドソームと細胞膜間の輸送に関与する28).またArf1およびArf3の活性化を介したクラスリンアダプタータンパク質AP1結合クラスリン小胞のゴルジ体から細胞膜への輸送を制御している.一方,GBF1は,小胞体とゴルジ体の中間に位置するオルガネラER-Golgi intermediated compartmentやcis-ゴルジに局在し,Arf1を介したCOPI小胞輸送に関与している29).本稿のテーマとはそれるが,BIG1は,冒頭で述べた末梢神経系の髄鞘形成細胞であるシュワン細胞の髄鞘化過程にも深く関与している.髄鞘化の際にシュワン細胞は自身の細胞膜を何十倍にも広げることにより,軸索周囲に髄鞘を形成していることから,髄鞘化の過程では多くのタンパク質の輸送と分泌が活発に行われている.それまで,cytohesin-1がArf6を介してシュワン細胞の初期発生過程を,また中後期過程ではcytohesin-1がcytohesin-2に置き換わり,同じくArf6を介してその発生過程を制御していることを明らかとなっていた(詳細は後述する).一方で,Arf1とArf1GEFが髄鞘化に関与するという報告はなく,長い間ブラックボックスであった.そこで,シュワン細胞特異的BIG1コンディショナルノックアウトマウス(cKO)を作製し,坐骨神経の解析を行った.その結果,BIG1 cKOマウスでは髄鞘層の厚さが薄くなっており,メカニズムとしてBIG1がArf1の活性化を介して,AP1結合クラスリン小胞複合体依存的に髄鞘構成タンパク質の輸送を促進している機構が考えられた30).Arf1 cKOマウスにおいても同様の現象が観察された.このように,BIG1やcytohesinなどArfGEFの新たな役割が明らかになってきている.
その他のArfGEFの話に戻り,IQSECサブファミリーは,接着分子やシグナル分子の輸送を制御している.たとえば,β1インテグリン受容体は,IQSEC1とArf5を介してインターナリゼーションし,乳がん細胞の転移を制御している31).また,IQSEC1, 2, 3はともに中枢神経系に高発現しており,IQSEC1および2はArf6の活性化を介してAMPA受容体のリサイクリングに関与している32).
残りのArfGEFであるEFA6サブファミリーのうち,EFA6B以外もまた脳に高発現しており,EFA6Aは前脳および小脳の顆粒細胞に33),EFA6Cは小脳のプルキンエ細胞に特異的に発現していること34)が確認されている.なかでもEFA6Aは,神経細胞の樹状突起やスパインに局在がみられ,Arf6を介してtelencephalinをエンドソームへ輸送し,それによりスパイン構造の安定化に寄与している35).EFA6Dに関しては10種類のalternative splicing formsが存在し,脳における解析も進んでいる.EFA6D1bと1cは海馬歯状回の顆粒細胞に,EFA6D1sは海馬錐体細胞のスパインなどに発現が確認されている36).
最後に,FBX8については研究があまり進んでいないが,Arf6をユビキチン化することにより,Arf6の活性を調節しているという報告があり,Sec7ドメインを有するにもかかわらず,GEF活性を有しない分子である37).
3)Cytohesin結合タンパク質
Arf6のGEFであるcytohesin結合タンパク質は数多く同定されているが(表1),なかでもCoiled-coilドメインを介したものが特に多い.以下,ドメインごとに順次主な結合タンパク質を紹介していく.
表1 cytohesinに結合するタンパク質| 結合タンパク質 | タンパク質の種類 | 結合による変化 | 結合するcytohesin | 結合するcytohesinのドメイン | 文献 |
|---|
| C1orf106 | ユビキチンリガーゼのコファクター | cytohesinをユビキチン化し,細胞間接着を安定化 | cytohesin-1, 2,3 | Coiled-coil | 38 |
| CASP | スキャフォールドタンパク質 | エンドソームへのリクルート | cytohesin-1 | Coiled-coil | 39, 40 |
| CCDC120 | スキャフォールドタンパク質 | 神経細胞の突起伸長 | cytohesin-2 | Coiled-coil | 41 |
| CNK1 | スキャフォールドタンパク質 | インスリン刺激による細胞膜へのリクルートとPIP5Kの活性化 | cytohesin-1 | Coiled-coil | 42 |
| CNK2 | スキャフォールドタンパク質 | Rac1GEFなどとシグナル複合体を形成し,スパイン形成を制御 | cytohesin-1, 2,3 | Coiled-coil | 43, 44 |
| CNK3 (IPCEF1) | スキャフォールドタンパク質 | HGFによるArf6の活性化と細胞遊走を制御 | cytohesin-2 | Coiled-coil | 45 |
| FRMD4A | スキャフォールドタンパク質 | Par3を介して上皮細胞の極性を制御,Tauの分泌を制御 | cytohesin-1 | Coiled-coil | 46, 48 |
| FRMD4B (GRSP1) | スキャフォールドタンパク質 | インスリン刺激による細胞膜への移行 | cytohesin-3 | Coiled-coil | 50 |
| Tamalin (GRASP) | スキャフォールドタンパク質 | グルタミン酸受容体のシナプス後膜への局在化など | cytohesin-2, 3 | Coiled-coil | 51-54 |
| Gαq | Gタンパク質 | Arf6の活性化を介したGαq共役型受容体のインターナリゼーション | cytohesin-1, 2 | Coiled-coil | 56, 57 |
| インスリン受容体 | 細胞膜受容体 | インスリン刺激によるArf1の活性化 | cytohesin-2 | Coiled-coil+PH | 58 |
| cytohesin-2 | グアニンヌクレオチド交換因子 | cytohesinの細胞膜での局在安定化 | cytohesin-2 | Coiled-coil | 59 |
| Munc13-1 | プレシナプス受容体 | cytohesin-1のシナプス前膜への局在化 | cytohesin-1 | Coiled-coil | 61 |
| Pallidin | リソソーム生合成複合体因子 | 海馬神経細胞の樹状突起形成 | cytohesin-2 | Coiled-coil | 62 |
| β2インテグリン | 細胞接着因子 | インテグリンの機能発現 | cytohesin-1, 3 | Sec7 | 63, 64 |
| EGF受容体 | 細胞膜受容体 | EGF受容体の活性修飾 | cytohesin-2 | Sec7 | 65 |
| ARFRP1 | 低分子GTP結合タンパク質 | cytohesinの細胞膜移行阻害によるPLD活性化抑制 | cytohesin-1 | N末端+Sec7 | 66 |
| Arf6 | 低分子GTP結合タンパク質 | cytohesinの細胞膜への移行 | cytohesin-2, 3 | PH | 67 |
| Arl4s | 低分子GTP結合タンパク質 | cytohesinの細胞膜への移行 | cytohesin-1, 2, 3, 4 | PH+PB | 68, 69 |
| A2Aアデノシン受容体 | Gαq共役型受容体 | MAPキナーゼの活性化 | cytohesin-2 | PH | 70 |
| EPI64 (TBC1D10A) | Rab27不活性化因子 | Arf6の活性化とEPI64によるRab27aの不活性化によるエンドサイトーシスの制御 | cytohesin-2 | PH | 71 |
| FE65 | アダプタータンパク質 | Arf6活性化による神経細胞の突起伸長を制御 | cytohesin-2 | PH | 73 |
| actinin1 | アクチン骨格制御タンパク質 | 神経突起伸長 | cytohesin-2 | PH+PB | 74 |
| paxillin | 細胞接着班タンパク質 | 脂肪細胞の遊走促進 | cytohesin-2 | PB | 75 |
a.Coiled-coilドメインを介した結合タンパク質
クローン病や潰瘍性大腸炎など,大腸や小腸の粘膜に慢性の炎症や潰瘍を引き起こす原因不明の疾患を総称して炎症性腸疾患と呼ぶが,その感受性遺伝子の一つとして,C1orf106が知られている.2018年,アフィニィティークロマトグラフィー法により,C1orf106に結合するタンパク質として,cytohesin-1, 2, 3が同定された38).C1orf106は,cytohesin-1のCoiled-coilドメインを含むN末端領域と結合し,cytohesin-1をユビキチン化によって分解することによりArf6の活性化を抑制し,細胞間接着の安定化に寄与している.
次に,cytohesin-associated scaffold protein(CASPまたはCYTIPまたはCybr)は,cytohesin-1のCoiled-coilドメインを含むN末端領域と結合する39).CASPはSorting nexin 27を介してcytohesin-1をエンドソームにリクルートしており,細胞内輸送の制御に深く関わっている40).
三つのCoiled-coilドメインを有するCoiled-coil domain-containing protein 120(CCDC120)は2005年,酵母ツーハイブリッド法によりcytohesin-2の結合タンパク質として同定されたが,長らく詳細な機能は不明であった.2014年,鳥居らは,CCDC120とcytohesin-2が複合体を形成し,神経細胞の突起伸長に必要であることを示した41).CCDC120はcytohesin-2のCoiled-coilドメインを介して相互作用し,ともに小胞内に局在して順行輸送によって成長円錐に運ばれ,Arf6を活性化することで突起伸長を制御している.
CNK(connector enhancer of KSR)は,タンパク質相互作用に関わるさまざまなドメインを有すことから,Ras-MAPキナーゼシグナル経路のスキャフォールドタンパク質として機能しており,哺乳動物ではCNK1, 2, 3が知られている.すべてのCNKはcytohesinのCoiled-coilドメインと結合する.CNK1はcytohesin-1と結合し,インスリンの刺激依存的に細胞膜にリクルートされ,Arf6を介してホスファチジルイノシトール4-リン酸5-キナーゼ(PIP5K)の活性化を引き起こす42).CNK2はX染色体連鎖性精神遅滞の原因遺伝子の一つとして報告されていた.精神遅滞の患者は,しばしば神経細胞の樹状突起スパインの形態異常を伴う認知機能の障害を呈するため,CNK2もその過程に関与すると予想されていた.Limらは,質量分析法を用い,CNK2がcytohesin-1, 2, 3のほか,RacのGTPase活性化タンパク質(GTPase-activating protein:GAP)として機能するVilse(またはARHGAP3),RacとCdc42に対するGEFとして機能するα-PIXとβ-PIX,さらにRacとCdc42のエフェクターであるPAK3とPAK4などとシグナル複合体を形成することを明らかにした.CNK2とこれらの複合体の結合が阻害されることにより,活性型Racと不活性型Rac間のバランスが崩れ,スパイン構造に障害が起こることが考えられた43).さらにごく最近,チロシンキナーゼ受容体AXLの下流でCNK2がcytohesin-1または-3によるArf6の活性化を介してRac1とRhoAの活性を調節し,がん細胞の遊走過程を制御していることが明らかとなった44).このように,CNK2はさまざまな細胞機能においてRacシグナルとArfシグナル経路の足場を提供する役割を果たしているようだ.CNK3はIPCEF1(interactor protein for cytohesin exchange factor 1)とも呼ばれ,HGFによる細胞遊走過程においてcytohesin-2とArf6の活性化を介して制御している可能性がある45).
FRMD4A(FERM domain containing 4A)は,酵母ツーハイブリッド法により,cytohesin-1の結合タンパク質として同定された46).FRMD4Aはcytohesin-1とPar-3をアドヘレンスジャンクションに局在させ,Arf6の活性化を介して,上皮細胞の極性形成を制御する.FRMD4Aの遺伝子多型は,アルツハイマー病の遺伝的リスク要因の一つとしても報告されている47).Yanらは,FRMD4Aがcytohesin-1とArf6を介してtauの分泌を制御することを報告しており,アルツハイマー病の神経細胞内において蓄積することが知られているtauの分泌メカニズムの一端を担っている可能性が示された48).FRMD4Aは,先天性小頭症によって知的障害を呈する患者でフレームシフトを起こす変異が検出されている49).一方,FRMD4Aと同じファミリーであるFRMD4B[別名GRSP1(Grp1 signaling partner 1)]は,cytohesin-3と結合することが知られており,インスリンの刺激に応じてcytohesin-3との複合体を細胞膜直下に移行させる役割を果たしている50).
酵母ツーハイブリッド法によって同定されたTamalin[別名GRASP(Grp1-associated scaffold protein)]も自身のCoiled-coilドメインを介してcytohein-3と結合する51).TamalinのPDZドメインを含むN末端領域は,代謝型グルタミン酸受容体とも結合しており,cytohesin-2の活性化を介して受容体をシナプス後膜に局在化させる役割を担っている52).また,TamalinのPDZドメインは神経栄養因子受容体TrkC受容体とも結合し,cytohesin-2とArf6を介してRac1シグナルの活性化を誘導している53).Tamalinはプロリンに富む領域を有しており,これを介してDock180のSH3ドメインに結合し,Rac1を活性化しているようだ54).このように,Tamalinはシグナルソームのプラットフォームとなっている.さらにごく最近,グリア細胞におけるTamalinの新しい機能についても報告がなされている.Tamalinをノックアウトしたゼブラフィッシュおよびマウスでは神経細胞とオリゴデンドロサイトの変性およびミエリン膜の形成不全が観察された55).Tamalinノックアウトゼブラフィッシュの脊髄から単離した神経細胞では,代謝型グルタミン酸受容体5がアップレギュレーションされていたため,この受容体の制御異常が神経変性などを引き起こした原因の一つと考えられる.
その他のCoiled-coilドメイン結合タンパク質のうちGαqは,cytohesin-2と直接結合することが報告されている56).同じグループが,cytohein-1との結合も報告しており57),いずれもArf6の活性化を介してGαq共役型受容体のインターナリゼーションを制御している
インスリン受容体もまた,Cytohesin-2のCoiled-coilドメインとPHドメインに結合し,インスリン刺激依存的にArf1の活性化を制御している58).
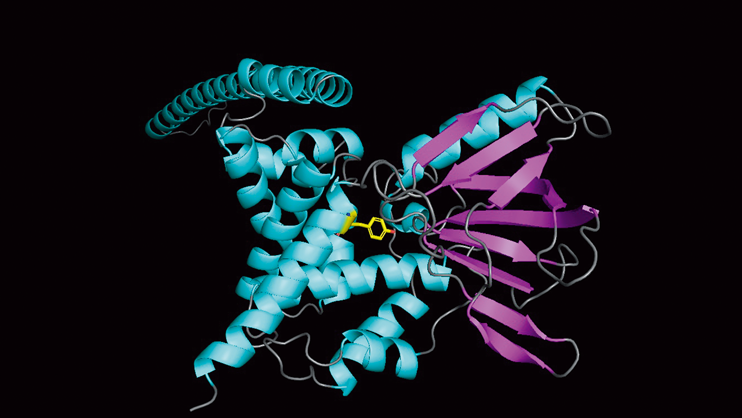
Cytohesin-2どうしがCoiled-coilドメインを介してホモ二量体を形成することで,細胞膜直下での局在を安定化させているという報告もある59).実際,cytohesin二量体の構造解析もなされている60).PHドメインを介して細胞膜に結合するcytohesin二量体は,Sec7とPHドメイン間のリンカー部位とC末端の塩基性アミノ酸に富む領域が,Sec7ドメインの活性化部位を覆うことにより自己活性抑制型を維持している.抑制が解除されると,塩基性アミノ酸領域が細胞膜に結合し,ArfのGTP型と結合する.これにより,Sec7とPHドメイン間のリンカー部位がSec7より外れ,Sec7ドメインの活性化部位が完全に剥き出しとなり,活性化される.二量体を形成しているcytohesinは,片方のPHドメインのみが細胞膜に結合しているが,PHドメインが交互に切り替わることにより,膜への結合効率を上昇させているのではないか,と推測されている.
Munc13-1と呼ばれるシナプス前膜のアクティブゾーンを構成するタンパク質は,cytohesin-1のCoiled-coilドメインに結合する61).Munc13-1はシナプス前膜に局在するSNARE複合体とも相互作用するため,cytohesin-1をシナプス前膜のアクティブゾーンに局在化させている.
最後に,酵母ツーハイブリッド法により,cytohesin-2の結合タンパク質として同定された分子がpallidinである62).pallidinとcytohesin-2は海馬神経細胞において,エンドソーム輸送と樹状突起の形成に関与している.
以上のように,Coiled-coilドメインを介したcytohesinサブファミリー結合タンパク質のうちスキャフォールドタンパク質は,cytohesinの細胞内局在を制御するケースが多い.
b.Sec7ドメインを介した結合タンパク質
Cytohesin-1同定の経緯から,cytohesin-2, 3, 4も細胞接着分子の細胞質側に結合しているシグナル複合体に含まれる分子であることが推定されていた.cytohesin-1に関しては,それがLFA-1(αLβ2インテグリン)であり,cytohesin-1がLFA-1と結合することで,インテグリンとしての機能発現に関与していることが明らかにされている63).cytohesin-3もSec7ドメインを介してインテグリンと結合することが知られている64).
EGF(epidermal growth factor)受容体もまた,cytohesin-2のSec7ドメインを介して結合している.cyotohesin-2のSec7ドメインには,EGF受容体のjuxtamembraneドメインに結合する領域があり,これがカルモジュリンのEGF受容体結合部位と類似していることから,cytohein-2とカルモジュリンにはEGF受容体の活性を修飾する共通のメカニズムが存在するのではないか,と推測されている65).
ARFRP1(ADP-ribosylation factor-related protein 1)は,Arfファミリー低分子量GTP結合タンパク質と比較的相同性の高いGTPaseである.酵母ツーハイブリッド法により,ARFRP1の結合タンパク質として,cytohesin-1のN末端領域とSec7ドメインが同定された66).ARFRP1はcytohesin-1の細胞膜移行を阻害することにより,Arfを介したPLDの活性化を抑制している.
c.PHドメインを介した結合タンパク質
低分子量GTP結合タンパク質のなかには,GEFの触媒活性ドメインであるSec7ドメインを介さずにcytohesinと結合するものがある.GTP結合型のArf6は,cytohesin-2および-3のPHドメインと結合し,それらを細胞膜へリクルートしている67).Arlファミリー低分子量GTP結合タンパク質のArl4a, Arl4c, Arl4dもまた,cytohesin-2のPHドメインと結合することで,細胞膜への移行に関与している68).Arl4dによるcytohesin-2の膜移行により,Arf6が活性化され,アクチン骨格の再編成と細胞遊走が促進される69).cytohesin-2のみならず,cytohein-1,-3,-4のPHドメインもArlによってリクルートされるようだ.
Gq共役型受容体であるアデノシンA2A受容体もcytohesin-2のPHドメインと直接的に結合する.cytohesin-2との結合は,A2A受容体アゴニストによるcAMPの産生には影響を及ぼさないが,A2A受容体によるMAPキナーゼの活性化に関与しているようだ70).
Rabファミリー低分子量GTP結合タンパク質Rab27aのGAPであるEPI64(またはTBC1D10A)もcytohein-2の結合タンパク質として同定された71).PI3キナーゼによって産生されたPIP3はcytohesin-2を細胞膜にリクルートし,同時にEPI64もcytohesin-2と結合することで細胞膜に移行する.膜直下でcytohesin-2はArf6の活性化を,EPI64はRab27aの不活性化を介してグルコース依存的なエンドサイトーシスを制御している.
FE65は,脳に豊富に発現するアダプタータンパク質で,当初APP(amyloid precursor protein)に結合するタンパク質として同定された.FE65はまた,低分子量GTP結合タンパク質やそのエフェクターと結合することもよく知られている.たとえば,Rhoファミリー低分子量GTP結合タンパク質のRac1のGEFであるDock180はELMO1と複合体を形成しているが,FE65はELMO1と直接結合し,Rac1の活性化と神経細胞の突起伸長を制御している72).その後,同じグループによって,FE65はcytohesin-2のPHドメインとも結合し,Arf6の活性化を介して神経突起伸長を制御することが報告されている73).
最後に,cyotohesin-2のPHドメインに結合するタンパク質として,actinin1が知られている.actinin1はspectrinファミリーに属し,アクチンフィラメントとさまざまな細胞骨格分子やシグナル分子間を架橋する役割を担う.抗うつ薬バルプロ酸は神経突起伸長促進作用を有する.我々は,バルプロ酸による神経突起伸長がArl4Dの活性化を引き起こし,cytohesin-2とArf6を介して神経突起伸長を制御することを報告していた.Arl4dがcytohesin-2を活性化することは知られていたものの,Arl4dのアップレギュレーションはバルプロ酸刺激下のみで観察され,生理的突起伸長下ではその現象が確認されていなかった.生理的条件下でcyotohesin-2がどのように突起伸長を制御しているかを検討する過程で,cytohesin-2の結合タンパク質として明らかとなったのが,actinin1であった74).
d.塩基性アミノ酸に富む領域を介した結合タンパク質
脂肪組織の発達過程においては,脂肪前駆細胞の遊走と脂肪細胞の分化が行われる.脂肪前駆細胞株3T3-L1細胞の遊走がcytohesinインヒビターSecinH3で阻害された75).3T3-L1細胞はcytohesin-2と-3の両者を発現しているが,遊走に関与するのはcytohesin-2のみであった.さらに,cytohesin-2は,塩基性アミノ酸に富む領域を介して,細胞接着斑タンパク質であるpaxillinと結合し,遊走中の細胞のleading edgeで共局在することでその過程を制御していた.
以上のように,今回はcytohesin側の結合ドメインが同定されているものに限定して,結合タンパク質を列挙した.cytohesinには多くの結合タンパク質が存在するが,その理由の一つがCCDC120のようにcytohesinを適切なタイミングで必要とする部位に局在化させることであり,二つ目はTamalinのようにシグナルソームを形成することで下流のエフェクターと特異的なシグナル伝達を効率よく行うこと,そして三つ目はcytohesinどうしの結合のように構造変化をもたらすことで,厳密な活性制御を可能にすることである.
4)Arf6を不活性化するArfGAP分子
Arfファミリー低分子量GTP結合タンパク質のGTPase不活性化因子であるGTPase加水分解促進分子ArfGAPとグリア細胞との機能関連性は,現在まで一部のGAPのみで指摘されており,これについては「4. Arf6によって制御されるオリゴデンドロサイトの髄鞘化の過程」で述べる.
ArfGAPタンパク質は,31種類の遺伝子によってコードされており,アミノ酸配列の相同性やドメイン構造に基づいて10種類ほどのサブタイプに分類される76).そのドメインの多様性から,ArfGAPはGAP活性を持つのみならず,たとえばGIT1のようにスキャフォールドタンパク質として機能するもの77),あるいはASAP1のようにミオシンと結合することでアクチン骨格系のリモデリングを介して細胞接着や遊走の制御に関わるもの78)など多岐にわたっている.
Arf6に対するArfGAPとして報告されているのは,ArfGAP1-3, ADAP1, 2, SMAP1, GIT1, 2, ASAP1-3, ACAP1-3, ARAP1-3, AGAP3である76).このうち神経細胞との機能関連性が報告されているものがACAP1とAGAP3である.末梢神経系の後根神経節ニューロンが軸索を伸長する際,α9β1インテグリンを含む小胞輸送が行われることが知られている.輸送される方向性はArf6の活性化状態によって決定される.すなわち,活性化因子のARNOまたはEFA6によってArf6が活性化されると逆行輸送が行われ,逆に不活性化因子ACAP1によってArf6が不活性化されると,インテグリンを細胞表層まで順行輸送・リサイクリングし,最終的に軸索伸長が誘導される79).一方,LTPと深く関与するNMDA受容体をベイトとして行った酵母ツーハイブリッド法によってAGAP3が同定された.AGAP3は神経細胞内でNMDA受容体と結合し,Ras/MAPKとArf6経路を介してLTPを誘導する80).
その他のArfGAPに関してはRandazzoなどの優れた総説76, 81, 82)を参考にされたい.
5)Arf6下流のエフェクター分子
Arfファミリー低分子量GTP結合タンパク質結合分子は複数あるが,特にArf6に結合する分子が多数知られている[公的バイオ情報サイトBioGRID4.4(https://thebiogrid.org/)では500種類以上の直接または間接的な結合タンパク質が登録されている].このなかで活性型Arf6であるGTP結合型に結合する分子がどのくらいあるか,不活性型Arf6であるGDP結合型に結合し不活性型を維持する分子があるかどうかは不明である.現在までグリア細胞との機能関連性は一部のエフェクター分子だけが指摘されているが,これは後述する.
感覚神経に代表される末梢神経線維のグリア細胞は,多機能性のシュワン細胞が主たるものであると言っても過言ではない.前駆細胞から分化したシュワン細胞は細胞膜を広げ,神経軸索を髄鞘化する.しかし,中枢神経のオリゴデンドロサイト前駆細胞(双極性細胞)がオリゴデンドロサイト(別名「希突起膠細胞」の名のとおり複数の突起を持つ細胞)へ形態変化する分化過程とは大きく異なり,シュワン細胞はその分化過程において,明確な形態変化を伴わないと考えられている.そのため,シュワン細胞の分化過程を追跡する方法としては,オリゴデンドロサイトの分化段階をモデルとした髄鞘化マーカーの変動を生化学的手法で調べる方法が一般的である88–91).末梢神経系の髄鞘過程は,胎生後期から生後数日までが分化期にあたる88–93).
げっ歯類の髄鞘は生後45日から60日程度で完成する.これはヒトでは出生前後を含め,約1年間に相当する93).シュワン細胞の髄鞘は神経軸索の周りを100回程度覆うダイナミックな形態変化を伴うため,その過程に細胞形態を制御するさまざまな低分子量GTP結合タンパク質が関わることが知られている94, 95).Arf6はその特性からも,これらの低分子量GTP結合タンパク質の最上流因子であると考えられており96),末梢神経組織の髄鞘化の中心的役割を担っていると推定される94, 95).
筆者らおよびほかの研究グループ97–99)が,マウスの坐骨神経でArf6の発現変化を調べたところ,髄鞘化前後でほとんど変動がみられなかった.一方,GTP結合型のArf6は発生期全体にわたって高レベルで維持される必要があることもわかった99).そこで,後根神経節神経前駆細胞からシュワン細胞と感覚神経細胞をそれぞれ95%以上まで精製単離し,シュワン細胞と感覚神経細胞の試験管内共培養システムによりArf6の上流に存在する活性化因子を探索したところ,数あるArf6の交換因子のなかでcytohesinファミリーがその中心をなすことを突き止めた98, 99).詳細に解析したところ,胎生期から分化期に相当する時期ではcytohesinファミリーのなかでcytohesin-1のみが発現し,その後はcytohesin-2がcytohesin-1に置き換わるように発現上昇した一方,cytohesin-1の発現は急速に低下していた.すなわち,髄鞘化の過程で実際にシュワン細胞が軸索周囲を巻く時期はcytohesinファミリーのうちのcytohesin-2が主体的に機能することが明らかとなった99).
シュワン細胞のシグナル伝達メカニズムにおいてチロシンキナーゼ型受容体分子であるヘテロ結合型ErbB2とErbB3は最もよく研究されており,シュワン細胞の胎生期の運命決定から生後の髄鞘化まですべてに積極的に関与している.ErbB2は神経細胞から提示されるニューレグリン-1(NRG1)などのリガンドには結合できないが強いキナーゼ活性を有し,ErbB3はNRG1と結合するがキナーゼ活性がないか非常に低いと考えられている90, 91).ErbB2/3は現在まで知られているシュワン細胞運命決定をつかさどるほぼすべての転写因子の上流にあると推定されている90, 91).Cytohesin-1はErbB2/3や,他のさまざまなチロシンキナーゼ型受容体によって活性化される非受容体型チロシンキナーゼFynによって,そのC末端がリン酸化され活性化されることがわかっている98).さらに,活性化されたArf6はシュワン細胞特異的エフェクターであるBcl2ファミリー分子の一つであるBcl2l12と結合し,線維状アクチンの形成を促進する100).おそらくBcl2l12によるアクチン骨格の再編成がトリガーとなり髄鞘化が進むと考えられる.
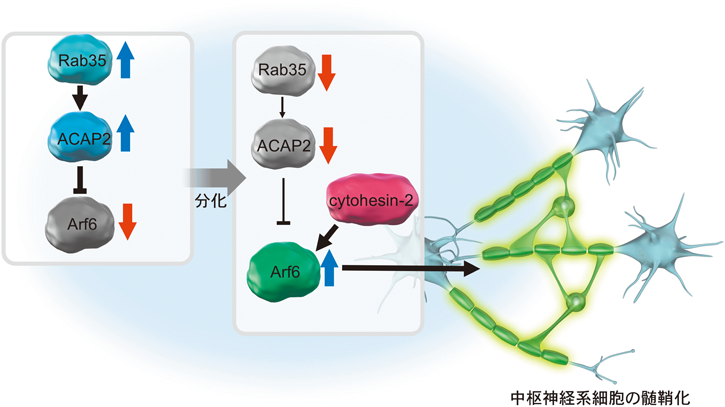
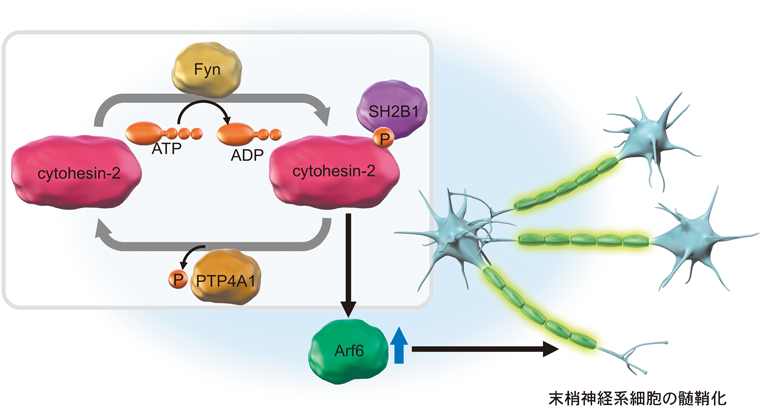
発生が進行するとともに,Arf6の活性を維持するcytohesin-1がcytohesin-2に変わり,髄鞘化過程をさらに促進する.cytohesin-2もcytohesin-1の活性化メカニズムと類似しており,FynがそのC末端をリン酸化することで活性化されるが,その詳細なメカニズムは非常にユニークである(図5).坐骨神経においてcytohesin-2の発現誘導に伴って脱リン酸化酵素であるprotein tyrosine phosphatase 4A1(PTP4A1)とSrc homology 2 family member B1(SH2B1)の発現上昇がみられる.シュワン細胞にはリン酸化チロシンに特異的に働くPTP4A1, protein tyrosine phosphatase non-receptor type 1(PTPN1),PTPN13, PTPN2の4種類の脱リン酵素の転写産物が存在するが,これらのなかでPTP4A1のみがリン酸化され活性化されたcytohesin-2を脱リン酸化できる99).一方,リン酸化されたcytohesin-2と特異的に結合する分子をゲノムワイドに調べたところ,SH2B1が同定された.興味深いことに,SH2B1はリン酸化されたcytohesin-2に特異的に結合し,PTP4A1による脱リン酸化と拮抗することでcytohesin-2の活性を維持することが判明した(図6)99).PTP4A1とSH2B1の発現は生後初期にはほとんど確認されないため,このメカニズムはcytohesin-2に特異的なものであると考えられた.また,オリゴデンドロサイトと同様に,Arf6の負の制御因子としてACAP2が関与する可能性が考えられる.
ここまでは末梢神経組織のなかで厚い髄鞘を持つAβ線維(神経伝導速度が早い)を構成するシュワン細胞を中心に述べた.一方,無髄線維であるC線維(神経伝導速度が遅い)を構成し,神経軸索に沿うかたちで存在する亜型シュワン細胞が存在する.この細胞にもハウスキーピング遺伝子産物に相当するArf6が発現していると推定されるが,現在までに報告はない.無髄線維構成シュワン細胞が一層だけ髄鞘化する能力を持つ細胞であると仮定すると,この細胞膜の形態変化にも多機能性のArf6が関与する可能性は高い.一方,シナプス周囲の過剰な神経伝達物質を吸収し,神経細胞に栄養分子をトランスサイトーシスするアストロサイトに相当する役割を持つサテライトグリア細胞(satellite glial cell)も末梢神経組織に存在する101, 102).Arf6はエンドサイトーシスやエキソサイトーシスにも必須な分子であるため,Arf6がサテライトグリア細胞における機能制御にも関与している可能性がある.
末梢神経組織のグリア細胞を分類できる機知の生化学的マーカーはわずかであり,そのことが末梢神経系グリア細胞の研究を遅延させている原因の一つであると考えられる.Arf6を切り口にして,それらの形態形成のメカニズム解明が進むことが期待される.