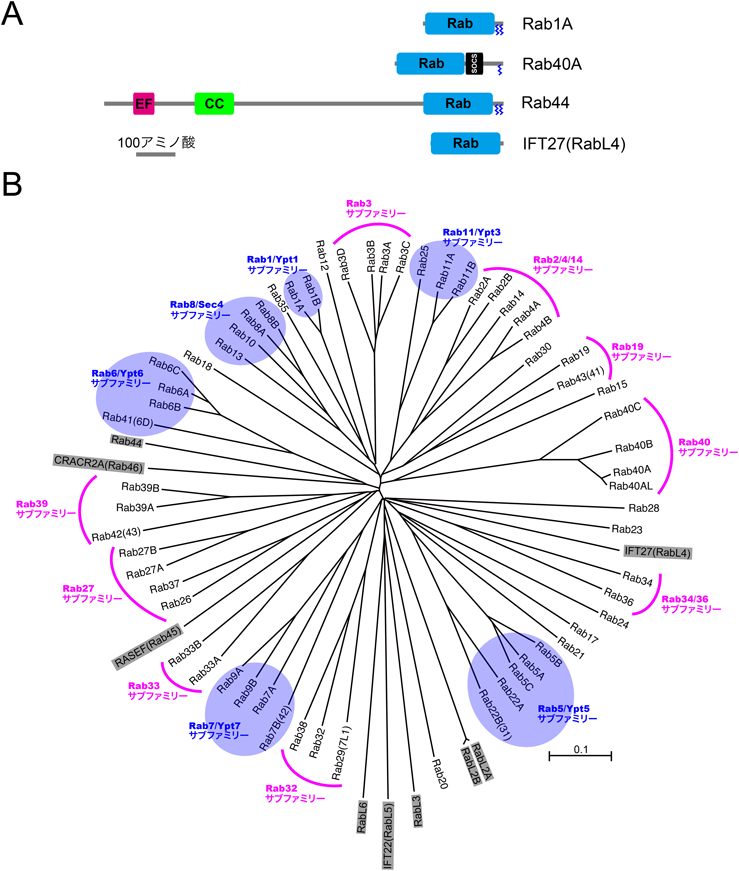
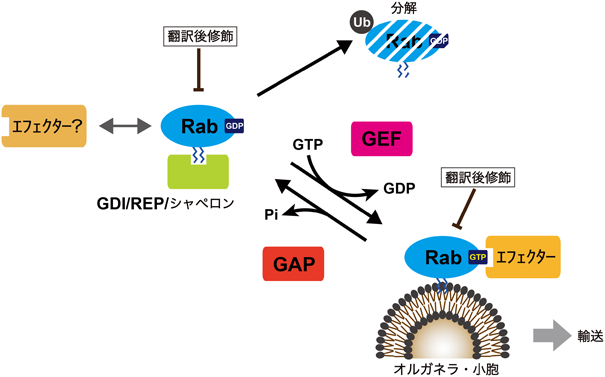
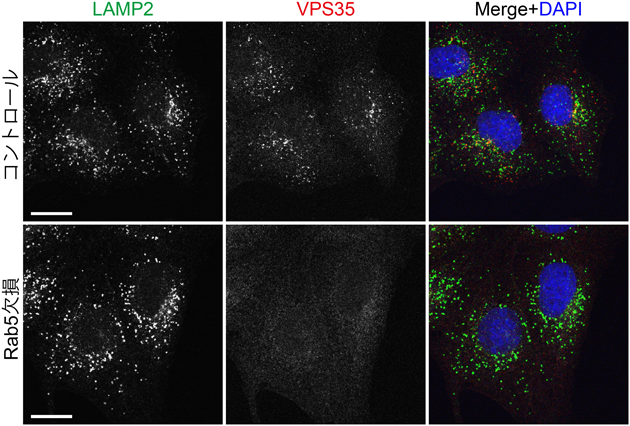
Rabファミリーによるメンブレントラフィック制御の新潮流New trends in the control of membrane traffic by Rab family small GTPases
東北大学大学院生命科学研究科膜輸送機構解析分野Laboratory of Membrane Trafficking Mechanisms, Department of Integrative Life Sciences, Graduate School of Life Sciences, Tohoku University ◇ 〒980–8578 宮城県仙台市青葉区荒巻字青葉6–3 ◇ Aobayama, Aoba-ku, Sendai, Miyagi 980–8578, Japan