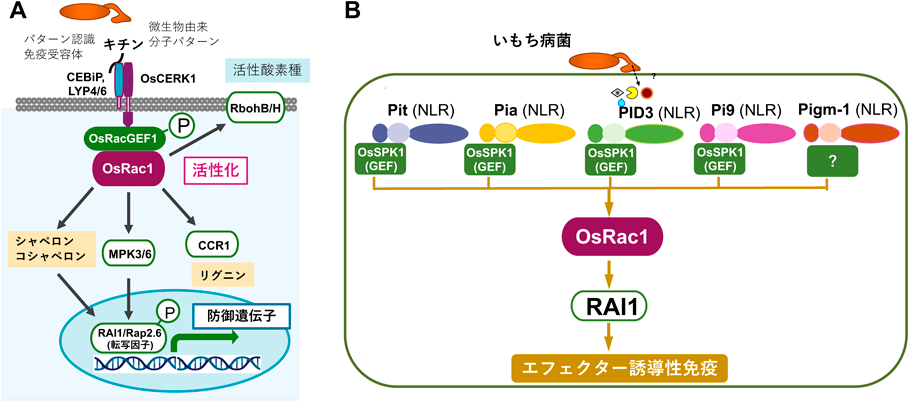
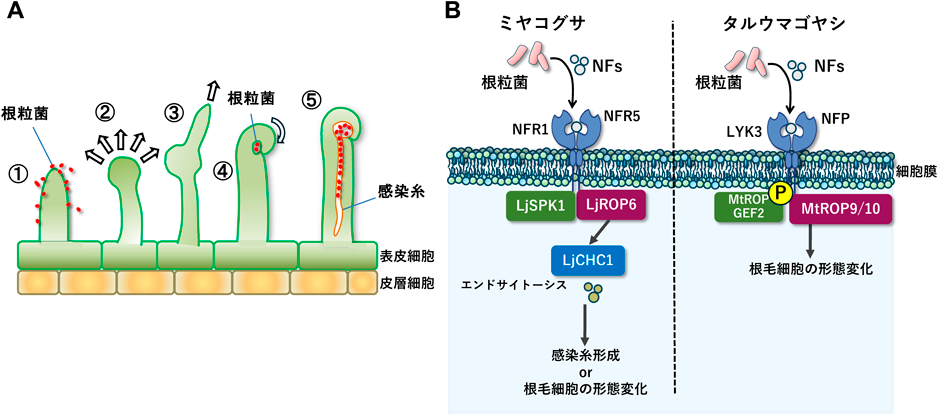
植物–病原菌の相互作用におけるRac/Ropファミリー低分子量GTP結合タンパク質の役割Role of Rac/Rop family small GTPases in plant-pathogen interactions
1 理化学研究所環境資源科学研究センターCenter for Sustainable Resource Science, RIKEN ◇ 〒230–0045 神奈川県横浜市鶴見区末広町1–7–22 ◇ 1–7–22 Suehiro-cho, Tsurumi-ku Yokohama-shi, Kanagawa 230–0045, Japan
2 立命館大学薬学部薬学科College of Pharmaceutical Sciences, Ritsumeikan University ◇ 〒525–8577 滋賀県草津市野路東1–1–1 ◇ 1–1–1 Nojihigashi, Kusatsu, Shiga 525–8577, Japan
3 岡山大学資源植物科学研究所Institute of Plant Science and Resources, Okayama University ◇ 〒710–0046 岡山県倉敷市中央2–20–1 ◇ 2–20–1 Chuo, Kurashiki, Okayama 710–0046, Japan