我々の日常はカレーライスやコーヒーのように香ばしく心惹かれる香りや,かび臭さのように遠ざけたくなるようなものまでさまざまな匂い分子に囲まれている.嗅覚はライフサイクルにおいて欠かすことのできない感覚の一つであり,外界に存在する多様な匂い分子(分子量約300以下の揮発性低分子化合物)は,鼻腔上部の嗅上皮(olfactory epithelium)の嗅神経細胞に存在する嗅覚受容体(olfactory receptor:OR)によって受容される.Gタンパク質共役型受容体(G protein-coupled receptor:GPCR)である嗅覚受容体の存在が知られるようになったのは,BuckとAxelが嗅覚受容体候補遺伝子のクローニングに成功した1991年にさかのぼり,彼らは2004年にノーベル医学生理学賞を受賞している1).同じく2004年に発表されたヒトゲノム配列からは嗅覚受容体の機能遺伝子として396個が同定されている2).嗅上皮には嗅覚受容体に加えて,微量アミン関連受容体(trace amine-associated receptor:TAAR)も発現しており,げっ歯類主嗅覚系におけるフェロモン受容体候補として知られている3).
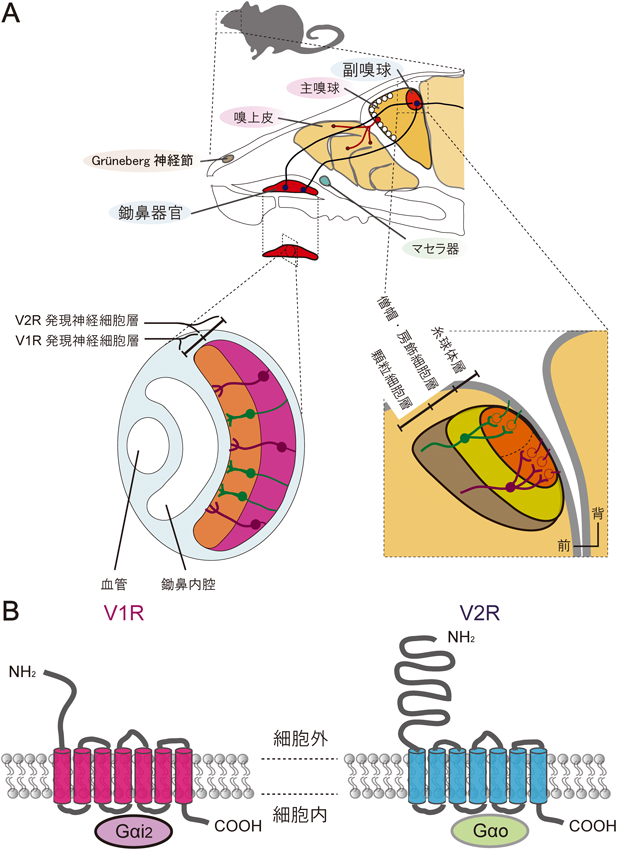
一方,マウスなどのげっ歯類を筆頭とした陸生の脊椎動物の多くは嗅上皮だけでなく,鼻腔下部に位置する鋤鼻器官(vomeronasal organ:VNO),Grüneberg神経節,マセラ器と嗅覚に関連した複数の受容器官を有している(図1A).これらのうち鋤鼻器官はフェロモン等のリガンドを介したコミュニケーションにおいて重要な役割を担っている.フェロモンは「生物が体外に分泌し,同種の他個体において作用する化学物質」と定義され,同種間のコミュニケーションに重要な役割を担っている.1959年にButenandtによって発見されたメスのカイコガが放出するボンビコールは化学的に機能が同定された初めてのフェロモンとして知られている4).
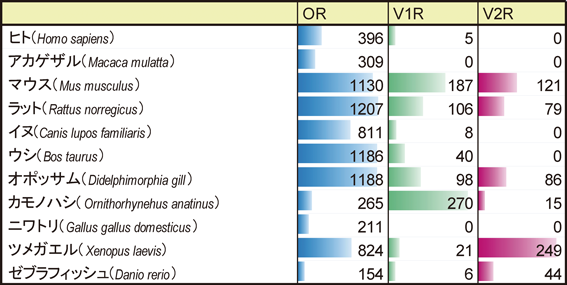
鋤鼻器官に分布する鋤鼻神経細胞(vomeronasal sensory neurons:VSNs)に発現する受容体(鋤鼻受容体)を介してフェロモン物質などの情報処理を行う感覚系は,匂い分子を介したコミュニケーションである主嗅覚系と対比させ,副嗅覚系や鋤鼻系と呼ばれている.鋤鼻受容体(vomeronasal receptor:VR)には,マウス尿中に含まれる2-ヘプタノンのような揮発性フェロモンなどを受容するV1R受容体(vomeronasal type 1 receptor:V1R)や,雄マウスの涙液中に含まれるexocrine gland-secreting peptide 1(ESP1)など不揮発性フェロモン物質を中心に受容するV2R受容体が発現している(図1B).マウスゲノム上にはそれぞれ187個のV1Rと121個のV2Rの機能遺伝子が存在する(図2)5–7).
2018年にはシーラカンスゲノムの解析によって,古代魚から哺乳類まで高度に保存されているフェロモン受容体候補遺伝子として,ancient vomeronasal receptor 1(ancV1R)が発見された8).ほぼすべてのVSNで発現しフェロモン受容体と共発現しているancV1Rは,フェロモン感受性に影響を及ぼすと考えられ,ancV1Rを欠損させた雌マウスでは雄マウスを正しく認識できないことに起因するマウント行動の拒絶が引き起こされる9).ヒトでは痕跡器官となっている鋤鼻器官であるが,げっ歯類をはじめとした動物においては正常な個体間コミュニケーションに重要な役割を果たしている10).
3. さまざまな鋤鼻リガンドによって制御される社会性行動
では,鋤鼻嗅覚系のリガンドとして具体的にどのようなものが存在しているのであろうか.これまでの知見からは性特異的なリガンドが数多く報告され,攻撃性や性行動といった性の認識が大切な行動における重要性が示されている.本節ではV2Rで受容されるリガンドに焦点をあてて解説を行う.マウスの尿には多数の匂い物質とともにペプチド等も含まれており,社会性を制御する化学感覚シグナルとして機能している.テストステロンや成長ホルモン依存的に雄マウスで産生される主要尿タンパク質(major urinary protein:MUP)もその一つであり,MUP3は雄マウスの攻撃性を亢進させる11).一方で,尿に含まれるMUPよりも低分子の雄特異的化合物(3 kDa)が雄マウスの攻撃性を高めることも知られており,リガンドは未同定であるもののV2RのひとつであるVmn2r53で受容されることが知られている12).分泌する雄マウス自らの攻撃性を高めているリガンドとしてはESP1が知られている13).
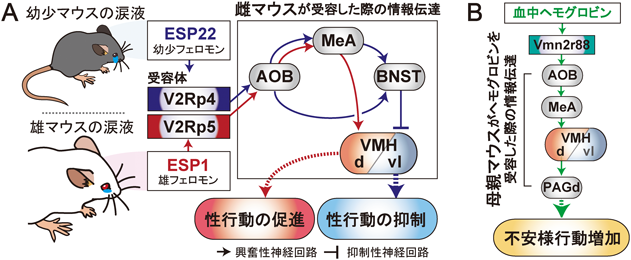
驚くべきことに,ESP1は尿ではなく雄マウスの涙液中に含まれる約7 kDaのペプチドである14).ESP1は鋤鼻受容体V2Rp5(Vmn2r116)を特異的な受容体として,雄マウスの攻撃性亢進のほかに,雌マウスが受容した際のロードシス反射の促進(雌マウスの性行動促進)(図3A,赤色),妊娠中のマウスが受容した際のブルース効果の促進といった多様な役割を担っている6, 15).ブルース効果とは,交尾後に交尾相手とは異なる系統の雄マウスと接触すると流産が引き起こされる現象のことであり,MHCペプチド分子の系統差などが原因として示唆されていた16, 17).2018年に発表された研究では,1959年に現象が報告されてから50年以上を経て,その原因物質の一つとしてESP1が同定されたことになる.
ESPはMUPと同様に遺伝子ファミリーを形成しており,マウスゲノムには38種類の,ラットゲノムには10種類のESPがコードされている18).ESPファミリーのなかでESP1に続いて解析が進んでいるのが,2~3週齢という幼少期マウスにおける時期特異的な分泌がみられる約10 kDaのぺプチドESP22である.幼少フェロモンESP22は,雄マウスが受容した際に性行動を抑制すること(マウント行動の減少)が最初に明らかにされた19).その後,ESP22の受容体としてESP1受容体であるV2Rp5と高い相同性を有するV2Rp4(Vmn2r115)が同定され,ESP22を雌マウスが受容した際の性行動抑制効果(雄マウスのマウント行動に対する拒絶行動の増加)が示された20)(図3A,青色).
鋤鼻受容体は異なる生物種由来のリガンドに対する応答にも関わり,個体の適切な応答を導出している.ラットの涙液中に含まれるペプチドcystatin-related protein 1(rat CRP1)はVmn2r28を含む複数種類のマウスV2Rを活性化し体温や心拍数を調節している21).また,マウスでは多様な生物種の血中ヘモグロビンがVmn2r88を中心とした受容体で受容され,母親マウスにおける不安様行動を増加させることが知られている22, 23)(図3B).このように,すでに同定されている鋤鼻リガンドと受容体のペアは数えられる範囲にとどまるものの,はたして鋤鼻受容体の脱オーファン化は今後どのように進捗していくであろうか.
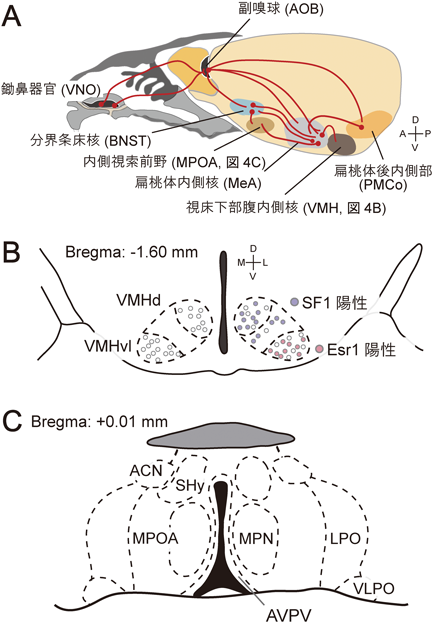
鋤鼻リガンドがさまざまな生理作用や社会性行動を引き起こすことができるのは,リガンド情報が脳に伝達され適切な情報処理がなされるからである.では,受容体で受け取られた鋤鼻リガンドの情報はどのように伝達されるのであろうか.個々の鋤鼻神経細胞(VSN)は基本的に1種類の機能的なVRを発現しており,リガンドがVRに結合するとGタンパク質を介した細胞内シグナル伝達によって活動電位が生じる.VSNは軸索を副嗅球(accessory olfactory bulb:AOB)へと伸ばしているが(図1),AOBからは内側核扁桃体(medial amygdala:MeA),分界条床核(bed nucleus of the stria terminalis:BNST),後内側部扁桃皮質核(posteromedial cortical amygdaloid nucleus:PMCo)などを経由して,社会性行動の制御に密接な内側視索前野(medial preoptic area:MPOA),視床下部腹内側核(ventromedial hypothalamus:VMH)へと情報が伝達される(図4A)24).それぞれの脳領域における情報処理の重要性が検証されているが,たとえば,BNSTの亜領域(principal component of BNST:BNSTpr)に発現するアロマターゼ陽性細胞群が,雄マウスにおけるフェロモンを介した性の識別とそれにひもづいた社会性の発現に重要であることが示されている25).また,AOBやMeAの神経活動からは性や系統の情報をデコードでき,これらの脳領域は相手の性や遺伝的バックグラウンドなどの情報をコードしているものと考えられる.
視床下部腹内側核VMHは二つ,または,三つの亜領域に分けて考察がなされることが多く,恐怖反応等に重要なVMHdm[dorsomedial part of VMH, steroidogenic factor 1(SF1)陽性細胞が主に分布する]と性行動や攻撃性の中枢として知られるVMHvl[ventrolateral part of VMH, estrogen receptor 1(Esr1)陽性細胞が主に分布する]に区分することができる(図4B)26).さまざまな鋤鼻リガンドに対してVMHのそれぞれの亜領域が特異的に応答することが知られているが,たとえば,マウスに恐怖反応(フリージング)を引き起こすネコの唾液中の鋤鼻リガンドはVMHdmを活性化させる27, 28).
近年のウイルストレーシングによる解剖学的解析では,MeAからposterior amygdalaやlateral hypothalamus等への軸索投射も明らかにされており,鋤鼻リガンドの情報がこれらの脳領域に伝達されている可能性も示唆される29).視床下部の前乳頭体腹側核(ventral premammillary nucleus:PMv)も鋤鼻リガンド情報伝達における重要な役割を担っており,PMvは雄マウスの尿中リガンドに強く応答し,雄フェロモンの情報を下流のVMHvlへと伝達している12, 30).痛み刺激に対する応答や恐怖反応などに関わりのある中脳灰白質(periaqueductal gray:PAG)は,VMHからの投射を受けて鋤鼻リガンドによるアウトプット調節に関わっていることが知られており,さらなる解析が期待される23, 31).
神経回路基盤の解析が進んでいる雄フェロモンESP1を例にとると,受容体V2Rp5からAOBへとリガンド情報が伝達されたのちに,雄マウスにおいては扁桃体内側核の後腹部(posteroventral MeA:MeApv)からMPOAへの伝達が行われる.一方で,雌マウスではMeApvからVMHd,そして,背側の中脳灰白質(dorsal part of periaqueductal gray:PAGd)へと情報が伝達され,性的二型の性質を持った情報伝達機構が明らかにされている(図3A)31).この特徴はESP1が雄マウスでは攻撃行動を促進し,雌マウスでは性行動を促進するという異なる行動出力を導くこととも矛盾しない.幼少期マウスの涙液中に含まれるESP22が雌マウスの性行動を抑制する際には,BNSTからVMHvlへと投射される抑制性の経路が重要な役割を担っていることが示されている(図3A)20).VMHvlが雌の性行動を促進させる機能を有することを鑑みると,BNSTからの抑制性入力がVMHvlの神経活動を抑えているがゆえに生じる性行動抑制であると推測することができる.ESP1とESP22は相同性の高い受容体で受容されるものの,それぞれが特異的な情報伝達経路を介して性行動を逆方向に制御するという興味深い特徴を有している.
このように鋤鼻系では多様なリガンドが受容され,動物の社会性を制御している.フェロモンを筆頭とした鋤鼻リガンドは行動の有無を決定づけるというよりも,行動の頻度・強度を調節しているものが多いと考えられる.特に,性特異的に分泌されるリガンドは行動の背後に存在する性の識別に重要であると推測される.鋤鼻リガンドの情報が伝達される脳領域は,社会性行動のオン・オフに重要な脳領域であることも多く,鋤鼻からの入力が他の情報と統合されることで,社会性の程度やその対象が適切に調節されているのかもしれない.
社会性行動は脳領域間の相互ネットワーク(social behavior network:SBN)によって制御されていると考えられており,複数の脳領域の重要性が示されている32).提唱されたSBNでは,extended medial amygdala, lateral septum, preoptic area, anterior hypothalamus, ventromedial hypothalamus, midbrainの六つがあげられているが,本稿では鋤鼻リガンドの節にも登場した内側視索前野(MPOA)ならびに視床下部腹内側核(VMH)と社会性のつながりについて概説する.
1)内側視索前野(MPOA)
POA(preoptic area)は脳の腹側に位置し,その吻側に存在する側坐核と尾部側の視床下部の間に位置している.POAはMPOA(medial POA),AVPV(anteroventral periventricular nuclei),ACN(anterior commissural nuclei),SHy(septohypothalamic nuclei)などの亜領域に区分することができ,遺伝子発現やその機能は亜領域ごとに異なっている(図4C)33).MPOAを筆頭としたPOAの亜領域は社会性行動の制御以外においても重要であり,睡眠の制御,体温調節,低温環境下における摂食の調節や,ストレス依存的な不安様行動などに関連している34–37).MPOAによる社会性の制御に関して,本項では雄マウスの性行動,攻撃性,そして,母親マウスの養育行動について解説する.
a.雄マウスの性行動
MPOAにおける社会性行動の制御に関しては,同領域に分布するエストロゲン受容体が着目されている38).ラットを用いた検証で活動量の変化とのつながりが示されていたMPOAのエストロゲン受容体であるが,shRNAを用いてMPOAのエストロゲン受容体1(Esr1)をノックダウンすると雄マウスの性行動が低下することが示されている39).後に発表されている研究では,MPOAのEsr1陽性細胞群(MPOAEsr1)がマウント行動(性行動)や仔の回収行動の発現に重要であることや,Esr1陽性かつ小胞型GABAトランスポーター(vesicular GABA transporter:vGat)陽性細胞群(Esr1+vGat+)が超音波発声(ultrasonic vocalization:USV)を伴った雄の性行動を制御していることが神経活動の記録や光遺伝学ツールなどによって示されている40, 41).また,MPOAを含む亜領域(POA)に分布するタキキニン受容体(Tachykinin receptor 1:Tacr1)発現細胞群が雄マウスの性行動に重要であるという知見も存在するが,POAにおけるTacr1陽性細胞は同じ領域に存在するEsr1陽性細胞の約20%ほどである42).いずれにしても,MPOAEsr1が雄マウスの性行動において主要なアクセルとして機能していることは明らかであろう43).
b.雄マウスの攻撃行動
MPOAEsr1は雄マウスの攻撃性を亢進する回路ネットワークの中心ではないことが示唆されている44).その一方で,MPOAにおいてEsr1陽性かつvGat陽性細胞群 (MPOAEsr1+vGat+)の一部が雄の攻撃行動によって活性化されることも示されている45).はたしてMPOAは雄の攻撃性をどのように制御しているのであろうか.MPOAの神経細胞は攻撃性亢進の中枢であるVMHvlにもその軸索を投射しているが,Esr1陽性かつvGat陽性細胞群のVMHvlへの軸索を活性化すると雄の攻撃性が著しく低下する41, 46, 47).また,雄マウスのMPOAEsr1を吻部(rostral)と尾部(caudal)に分けてそれらの役割を探索した解析も存在する.雌マウスに対して強い応答を示すrostral(rMPOAEsr1)-VMHvlの経路に対して,caudal(cMPOAEsr1)-VMHvlは攻撃行動と同期的に活性化される.そして,cMPOAEsr1-VMHvlは遭遇した雄マウスの社会的順位(攻撃性)の認識に関わり,不利な状況下での攻撃行動を抑制していることが明らかにされている47).
c.母親マウスの養育行動
MPOAは養育行動の制御にも欠かせない.げっ歯類の養育行動には,巣作り,仔の回収行動,母親マウスが示す母性攻撃行動など各要素が存在する.single cell RNA解析からは,養育行動に重要なMPOA神経細胞群の一部が抑制性神経細胞(MPOAvGat)であることが示されており,光遺伝学ツール等を用いた解析ではPAGに投射するMPOAvGatが仔の回収行動などの行動に重要であることが示されている37, 45).それ以外にも,MPOAのGalanin陽性細胞群(MPOAGal)やMPOAEsr1から腹側被蓋野(ventral tegmental area:VTA)への抑制性の投射(MPOAEsr1+vGat+ →VTA)が仔の回収行動を筆頭とした養育に重要であることが発表されている48, 49).MPOAGalに関しては,ステロイドホルモンであるエストラジオールやプロゲステロンがMPOAGalに作用することによる可塑的な変化が,養育に向けた妊娠期に生じていることも示されている50).
MPOAは領域をさらに細分化した解析も進んでおり,亜領域の一つであるcMPOA(central part of the MPOA)に分布するカルシトニン受容体(Calcitonin receptor:CalcR)発現神経細胞の養育における重要性が示されている51).POAにはCalcRのリガンドであるアミリンや神経ペプチドオキシトシンを産生する細胞群などが発現しており51, 52),神経ペプチドや神経伝達物質がどのように養育行動と関わっているかや,父性養育行動の制御にも関与しているかなど今後の研究の進展が期待される.
2)視床下部腹内側核(VMH)
視床下部腹内側核VMHの内側部(VMHdm)は脳由来神経栄養因子(brain-derived neurotrophic factor:BDNF)やSF1を発現する神経細胞が分布しており,摂食制御や先天的な恐怖行動の発現などに重要である(図4B)53–55).
一方で,Esr1などを分子マーカーとして社会性とのつながりを調べた研究が数多く存在している外側部(VMHvl)であるが(図4B),近年のsingle cell RNA解析からは,約4000の神経細胞からなるVMHvlが17のグループに分類された.VMHvlの神経細胞は異質性が高く,各グループが異なる行動に関与していることも示唆されており,さらなる解析が待たれるところである56).本項ではVMHvlに焦点をあて,同領域が持つ本能的な社会性行動の制御機構について解説する.
a.攻撃行動・社会的ヒエラルキーとVMHvl
カリフォルニア工科大学で研究グループを主宰し,社会性行動の脳内ダイナミクスに関する数多な研究を発表し続けているDavid Anderson博士(https://davidandersonlab.caltech.edu/)であるが,彼のグループの論文において初めてVMHvlという単語が登場したのは2011年にさかのぼる.彼らはアデノ随伴ウイルスベクターを用いることで,VMHvlに青色光照射依存的に神経活動を活性化させるチャネルロドプシン2(Channelrhodopsin-2:ChR2)を発現させた.そして,光照射による神経活動の活性化によって雄マウスの攻撃行動を人為的に引き起こすことに成功し,活性化されたマウスは膨らませたゴム手袋に対しても攻撃性を示すようになった57).2014年に同グループから発表された論文では,VMHvlに分布するEsr1陽性細胞(VMHvlEsr1)の神経活動の強度の違いによって表出される行動が異なるという概念が提唱されたが,当論文が後に続くVMHvlEsr1に焦点をあてた研究の端緒となっている58).Andersonの研究グループからは,VMHvlEsr1の単一神経細胞解像度での記録と,社会性行動の各要素を脳の活動で記述するモデリングも行われた.雄マウスどうしの相互作用によって活動が徐々に増加する神経集団をVMHvlEsr1に発見し,雄マウスの攻撃行動の亢進と相関していることを見いだした.彼らの提唱は,「VMHvlEsr1の活動変化と攻撃性の促進という社会性行動の推移の関係性が,連続的な状態変化を表現するモデルであるライン・アトラクターで説明できる」というものである59).
Anderson研究室の出身であり現在ニューヨーク大学において研究室を主宰するDayu Lin博士(Lin D. et al., Nature, 201157)の筆頭著者,https://www.dayulinlab.org/)の独立後の研究からは,VMHvlEsr1は雄マウスだけでなく雌マウスによる攻撃行動にも重要であることや,吻部VMHvl(anterior VMHvl:aVMHvl)と尾部VMHvl(posterior VMHvl:pVMHvl)の役割が異なり,aVMHvlEsr1は社会的順位の高い個体によって攻撃されたときの防御行動の表出に,pVMHvlEsr1は自らが攻撃行動を示す際に重要であることが示されている60, 61).また,pVMHvlの興奮性神経細胞(VMHvlvGlut2)が中脳灰白質の一部(lateral periaqueductal gray:lPAG)に軸索を投射し,「齧る」という攻撃行動における動作出力に関わっていることや,勝つという経験による勝利者効果(Winner Effect)にVMHvlEsr1の可塑性が寄与していることが明らかにされている62, 63).
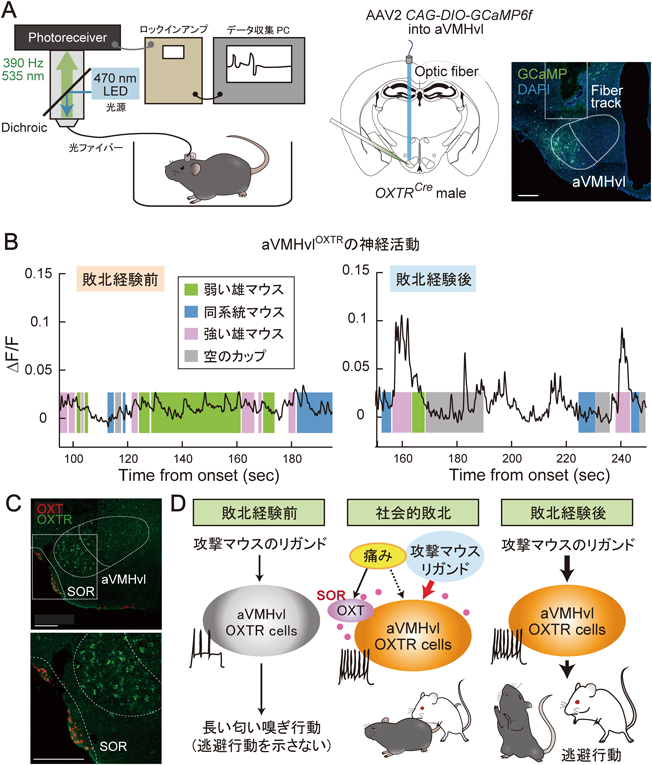
社会的ヒエラルキーの中に存在するコミュニティにおいて,攻撃行動(aggression)が相手個体の社会的敗北(social defeat)と対をなして存在することは自明である.社会的順位の高い個体(aggressor)に遭遇し敗北を経験したマウスは,再度aggressorに遭遇した際に強い逃避行動を示す64).すなわち,敗北経験前の頻繫なアプローチや匂い嗅ぎ行動と比較するとまったく異なる行動パターンを見せるようになる.このような可塑的な行動変容の背後には行動を制御する神経回路基盤における可塑性が存在していると予想された.社会的敗北時に重要であることが示されていたaVMHvlであるが,同領域にはEsr1陽性細胞だけでなくオキシトシン受容体(oxytocin receptor:OXTR)発現細胞も豊富に分布する65, 66).筆者がLin研究室における研究を開始した2018年当時,VMHvlに分布するOXTRの機能には未解明な点が多く存在した.そこで筆者らは,ファイバーフォトメトリー法(図5A)を用いてaVMHvlOXTRの神経活動の記録を行った67).すると,aggressorに遭遇した際のaVMHvlOXTRの活動を敗北経験前後で比較すると敗北経験依存的に著しく活動が上昇することが明らかになり(図5B),続いて行われた光遺伝学ツール等を用いた解析により逃避行動の発現におけるaVMHvlOXTRの機能的な重要性が示された.aVMHvlOXTRにリガンドであるオキシトシンペプチド(OXT)を供給する脳領域としては,視交叉後部視索上核(retrochiasmatic supraoptic nucleus:SOR)が明らかにされている(図5C)68).本研究からは,SOROXT-aVMHvlOXTRというモチーフが社会的敗北に依存した行動の可塑的な変化に重要であることが示された.VMHvlに発現するペプチド受容体の雄攻撃行動における重要性は,先述したAnderson研究室から発表されている研究成果からも示唆されている69).
b.雌マウスの性行動とVMHvl
ラットなどを用いた研究によって雌個体の性行動における重要性が示されていたVMHであるが,先述したMPOAと同様に組換え酵素Creのドライバーマウスや光遺伝学を筆頭とした解析ツールの充実によって詳細な回路基盤が明らかにされている70, 71).
先述したAnderson研究室でPh.D.を取得したNirao Shah博士率いるスタンフォード大学の研究グループ(https://med.stanford.edu/nirao/about.html)はVMHvlに発現するプロゲステロン受容体(progesterone receptor:PR)を分子マーカーとして社会性を制御する回路基盤の研究を進めており,アポトーシスをVMHvlPRに誘導すると雌マウスの性行動(ロードシス反射の割合)は低下した72).2019年に発表された研究ではVMHvlPRからAVPVへの軸索投射に着目し,性周期依存的に変化する神経接続の可塑性による雌性行動の制御機構を明らかにした73).ちなみにVMHEsr1とVMHvlPRは約92%が共局在している72).
雌マウスは雄のマウント行動に対してロードシス反射を示さない際,発情間期を中心として拒絶反応(rejection)を示すことが多い.別のグループから発表された研究では,aVMHvlのPR陽性細胞群(aVMHvlPR)が雌マウスにおけるrejectionの発現に重要であることが示されている74).前半部で述べたように,幼少フェロモンESP22はBNSTからVMHvlへの抑制性神経細胞を介して雌マウスのrejectionを促進するが20),機能的な接続はVMHvlのなかでもanterior部が担っているのかもしれない.
雌マウスの性行動におけるVMHvlの重要性に関しては,PR以外の分子マーカーに着目した研究も存在する.VMH近辺のサンプルを用いたsingle cell RNA解析からは雌マウスが示す攻撃性に重要な細胞群と性行動をつかさどる細胞群が異なることが示され,前者はNpy2r陽性細胞群(Npy2r+)であり,後者はNpy2r陰性細胞群(VMHvlEsr1+, Npy2r−)であることが示されている75).ほぼ同時にLinのグループから発表された研究では,VMHvlに発現するCckar発現細胞群(VMHvlCckar)が雌マウスの性周期依存的な性行動調節に重要であることが発表されている76).なお,VMHvlEsr1+, Npy2r−とVMHvlCckarはほぼ同一の集団であり,単一神経細胞解像度での神経活動記録からは先述したライン・アトラクターが雌マウスの性行動においても存在するかどうか検証がなされている77).
VMHvlを中心とするネットワークに属する神経細胞の遺伝子発現は雌雄や性周期に依存的であり,血流を通して脳に運ばれるステロイドホルモンの性差などと合わせて,性特異的な社会性行動の発現に関わっていると考えられる78–80).これまでに概説したように,社会性を制御する神経回路基盤はさまざまな脳領域・分子マーカー・神経ペプチドなどに着目して解析が進められている.社会性行動は脳からの綿密な制御を受けているがゆえに,ストレス,精神疾患,加齢などを原因として変調をきたしてしまうことも多い.今後は,ヒトにおける社会性低下の背後に存在する回路の変調やそこからの回復につながる知見も含めて明らかにされていくことが期待される.