哺乳類(ヒトを含む)では,一つの受精卵が細胞分裂を繰り返し,一つの個体へと成長する.胎仔期には,胚の最も背側にある外胚葉の一部が神経板となり,それが陥入して神経管が形成される.神経管は一層の神経上皮細胞からなり,その細胞が分裂して神経管のサイズが大きくなる.神経発生の中期になると,神経上皮細胞はラディアルグリアとも呼ばれるようになる.このラディアルグリアから脳神経系の基本単位である神経細胞が生まれるが,すぐに脳神経ネットワークが構築されるわけではない.複数の発生段階を経て,段階的に脳神経ネットワークに組み込まれていく.脳神経系には神経細胞以外にもグリア系,血管系,免疫系などのさまざまな細胞種が含まれるが,神経細胞の立場からするとこれらの発生段階は,大きく4段階に分けて考えることができる.それらは,(1)神経細胞の誕生と各神経細胞種への運命決定,(2)神経細胞の移動,(3)神経突起の伸長と経路探索,(4)シナプスの形成と刈り込み,である.これらの各段階では,さまざまな遺伝子が働いており,脳神経発生の遺伝子プログラムを完全に解き明かすことが,「神経発生生物学」の究極の目的であるといえる.また,この遺伝子プログラムに異常を来すと,脳神経系がうまく作り上げられず,発達障害やてんかんなどさまざまな精神神経疾患の原因・誘因となりうるため,脳神経系の発生と疾患の研究はある意味で表裏一体の関係にあるともいえる.
脳神経系発生の遺伝子プログラムを明らかにする方法は,in vitro, in vivo, in silicoとさまざまあるが,それらは別々のものではなく,うまく組み合わせることが肝要である.本稿では,筆者のこれまでの体験や思い出をたどりながら,その「遺伝子変異動物を用いた」神経発生生物学の研究について紹介する.私の研究は偶然出会った突然変異動物やその関連遺伝子の解析に基づく行きあたりばったりのものであったが,Ptf1a遺伝子の研究から「各神経細胞種を生み分ける仕組み」に,またAuts2遺伝子の解析から「神経細胞の誕生,移動,突起伸長,シナプス形成の分子機構や,その障害による脳疾患」にアプローチすることになった.
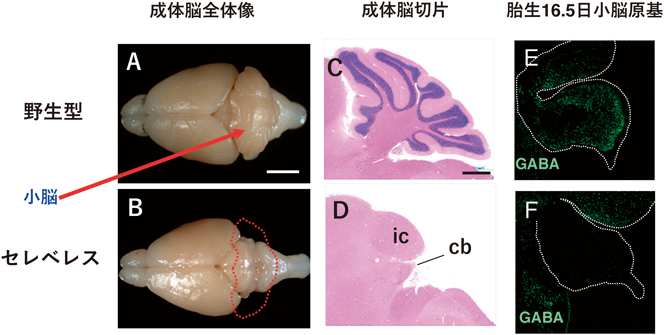
今から四半世紀前の2000年,筆者は京都大学医学研究科の鍋島陽一教授の研究室の助手(のちに助教)で,神経研究チームのリーダーとして働いていた.鍋島研究室では老化に関係するとされるKlotho(クロトー)遺伝子の研究に取り組んでおり,この遺伝子を異所性に発現させるトランスジェニックマウスの作出に取り組んでいた.トランスジェニックマウスは何系統も得られたが,その一つの系統で,ホモ接合体にするとふらつく,転倒するなどの異常行動が観察された.ただ,運動失調症状はあるものの,実際にマウスは元気に活動している.その脳を解剖してみたところ,小脳らしきものがないことに気がついた(図1A, B)1).後でわかったことであるが,このマウスは正常マウスと同等の寿命(約2年半)生きる.ここで不覚にも「おー,生きていくためには小脳はいらないのか」と純粋に感動してしまった.生命維持のための多くの機能は脳幹にあるので,そういうこともありうると思いはするものの,やはり小脳のないマウスを目のあたりにすると衝撃であった.小脳がないという表現型がメンデルの法則どおりに潜性(劣性)遺伝するので,このマウスではある遺伝子が破壊されているのだろうと推測された.確かに,トランスジェニックマウス作製の過程で,関係のない遺伝子が壊されて突然変異体が生み出されるということは少なからずある.とはいっても,「このマウスで何が起こっているのか・いかにして小脳が失われているのか・どんな遺伝子が壊されているのか」まったく謎である.この謎を少しずつ解いていかなければならない.筆者は,この突然変異マウスに「小脳(セレベルム,cerebellum)がない」という意味で「セレベレス(cerebelless)」と名づけた.翌春からは,新入大学院生の中村祥子さんがこのプロジェクトに加わってくれた.
まずは,表現型の解析である.大学院時代にショウジョウバエの神経発生をテーマにしていたこともあり,セレベレスに出会った当時,筆者はマウス脳の解剖学には明るくなかった.そこでたくさんの切片を持って,神戸大学医学部の寺島俊雄教授(当時)にご相談にうかがった.寺島先生は日本を代表する神経解剖学者である.半ば強引に押しかけた私に,寺島先生はいやな顔一つせずに一緒に切片を見てくださった.そしてセレベレスの成体においては小脳皮質が完全に失われており(図1C, D),小脳の内側の構造(小脳核)がわずかに残っているだけであることがわかった.小脳以外にはほとんど異常が認められないが,例外として,下オリーブ核と橋核と呼ばれる神経核が完全に失われていることも明らかになった.
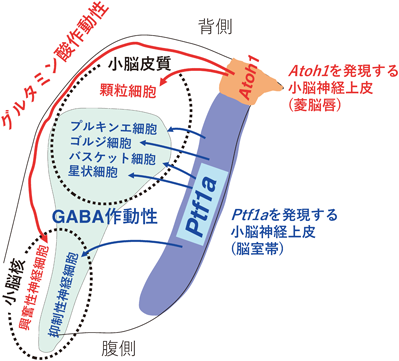
ここで小脳について簡単に述べよう.運動の制御に関わると考えられている小脳は,その大部分を占める外側の皮質と,内側の白質および小脳核から構成されている.小脳に含まれる神経細胞としては,皮質にプルキンエ細胞,顆粒細胞,ゴルジ細胞,バスケット細胞,星状細胞などが,小脳核には興奮性神経細胞と抑制性神経細胞がある(図2に記載された細胞.図2にはセレベレスの論文で解明された事象も記載されているが,それは後述する).図2に赤字と青字で表記したように,顆粒細胞と小脳核の興奮性神経細胞がグルタミン酸を神経伝達物質とする興奮性神経細胞で,それ以外はすべてガンマアミノ酪酸(GABA)を神経伝達物質とする抑制性神経細胞である.これらの,興奮性および抑制性神経細胞が,小脳の神経回路において互いに神経活動を制御し合うことによって,適切な小脳機能が発揮されると考えられている.
発生途上のセレベレス胚のヘマトキシリン・エオジン染色標本を観察すると,プルキンエ細胞層が見当たらないことに気がついた.実際に,マーカーであるカルビンジン免疫染色を行っても,プルキンエ細胞は観察されなかった.それに対して,外顆粒層の細胞,すなわち将来顆粒細胞へと分化するはずの細胞は生み出されていた.だが,この細胞も出生前後から失われていき生後7日にはまったく見えなくなる.実は「外顆粒層の細胞の増殖のためにはプルキンエ細胞から分泌される栄養因子(ソニックヘッジホッグタンパク質)が必要である」という報告2)があるので,セレベレスではプルキンエ細胞が生まれないため二次的に外顆粒層の細胞が増殖できずに失われるのだろう,と考えられた.
下オリーブ核と橋核に関しても同様な現象が観察された.それぞれ出生後2日目,5日目までは正常に発生してくるのだが,その後の2~3日の間に忽然と消えるのである.実はこの二つの神経核の神経細胞には共通点がある.前者はプルキンエ細胞へ,後者は顆粒細胞へと,いずれも小脳皮質の神経細胞へとその軸索を投射している.セレベレスでは小脳皮質が完全に失われるので,これらの神経核は投射先を失うことによって二次的に脱落するのだろうと考えられた.
さらにこの謎を解きすすめるためには,セレベレスで破壊されている遺伝子,すなわちセレベレスの原因遺伝子を見つけなくてはならなかった.まず遺伝学的交配によって,原因遺伝子の存在する可能性のあるゲノム領域を450万塩基の範囲まで狭めた.トランスジェニックマウス作製の過程では,しばしばゲノムの欠失を伴うことがある.そこでセレベレスゲノムを調べてみたところ,その450万塩基の中に31万3千塩基のゲノム欠失領域が存在することがわかった.次に,当時セレラ社が世界で初めて作成した全ゲノムデータベースが利用可能になったのでそれを参照したところ,そのゲノム欠失領域から少し離れたところに,Ptf1a(膵臓転写因子1a)という遺伝子が見つかった.この遺伝子は,DNAに結合して遺伝子発現を調節する転写因子PTF1Aをコードしているが,その名のとおり膵臓の発生に関わることが知られていた3, 4).Ptf1aのノックアウト(KO)マウスでは,膵臓の形成が大きく損なわれ,また出生後しばらくして死んでしまう.しかし,セレベレスはずっと生きているし,解剖してみたところ膵臓もちゃんとある.
(うーん,やはりこの遺伝子はセレベレスの原因遺伝子とは違うのだろうか?)
実は幸運にも,Ptf1a遺伝子のKOマウスが同じ京都大学医学部の動物施設に飼育されていた4).当時,京大病院外科・講師であった川口義弥先生(現・京大CiRA教授)が米国留学中に作ったそのマウスを,帰国する際に一緒に連れて来ていたのだ.これ幸いと,川口先生から出生直後の個体をいただいて調べたところ,予想どおりセレベレスと同様な小脳異常がみられた.この時点でようやく「この遺伝子があたりだ!」という手応えを感じた.2004年7月中旬のことである.セレベレスの研究を始めてから4年近くが経過していた.その後,マウスの交配によって,セレベレスとPtf1a KOのダブルヘテロ変異体を作出したところ,やはり同様な小脳異常が観察された.このことから,セレベレスの原因遺伝子がPtf1aであると確定した.本来は,この遺伝子にセレベレス(cerebelless)と命名したかったのだが,既知の遺伝子(Ptf1a)であったために,残念ながらそれは実現しなかった.
実は,セレベレスではPtf1aの小脳における発現は失われるものの,膵臓での発現は維持されたままであった.すなわち,セレベレスではPtf1aの小脳での発現に必要なゲノム領域は失われているが(31万3千塩基のゲノム欠失領域に含まれている),膵臓での発現に必要な部分は保存されているということである.結果として膵臓は正常に発生するため,成体まで生き残るのであろう.こんな都合のよい突然変異体が生み出されたとは,何か「神の手」のようなものの存在を感じてしまった.実際に,セレベレスは,小脳皮質を完全に失いながらも大人まで成長する世界で唯一の変異マウスなのである.
その後,遺伝子組織化学(in situハイブリダイゼーション)によって,Ptf1aが小脳原基の神経上皮細胞(ラディアルグリア)層の一部(図2参照,腹側の脳室帯と呼ばれる部分)で発現していることがわかった.逆にいえば,セレベレスにおいてはこの発現がなくなったために,小脳脳室帯からプルキンエ細胞が生み出されなくなる,ということである.ここまでが2004年7月末の時点でわかっていた.
(ということは,この遺伝子は小脳脳室帯でプルキンエ細胞の誕生をつかさどっているのであろうか?)
どうも釈然としなかった.それだけで,「小脳皮質がまったくない」という表現型を説明できるのだろうか? よく考えてみると,小脳にはさまざまな種類の神経細胞があるが,これを大きくカテゴライズすれば興奮性神経細胞と抑制性神経細胞とに分けられる.「プルキンエ細胞は抑制性神経細胞であるが,もしかしたらセレベレスではほかの抑制性神経細胞にも影響があるのではないか?」そう考えて,小脳の抑制性神経細胞の神経伝達物質であるGABAで免疫染色したところ,予想どおりセレベレスではプルキンエ細胞を含む抑制性神経細胞がまったく生まれてこないことがわかった(図1E, F).しかし,興奮性神経細胞(顆粒細胞および小脳核興奮性神経細胞)はちゃんと生まれてくる.さらに,川口先生が作ったKOマウス4)は,Ptf1aが本来発現する細胞とその子孫細胞を標識するための遺伝学的仕掛け(Ptf1a遺伝子座へのCreノックイン)が施してあるスグレモノであった.そこでそれを活用し,小脳におけるすべての種類の抑制性神経細胞は小脳脳室帯のPtf1aを発現する神経上皮細胞から生まれ,逆に興奮性神経細胞はどこかのPtf1aを発現しない神経上皮細胞に由来することがわかった(図2).
次に,胎仔期の背側大脳皮質の神経上皮細胞,すなわち「興奮性神経細胞しか生み出さないはずの細胞」にPtf1a遺伝子を異所性に導入してみた.子宮内電気穿孔法という方法で胎生14.5日目のマウス胚に遺伝子導入しその5日後に調べたところ,生み出された神経細胞が抑制性神経細胞の神経伝達物質であるGABAをたくさん含んでいた.さらにその神経細胞は,抑制性神経細胞特有の細胞移動様式や細胞形態を示すことも観察された.どうやらPtf1a遺伝子は,ただ単に神経伝達物質の合成系に関与するという単純なものではなくて,細胞形態や移動様式も含めた抑制性神経細胞の総合的な形質を付与する「運命決定因子」であることがわかってきたのである.
最終的に,この結果をまとめた論文,すなわちセレベレスの表現型解析と小脳抑制性神経細胞の運命決定遺伝子Ptf1aについての論文は,2005年7月に出版されることになった1).この研究は,セレベレスマウスと出会うという偶然からスタートした研究だったので,類似な研究をしている研究者が世界にいるだろうとは想像していなかった.しかし,驚いたことに密接に関連する論文がその2か月半後に2報も同じジャーナルに掲載された.その論文の筆者らは,菱脳唇でbHLH型転写因子をコードするAtoh1が発現することを利用してCre-LoxPシステムを用いた遺伝学的細胞系譜追跡実験を行い,従来報告されていた顆粒細胞だけではなくて,(おそらくは興奮性の)小脳核神経細胞も菱脳唇の神経上皮由来であることを示した5, 6)(図2).彼らは,顆粒細胞に加えて,その小脳核神経細胞が,Atoh1 KOマウスでは生まれてこないことも示している.実は,Ptf1a遺伝子がコードするタンパク質も,Atoh1と同様にbHLH型の転写因子である.
以上から,小脳全体において,「グルタミン酸作動性の興奮性神経細胞はすべて菱脳唇由来であり,GABA作動性の抑制性神経細胞はすべて脳室帯由来である」というように単純化して考えることができることになった.実際に,小脳皮質の神経細胞としては比較的マイナーであまり研究がなされてこなかったグルタミン酸作動性の単極性刷毛細胞も,菱脳唇由来であることが,その後報告された7).これまで小脳の神経細胞の個性決定機構はほとんど明らかにされていなかったが,筆者および米国の二つの研究室の論文をきっかけにして,小脳をモデル系とした各神経細胞種への運命決定の研究は大きく展開していくこととなる.
5. 小脳をモデル系とした個性の異なる各種神経細胞を生み分ける仕組みの研究
筆者は,上述の研究を元にして,小脳発生における新たなモデル「bHLH型転写因子による小脳神経上皮の領域化モデル」を提唱した(図2)8).これは,「小脳における2か所の神経上皮領域,つまり脳室帯と菱脳唇の神経上皮細胞が,それぞれ異なるbHLH型転写因子をコードするPtf1aとAtoh1遺伝子によってその場所に固有の形質(アイデンティティ)を与えられ,その結果としてそれぞれ抑制性および興奮性神経細胞を生み出す」というモデルである.もっとも,小脳の抑制性および興奮性神経細胞には,さらに細分化された種類の細胞があるため,このモデルだけでは,小脳におけるさまざまな種類の神経細胞を生み分ける仕組みは完全には説明できない.しかし筆者の論文が掲載された当時,それらの各種神経細胞が生み出される発生時期はそれぞれに異なることが知られていた.脳室帯からは,最初にプルキンエ細胞が,次にゴルジ細胞,最後にバスケット細胞・星状細胞が生み出される(直接生み出されるものと,間接的に生み出されるものがあることがその後わかったが,ここではそこまで踏み込まない).菱脳唇からは,最初は興奮性小脳核神経細胞が,次に顆粒細胞,その後,単極性刷毛細胞が生み出される.以上から筆者らは,生み出される神経細胞の種類は,神経上皮細胞が位置する脳内の「場所(空間)」と「発生時期(時間)」によって規定される「固有の形質」,すなわち神経上皮(幹)細胞の「時間および空間のアイデンティティ」によって規定されるのであろうと考えた.ただ,空間アイデンティティはPtf1aやAtoh1などの遺伝子の発現によってもたらされると推定できたが,当時,時間アイデンティティの分子的実体についてはほとんどわかっていなかった.
2007年暮れになると,筆者は京都大学医学研究科(鍋島陽一研究室)から現在の所属へ異動し,PIとして新たな研究室を開くことになった.幸いにしてほぼ同時期に,「神経上皮(幹)細胞の時空間細胞アイデンティティ」という研究課題で科学研究費補助金「若手研究S」(残念ながら,現在ではこの研究費制度は廃止されてしまった)に採択されたので,研究室のセットアップをしつつこの研究テーマに取り組むことができた.京都大学で私の研究チームの大学院生だった山田真弓さん(現・京都大学・特定准教授)と藤山知之君(現・筑波大学・助教)が一緒に東京へ移住し,研究室の立ち上げを手伝ってくれた.
山田さんは,Ptf1a遺伝子座にAtoh1 cDNAを,Atoh1遺伝子座にPtf1a cDNAを導入した相互ノックインマウスを作出してくれた9).このマウスでは,Ptf1aおよびAtoh1を発現する神経上皮領域が逆になる.その結果,予想どおり抑制性神経細胞が菱脳唇から,興奮性神経細胞が脳室帯から生み出されることが観察された.さらに,このマウスを使って各種神経細胞の生まれる発生時期を検討したところ,たとえ異所性にそれぞれのbHLH型転写因子が発現されても,特定の時期に生み出される神経細胞の種類は,正常発生のものと同じであることが明らかになった.つまり,各種神経細胞が生み出される順番は変わらなかったのである.以上から,たとえ菱脳唇と脳室帯という異なる空間アイデンティティを持った神経上皮細胞であっても,共通の時間アイデンティティを持っていることが示唆された9).
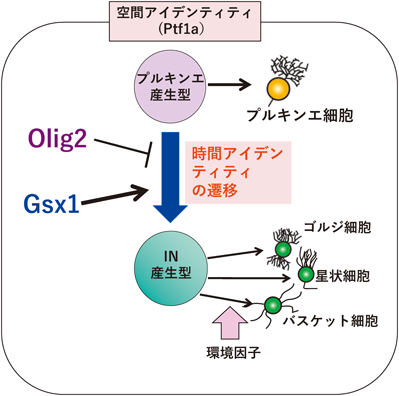
小脳抑制性神経細胞は,大きく2種類に分けられる.長い軸索で遠方へと投射するプルキンエ細胞と,それ以外の局所回路で働く介在神経細胞(インターニューロン)である.後者は,小脳核抑制性神経細胞,ゴルジ細胞,バスケット細胞,星状細胞などを含む.当時,連携大学院の早稲田大学の大学院生だった瀬戸裕介君は,小脳原基のPtf1aを発現する脳室帯の中に,さらにOlig2およびGsx1という転写因子をコードする遺伝子を発現するサブドメインがあることを見いだした10).さらに,それぞれの遺伝子座に緑色蛍光タンパク質(GFP)をノックインしたマウスを用いて,それぞれの遺伝子を発現する細胞から生み出される細胞を調べる実験(リニエージ解析)を行ったところ,Olig2を発現するものが「プルキンエ細胞」を生み出す神経上皮細胞(プルキンエ細胞産生型)であり,Gsx1を発現するものが「インターニューロン」を生み出す神経上皮細胞(インターニューロン産生型)であるとわかった(図3).さらに,小脳発生の初期段階には脳室帯の大部分の神経上皮細胞が「プルキンエ細胞産生型」であるのに,その後,細胞分裂を繰り返す時間的経過に伴って次第に「インターニューロン産生型」に遷移するということがわかった.これは言葉を変えていえば,神経上皮細胞の「時間アイデンティティ」が,「プルキンエ細胞産生型」から「インターニューロン産生型」へと遷移したということである.また,さまざまな遺伝子改変マウスの解析から,この神経上皮細胞の時間アイデンティティの遷移がOlig2によって減速され,Gsx1によって加速されるということも明らかになった.このように,神経上皮細胞の時空間アイデンティティの制御によって,興奮性・抑制性,プルキンエ細胞・インターニューロンの生み分けがなされているということが,小脳をモデル系として明らかになってきたのである.
さらに,インターニューロン産生型の神経上皮細胞から,いかにしてゴルジ細胞やバスケット細胞・星状細胞などが生み分けられるかについては,イタリア・トリノ大学のRossiらのグループが,細胞移植実験などによってその細胞の周囲の環境要因が重要であることを示唆している11–13).つまり,神経上皮細胞の空間・時間・環境の三要因によって,異なる種類の神経細胞種が生み分けられるというモデルが,小脳の解析から明らかになってきたといえる(図2, 3).筆者は,この「空間×時間×環境」の原則は,小脳だけでなくほかの脳領域にも適用できる普遍的なものなのではないか,と考えている.
6. 小脳の空間アイデンティティ仮説はほかの脳領域に適用できるか?
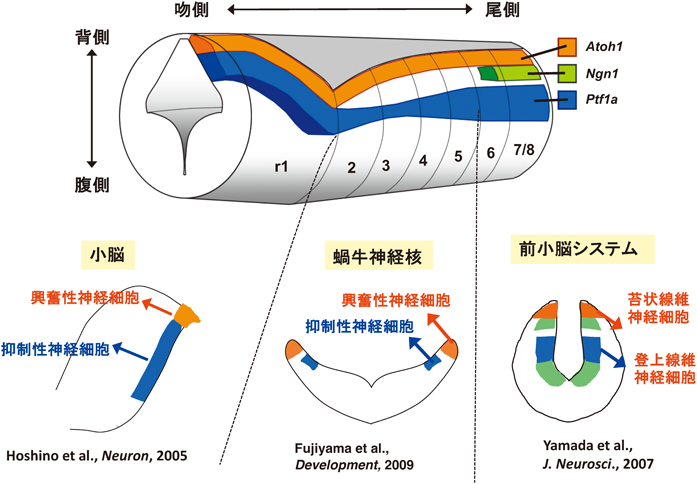
後脳は前後軸に沿って八つのロンボメア(rhombomere, r1~r8)からなる構造をなしている.筆者を含むいくつかの研究グループの研究により,Atoh1およびPtf1a遺伝子は後脳を前後に貫くように発現し,それぞれ背腹軸に沿った異なる神経上皮ドメインを形成することが明らかになっていた(図4).ちなみに,r1の背側からは小脳が生み出される.京大から一緒に東京へと異動してきた大学院生の山田さんは尾側後脳(r6~8)では,Ptf1aを発現する神経上皮ドメイン(Ptf1aドメイン)から登上線維神経細胞が生み出され,その発生にはPtf1aが必要であるということを明らかにした14).実はその少し前に,Atoh1神経上皮ドメインからは苔状線維神経細胞が生み出されることが他グループから報告されていた6).山田さんと同じく京大から異動してきた大学院生の藤山君は,中央部後脳(r2~5)では,Ptf1a神経上皮ドメインから蝸牛神経核のすべての種類の抑制性神経細胞が,Atoh1神経上皮ドメインからは蝸牛神経核のすべての種類の興奮性神経細胞が,それぞれ生み出されるということ,そしてその発生を両者の転写因子がつかさどっているということを明らかにしてくれた15).
以上の研究から,小脳原基(r1)だけでなく,その他の神経上皮細胞領域(後脳のr2~r8)においても,異なるbHLH型転写因子をコードするPtf1aおよびAtoh1遺伝子によって,神経上皮細胞の空間アイデンティティが決定されていることが示唆されたといえる.また,以上の研究によって,後脳背側から生まれる神経細胞は,そのロンボメアによって規定される前後軸の位置情報(おそらくはHox遺伝子群などが関係するのだろう)と,bHLH型転写因子によって規定される背腹軸の位置情報(Ptf1a, Atoh1など)によって生み分けられる,というモデルが提唱されることになった(図4)16).筆者は,前述の空間,時間,および環境情報の組合わせによって,多種多様な神経細胞がさらに生み分けられるのだろう,と考えている.
7. Ptf1a遺伝子は脳の性分化の初期段階に関与する
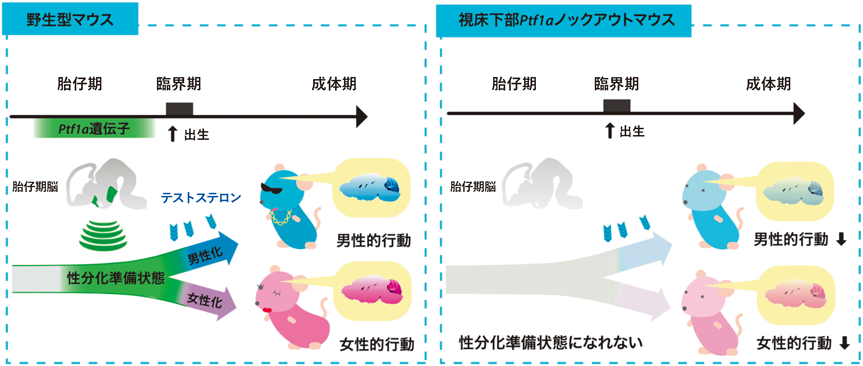
蝸牛神経核の研究に従事してくれた藤山君は,その後,筑波大学IIISの柳沢正史先生の研究室へ異動し,助教として睡眠の研究をすることになった.しかし,空いた時間にPtf1a遺伝子の研究も続けてくれて,この遺伝子がマウスの脳の性分化に働くことを見いだしてくれた17).哺乳類の脳は,「臨界期」と呼ばれる時期にテストステロン刺激を受けるとオス化し,その刺激を受けないとメス化することが知られている.しかし「臨界期」以前の脳の性分化機構についてはよくわかっていなかった.藤山君は,Ptf1a遺伝子が,「臨界期」よりはるかに前の胎仔期において,視床下部の細胞を生み出す神経上皮領域で発現することを見いだした.またその細胞から生まれた細胞は視床下部の多くの神経核のさまざまな興奮性神経細胞および抑制性神経細胞となることも明らかにした(視床下部神経細胞の20%程度).さらに,その領域でPtf1a遺伝子を破壊したコンディショナルKO(cKO)マウスを作製したところ,その脳は「臨界期」にテストステロン刺激を受けてもオス化できず,またテストステロン刺激を受けなくてもメス化しないことが観察された.このことから,(1)脳の性分化(オス化またはメス化)のためには,「臨界期」以前に「性分化準備状態」になる必要があること,そして(2)胎仔期の視床下部Ptf1aが脳を「性分化準備状態」へと導き,その後の「臨界期」でのテストステロン刺激・非刺激によってオス化脳・メス化脳へと性分化させるということが明らかとなった(図5)17).これまでにも脳の性分化に関わる遺伝子はいくつも報告されているが,Ptf1aはそれらの中で最も早く働く遺伝子の一つであり,藤山君の研究は脳の性分化の初期段階を明らかにしたといえる.それにしてもPtf1a遺伝子の持つ多様な機能には,ただただ感嘆するばかりである.ただPtf1aが視床下部のどの神経細胞への分化をどのように助けることによって,脳の性分化に寄与しているのかについては,まだ明らかになっていない.
さて,Ptf1aが小脳の抑制性神経細胞の運命決定因子であることはわかったが,その作用機序を知るために,筆者らはその下流で働く遺伝子を探索することにした.当時はまだRNAマイクロアレイという手法が主流だったので,その方法を用いて,野生型とPtf1a KOマウスの小脳原基において遺伝子発現が変動する遺伝子の探索を行い,結果的に20数種類もの下流候補遺伝子を得ることができた.それらの中には,抑制性の神経伝達物質の合成に関わる遺伝子などもあったが,ひねくれ者の筆者はそうした「ストーリーがみえる」わかりやすい遺伝子の解析を行うことに抵抗があった.そういう研究は,確かに結果を出しやすいのだが,「想定内」の結果しか得られずに,最終的に大きな研究成果となりにくいと考えたからである.(こうした考え方は,筆者の元ボスの鍋島陽一先生の影響を受けているかもしれない.)そこで,当時,筆者の研究室に来た堀啓研究員(その後,室長へと昇進)と相談した結果,Autism Susceptibility Candidate 2(マウス表記はAuts2,ヒトではAUTS2)という風変わりな名前の遺伝子の解析をすることにした.ただ,Ptf1aの下流遺伝子候補であることをきっかけとして始めた研究ではあったが,大脳皮質発達における機能解析の研究が先行し,Auts2の小脳発生における役割解明は結果的に後回しになってしまった.
この遺伝子は,2002年に自閉スペクトラム症患者で変異を持つ遺伝子として同定されていた18).その後,てんかん,統合失調症,注意欠陥多動性障害,知的障害,言語障害,薬物依存など,さまざまな精神神経疾患で,DNA欠失,重複,逆位,転座などのAUTS2遺伝子変異が報告された19).また,小頭症や顔貌異常などのさまざまな症状との関連も指摘されているため,この遺伝子の変異による一連の徴候は「AUTS2症候群」と呼ばれている20, 21).この遺伝子に変異を持つほとんどのケースはde novo発症であり,ヘテロ接合体発症である.
9. AUTS2タンパク質の細胞内における分子機構
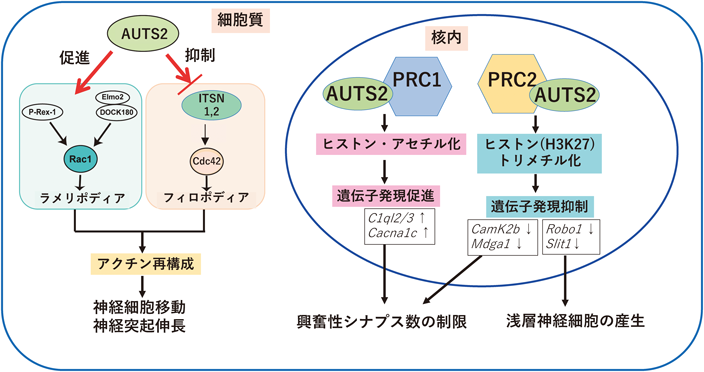
研究開始当時,世界の多くの研究室はAUTS2が核にしか局在しないと考えていたが,堀室長はAUTS2が細胞質にも局在することを見いだした.それまでに筆者は,京大・鍋島研の私の研究グループの大学院生だった松尾直毅君(現・九州大学・教授),川内健史君(現・京都大学・特定教授),吉澤匡人君(現・ハワイ大学・准教授)らとともに定分子量Gタンパク質による細胞骨格制御の研究も行っていたので22–24),その経験を活かしてAUTS2にもそのような機能がないかどうか,他の実験のついでに調べてみた.すると,AUTS2タンパク質がP-Rex1やElmo2/DOCK180複合体などのGタンパク質活性化因子(グアニンヌクレオチド交換因子,GEFと略す)と結合することでRhoファミリー低分子量Gタンパク質Rac1を活性化し,細胞内にラメリポディアという網目状アクチン構造を誘導すること,またその一方で,このタンパク質がIntersectin-1およびIntersectin-2という別のGEFと結合することでRhoファミリー低分子量Gタンパク質Cdc42の活性を抑制し,フィロポディアという糸状のアクチン構造の形成を阻害することが明らかになった(図6).この論文は,2014年12月18日に出版された25).しかし,セレベレス論文のときと同様に,類似の研究はほぼ同時に世界のどこかで行われているものである.筆者らの論文とまったく同じ2014年12月18日,アメリカの研究グループのGaoらは,AUTS2タンパク質が細胞核において,ポリコーム複合体1(PRC1)と相互作用することを発表した26).本来PRC1はヒストンのユビキチン化を介してさまざまな遺伝子の発現抑制に働くのだが,AUTS2がPRC1と相互作用すると,PRC1がヒストンのアセチル化を促し,遺伝子発現の活性化に働く(図6).
2014年に出たこれら二つの論文が,結果的にAUTS2の哺乳類の細胞内における分子機能を,初めて実質的に明らかにしたものとなった.2021年に,Monderer-Rothkoffらは,AUTS2が遺伝子の転写活性化だけでなく転写抑制にも働くことを示したが27),その分子メカニズムについては明らかになっていなかった.しかし筆者らは,2025年にAUTS2がポリコーム複合体2(PRC2)と共役して,ヒストンH3の27番目のリシン残基のトリメチル化を促進することで,遺伝子発現抑制に働くことを明らかにした(図6)28).
AUTS2遺伝子変異によるAUTS2症候群では,脳神経発達期から上述のようなさまざまな精神神経障害(自閉スペクトラム症,知的障害,統合失調症,てんかん,等)が引き起こされる.形態学的にも,小頭症,脳梁縮小,小脳縮小などが観察されている.しかし我々の研究開始時点では,ノックダウンするとゼブラフィッシュの脳が小さくなることが報告されていたくらいで,ヒトを含む哺乳類の神経発生における役割はほとんど明らかになっていなかった.ところが,その後の筆者らの研究により,Auts2遺伝子が上述の神経発生におけるすべての段階,すなわち(1)神経細胞の産生,(2)神経細胞の移動,(3)神経突起の伸長と経路探索,(4)シナプスの形成・刈り込み,に関わっていることが明らかになった.
まず堀室長は,Auts2の機能について,マウスを用いた遺伝子ノックアウト(KO)やノックダウン(KD)実験を行うこととした.筆者の星野は京大・鍋島研時代から,前述の川内君,吉澤君と一緒に神経細胞移動の研究を精力的に行っていたため23, 24, 29, 30),まずはその手法を用いて神経細胞移動について解析した.すると,Auts2 KO,あるいはKDマウスの大脳皮質の神経細胞移動が大幅に遅延していることを見いだした.神経細胞移動の異常は,知的障害やてんかんなどとの関連が指摘されており,これはAUTS2症候群でみられる精神・神経障害の一部を説明できると考えられた.また,Auts2 KOマウスでは,大脳皮質2/3層神経細胞から脳梁を超えた対側半球へと投射される軸索伸長が大きく妨げられることも観察された.AUTS2症候群では,脳梁の浅薄化が報告されているが,これに対応しているのかもしれない.神経細胞移動および神経軸索伸長の障害は,いずれもRac1の遺伝子導入によってレスキューされたことから,AUTS2によるRac1の活性化が神経細胞移動や神経軸索伸長に必要とされることが明らかになった25).
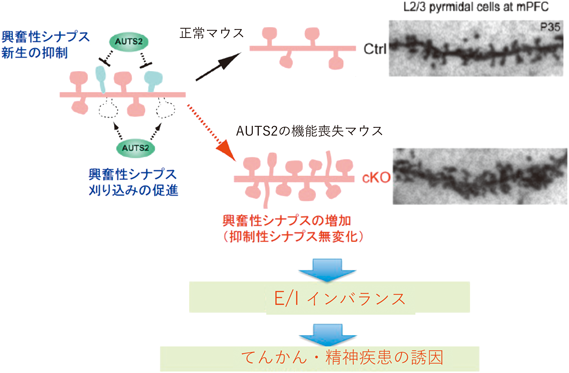
また堀室長は,AUTS2が大脳皮質や海馬において,興奮性シナプスの数を制限することを見いだした31).AUTS2は,興奮性シナプスの新規形成を抑制するとともに,刈り込みを促進することで,結果的に興奮性シナプスの数が増えすぎないように調節する.一方で,抑制性シナプスの数には影響しない.実際に,Auts2遺伝子のKOマウスでは,脳の各部位の神経細胞で興奮性シナプスが増加する(一方で抑制性シナプス数には変化がない).これにより,神経細胞における興奮性シナプス入力は増加するが,抑制性シナプス入力は変化せず,結果として脳内の神経細胞の活動性が高まることが観察された(図7).この興奮性/抑制性の不均衡(E/Iインバランス)はてんかんのみならず,さまざまな精神疾患や脳機能障害の原因・誘引となりうることが報告されてきている.なお,細胞核局在シグナルと細胞質局在シグナルを付与したAUTS2タンパク質を使った実験から,この興奮性シナプスの数を制限する機能を持つのは核内AUTS2タンパク質であることが判明した.このことから現在我々は,AUTS2が下流遺伝子の発現量を変化させることでシナプス数を制限するのではないか,と考えている.ちなみに,Auts2遺伝子を発生途上ではなく脳が完成してから時期特異的にノックアウトしても,興奮性シナプスの増加が認められるため,AUTS2はシナプスの発生だけでなく成体におけるシナプスの恒常性維持にも働いていることが示された.
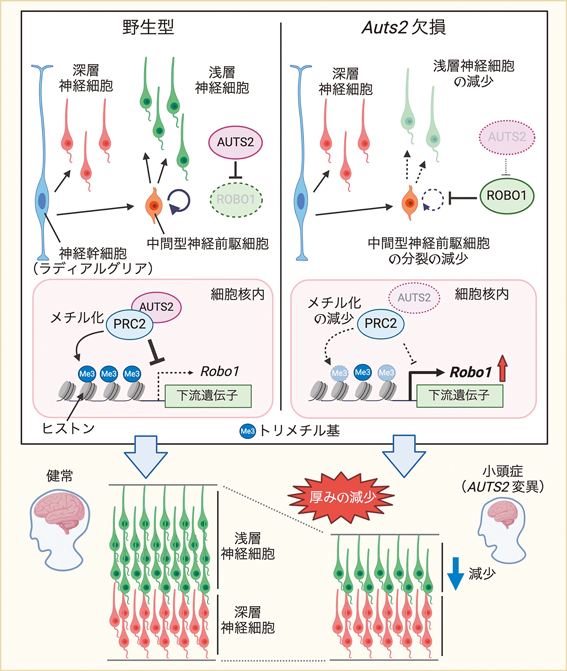
筆者の研究室の嶋岡可純研究員は,Auts2の大脳皮質特異的KO(cKO)マウスにおいて,大脳皮質の浅層神経細胞が減少し,脳が薄くなることを観察した28).一方で,深層神経細胞の数には変化がなかった.哺乳類においては,脳発生の初期ではラディアルグリアの分裂によって深層神経細胞が直接生み出されるのに対して,脳発生中期~後期では,ラディアルグリアが中間神経前駆細胞を生み出し,その後中間神経前駆細胞が1回~数回分裂することによって浅層神経細胞が生み出される場合が多い.Auts2 cKOでは,中間神経前駆細胞の分裂回数が減少することで,浅層神経細胞の数が減少する.嶋岡さんは,この中間神経前駆細胞の細胞核において,AUTS2タンパク質がPRC2と共役していろいろな遺伝子(Robo1, Slit1など)の発現を抑制することで,その細胞分裂を促進し,結果的に浅層神経細胞の数を増やす働きを持つことを明らかにしてくれた.この機能が失われると,大脳皮質浅層神経細胞が減少し,大脳皮質が薄くなってしまう.AUTS2症候群では,かなりの高確率(65%)で小頭症を併発するのだが,その背後にこうした病態メカニズムがあると考えられた(図8)28).
なお,念願のAuts2の小脳発生における役割については,東京医科歯科大学(現在の東京科学大学)博士課程の大学院生だった山城邦比古君(現・米国テキサス大学・博士研究員)が研究し,AUTS2がプルキンエ細胞の成熟とシナプス形成に関わることを明らかにしてくれた32).彼は,Auts2の小脳特異的cKOマウスでは小脳が縮小することも観察した.AUTS2症候群では,小脳がかなり小さくなることが報告されているが,このcKOマウスの表現型はそのよい疾患モデルとなると考えられる.
また,AUTS2遺伝子は,霊長類から人類が分岐した後で,さらには我々ホモ・サピエンスがネアンデルタール人と共通の祖先から分岐した後で,加速的に変化したゲノム領域であることが報告されている33).この遺伝子が特に前頭前皮質などの高次脳機能をつかさどる脳領域でより強く発現することから,AUTS2がヒトの脳の進化に大きな役割を果たしたのではないかとも考えられている.
脳神経系の発生は多段階かつ複雑であり,おそらく関わる遺伝子は全遺伝子の2~4割にも及ぶであろう.それに比べれば,筆者が明らかにしたことは,脳神経系発生の分子機構をすべて明らかにするという神経発生生物学の究極の目標に比べれば,砂漠の中の一粒の砂のようなものである.しかし,偶然の突然変異マウスとの出会い,遺伝子との出会い,人との出会いがあってこそ,そうした一粒の砂の研究を達成することができた.そしてその研究過程がとても楽しかったことを思えば,やはり研究活動はすばらしいものだと思う.ただ,研究は一人ではできない.私を指導してくださった鍋島陽一先生,浜千尋先生をはじめ,これまで出会ったすべての共同研究者に感謝したい.神戸市のKAN研究所(当時)の尾野雄一先生には,特に小脳の時間アイデンティティの研究において,重要な各種ノックインマウスや特異抗体をご提供いただき,研究のアイデアについても大いに助けていただいた.ただ筆者の研究はもうしばらく続くので,ここで回想にふけらず,研究活動を仲間と続けていきたい.最近は,マルチオミックス解析などのバイオインフォーマティクス解析に研究室の1/3~1/2の戦力を割いて,新たな神経発生と精神神経疾患の研究に取り組んでいる.
引用文献References
1) Hoshino, M., Nakamura, S., Mori, K., Kawauchi, T., Terao, M., Nishimura, Y.V., Fukuda, A., Fuse, T., Matsuo, N., Sone, M., et al. (2005) Ptf1a, a bHLH transcriptional gene, defines GABAergic neuronal fates in cerebellum. Neuron, 47, 201–213.
2) Wechsler-Reya, R.J. & Scott, M.P. (1999) Control of neuronal precursor proliferation in the cerebellum by Sonic Hedgehog. Neuron, 22, 103–114.
3) Krapp, A., Knöfler, M., Ledermann, B., Bürki, K., Berney, C., Zoerkler, N., Hagenbüchle, O., & Wellauer, P.K. (1998) The bHLH protein PTF1-p48 is essential for the formation of the exocrine and the correct spatial organization of the endocrine pancreas. Genes Dev., 12, 3752–3763.
4) Kawaguchi, Y., Cooper, B., Gannon, M., Ray, M., MacDonald, R.J., & Wright, C.V. (2002) The role of the transcriptional regulator Ptf1a in converting intestinal to pancreatic progenitors. Nat. Genet., 32, 128–134.
5) Machold, R. & Fishell, G. (2005) Math1 is expressed in temporally discrete pools of cerebellar rhombic-lip neural progenitors. Neuron, 48, 17–24.
6) Wang, V.Y., Rose, M.F., & Zoghbi, H.Y. (2005) Math1 expression redefines the rhombic lip derivatives and reveals novel lineages within the brainstem and cerebellum. Neuron, 48, 31–43.
7) Englund, C., Kowalczyk, T., Daza, R.A., Dagan, A., Lau, C., Rose, M.F., & Hevner, R.F. (2006) Unipolar brush cells of the cerebellum are produced in the rhombic lip and migrate through developing white matter. J. Neurosci., 26, 9184–9195.
8) Hoshino, M. (2006) Molecular machinery governing GABAergic neuron specification in the cerebellum. Cerebellum, 5, 193–198.
9) Yamada, M., Seto, Y., Taya, S., Owa, T., Inoue, Y.U., Inoue, T., Kawaguchi, Y., Nabeshima, Y., & Hoshino, M. (2014) Specification of spatial identities of cerebellar neuron progenitors by ptf1a and atoh1 for proper production of GABAergic and glutamatergic neurons. J. Neurosci., 34, 4786–4800.
10) Seto, Y., Nakatani, T., Masuyama, N., Taya, S., Kumai, M., Minaki, Y., Hamaguchi, A., Inoue, Y.U., Inoue, T., Miyashita, S., et al. (2014) Temporal identity transition from Purkinje cell progenitors to GABAergic interneuron progenitors in the cerebellum. Nat. Commun., 5, 3337.
11) Leto, K., Carletti, B., Williams, I.M., Magrassi, L., & Rossi, F. (2006) Different types of cerebellar GABAergic interneurons originate from a common pool of multipotent progenitor cells. J. Neurosci., 26, 11682–11694.
12) Leto, K., Bartolini, A., Yanagawa, Y., Obata, K., Magrassi, L., Schilling, K., & Rossi, F. (2009) Laminar fate and phenotype specification of cerebellar GABAergic interneurons. J. Neurosci., 29, 7079–7091.
13) Rolando, C., Gribaudo, S., Yoshikawa, K., Leto, K., De Marchis, S., & Rossi, F. (2010) Extracerebellar progenitors grafted to the neurogenic milieu of the postnatal rat cerebellum adapt to the host environment but fail to acquire cerebellar identities. Eur. J. Neurosci., 31, 1340–1351.
14) Yamada, M., Terao, M., Terashima, T., Fujiyama, T., Kawaguchi, Y., Nabeshima, Y., & Hoshino, M. (2007) Origin of climbing fiber neurons and their developmental dependence on Ptf1a. J. Neurosci., 27, 10924–10934.
15) Fujiyama, T., Yamada, M., Terao, M., Terashima, T., Hioki, H., Inoue, Y.U., Inoue, T., Masuyama, N., Obata, K., Yanagawa, Y., et al. (2009) Inhibitory and excitatory subtypes of cochlear nucleus neurons are defined by distinct bHLH transcription factors, Ptf1a and Atoh1. Development, 136, 2049–2058.
16) Hoshino, M. (2012) Neuronal subtype specification in the cerebellum and dorsal hindbrain. Dev. Growth Differ., 54, 317–326.
17) Fujiyama, T., Miyashita, S., Tsuneoka, Y., Kanemaru, K., Kakizaki, M., Kanno, S., Ishikawa, Y., Yamashita, M., Owa, T., Nagaoka, M., et al. (2018) Forebrain Ptf1a is required for sexual differentiation of the brain. Cell Rep., 24, 79–94.
18) Sultana, R., Yu, C.E., Yu, J., Munson, J., Chen, D., Hua, W., Estes, A., Cortes, F., de la Barra, F., Yu, D., et al. (2002) Identification of a novel gene on chromosome 7q11.2 interrupted by a translocation breakpoint in a pair of autistic twins. Genomics, 80, 129–134.
19) Beunders, G., van de Kamp, J., Vasudevan, P., Morton, J., Smets, K., Kleefstra, T., de Munnik, S.A., Schuurs-Hoeijmakers, J., Ceulemans, B., Zollino, M., Hoffjan, S., et al. (2016) A detailed clinical analysis of 13 patients with AUTS2 syndrome further delineates the phenotypic spectrum and underscores the behavioural phenotype. J. Med. Genet., 53, 523–532.
20) Hori, K. & Hoshino, M. (2017) Neuronal migration and AUTS2 syndrome. Brain Sci., 7, 54.
21) Hori, K., Shimaoka, K., & Hoshino, M. (2021) AUTS2 Gene: Keys to understanding the pathogenesis of neurodevelopmental disorders. Cells, 11, 11.
22) Matsuo, N., Hoshino, M., Yoshizawa, M., & Nabeshima, Y. (2002) Characterization of STEF, a guanine nucleotide exchange factor for Rac1, required for neurite growth. J. Biol. Chem., 277, 2860–2868.
23) Kawauchi, T., Chihama, K., Nabeshima, Y., & Hoshino, M. (2003) The in vivo roles of STEF/Tiam1, Rac1 and JNK in cortical neuronal migration. EMBO J., 22, 4190–4201.
24) Yoshizawa, M., Kawauchi, T., Sone, M., Nishimura, Y.V., Terao, M., Chihama, K., Nabeshima, Y., & Hoshino, M. (2005) Involvement of a Rac activator, P-Rex1, in neurotrophin-derived signaling and neuronal migration. J. Neurosci., 25, 4406–4419.
25) Hori, K., Nagai, T., Shan, W., Sakamoto, A., Taya, S., Hashimoto, R., Hayashi, T., Abe, M., Yamazaki, M., Nakao, K., et al. (2014) Cytoskeletal regulation by AUTS2 in neuronal migration and neuritogenesis. Cell Rep., 9, 2166–2179.
26) Gao, Z., Lee, P., Stafford, J.M., von Schimmelmann, M., Schaefer, A., & Reinberg, D. (2014) An AUTS2-Polycomb complex activates gene expression in the CNS. Nature, 516, 349–354.
27) Monderer-Rothkoff, G., Tal, N., Risman, M., Shani, O., Nissim-Rafinia, M., Malki-Feldman, L., Medvedeva, V., Groszer, M., Meshorer, E., & Shifman, S. (2021) AUTS2 isoforms control neuronal differentiation. Mol. Psychiatry, 26, 666–681.
28) Shimaoka, K., Hori, K., Miyashita, S., Inoue, Y.U., Tabe, N.K.N., Sakamoto, A., Hasegawa, I., Nishitani, K., Yamashiro, K., Egusa, S.F., et al. (2025) The microcephaly-associated transcriptional regulator AUTS2 cooperates with Polycomb complex PRC2 to produce upper-layer neurons in mice. EMBO J., 44, 1354–1378.
29) Kawauchi, T., Chihama, K., Nabeshima, Y., & Hoshino, M. (2006) Cdk5 phosphorylates and stabilizes p27kip1 contributing to actin organization and cortical neuronal migration. Nat. Cell Biol., 8, 17–26.
30) Kawauchi, T., Sekine, K., Shikanai, M., Chihama, K., Tomita, K., Kubo, K., Nakajima, K., Nabeshima, Y., & Hoshino, M. (2010) Rab GTPases-dependent endocytic pathways regulate neuronal migration and maturation through N-cadherin trafficking. Neuron, 67, 588–602.
31) Hori, K., Yamashiro, K., Nagai, T., Shan, W., Egusa, S.F., Shimaoka, K., Kuniishi, H., Sekiguchi, M., Go, Y., Tatsumoto, S., et al. (2020) AUTS2 regulation of synapses for proper synaptic inputs and social communication. iScience, 23, 101183.
32) Yamashiro, K., Hori, K., Lai, E.S.K., Aoki, R., Shimaoka, K., Arimura, N., Egusa, S.F., Sakamoto, A., Abe, M., Sakimura, K., et al. (2020) AUTS2 governs cerebellar development, purkinje cell maturation, motor function and social communication. iScience, 23, 101820.
33) Green, R.E., Krause, J., Briggs, A.W., Maricic, T., Stenzel, U., Kircher, M., Patterson, N., Li, H., Zhai, W., Fritz, M.H., et al. (2010) A draft sequence of the Neandertal genome. Science, 328, 710–722.
著者紹介Author Profile
 星野 幹雄(ほしの みきお)
星野 幹雄(ほしの みきお)国立精神神経医療研究センター神経研究所病態生化学研究部 部長.博士(医学).
略歴1964年新潟県生まれ,89年新潟大学医学部卒業,93年同大学院博士課程修了,国立精神神経センター,スタンフォード大学医学部・博士研究員を経て,97年大阪大学助手,98年京都大学大学院医学研究科(鍋島陽一研究室)助手/助教.2007年より現職.
研究テーマと抱負研究テーマは,脳神経系発生の遺伝子プログラム解明と,その破綻による精神神経疾患の病態解明.最近のマイブームは手術脳・死後脳検体のXenium空間トランスクリプトーム解析.
ウェブサイトhttps://byosei-neuroscience-institute.ncnp.go.jp
趣味葡萄栽培,ワイン醸造,ワインテイスティング.鹿島アントラーズの試合観戦.