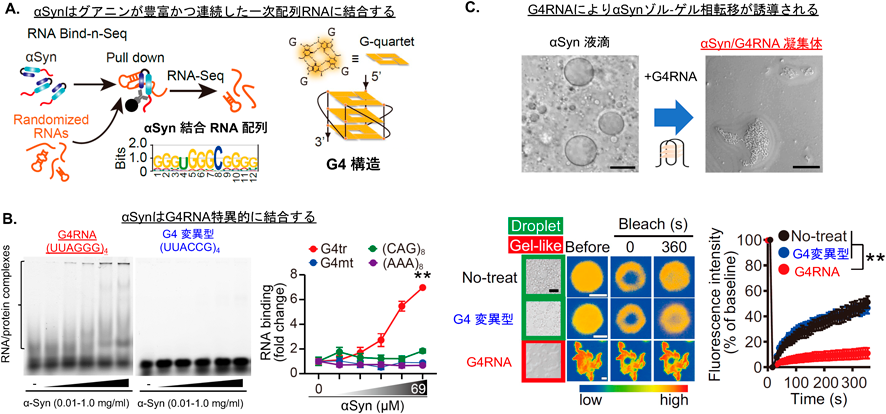
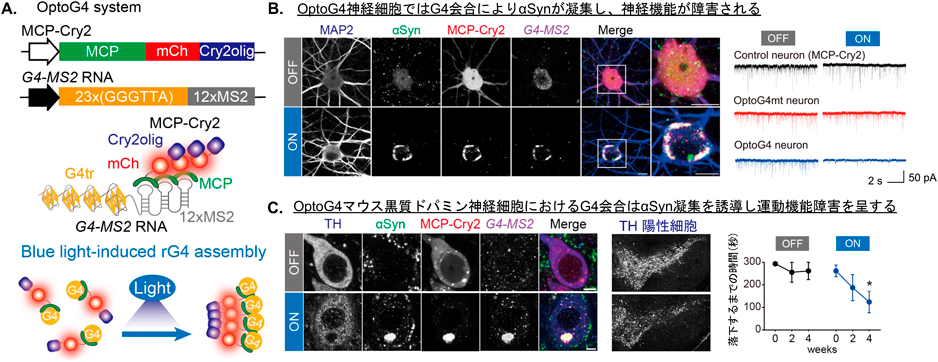
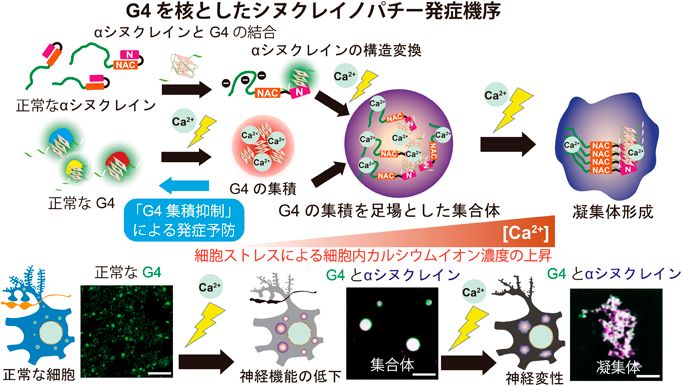
グアニン四重鎖を核としたαシヌクレイン凝集による神経変性機構The mechanism underlying neurodegeneration by αSynuclein aggregation initiated by G-quadruplex
熊本大学発生医学研究所ゲノム神経学分野Department of Genomic Neurology, Institute of Molecular Embryology and Genetics, Kumamoto University ◇ 〒860–0811 熊本市中央区本荘2–2–1 ◇ 2–2–1 Honjo, Chuo-ku, Kumamoto 860–0811, Japan