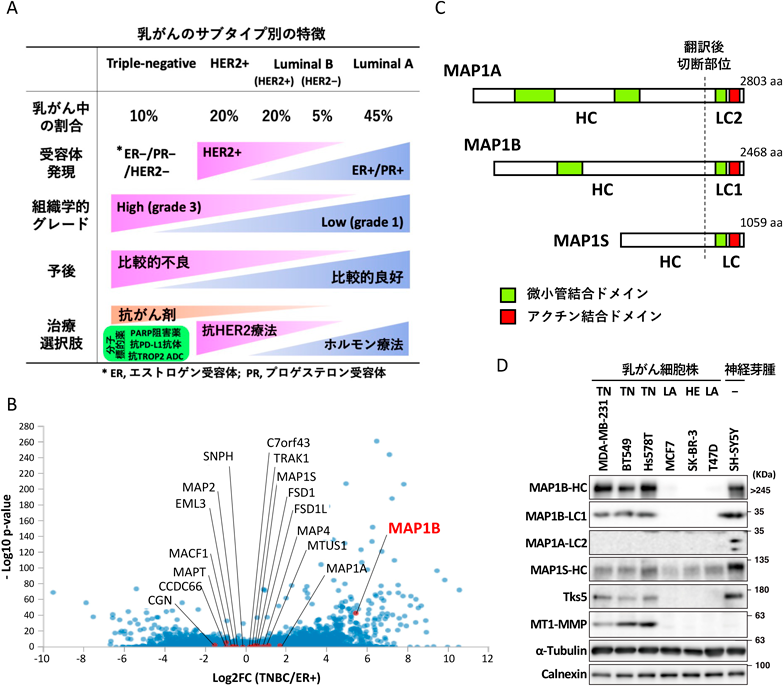
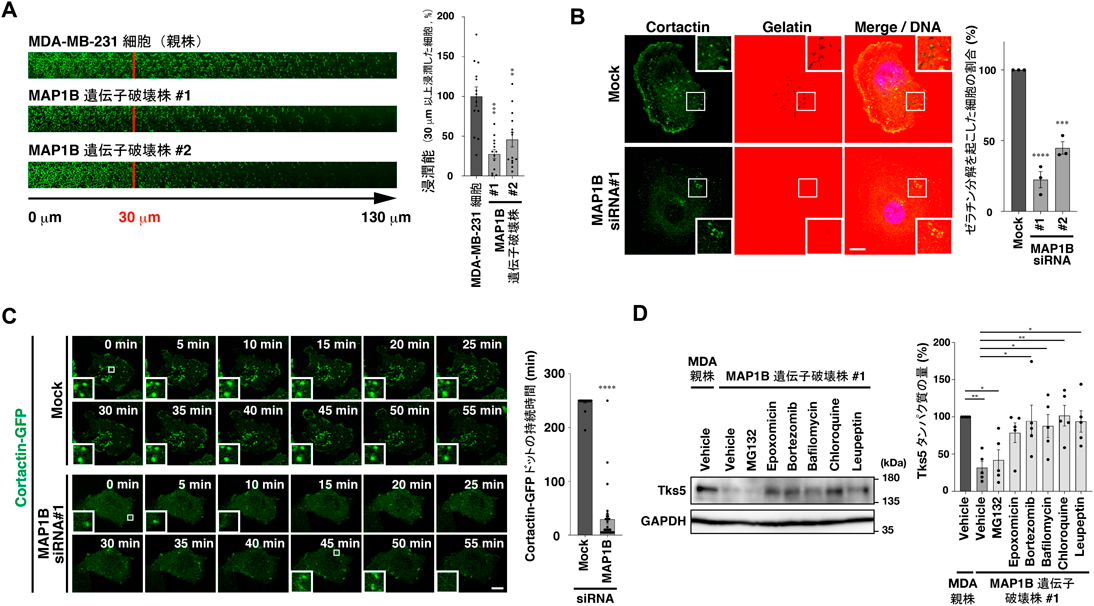
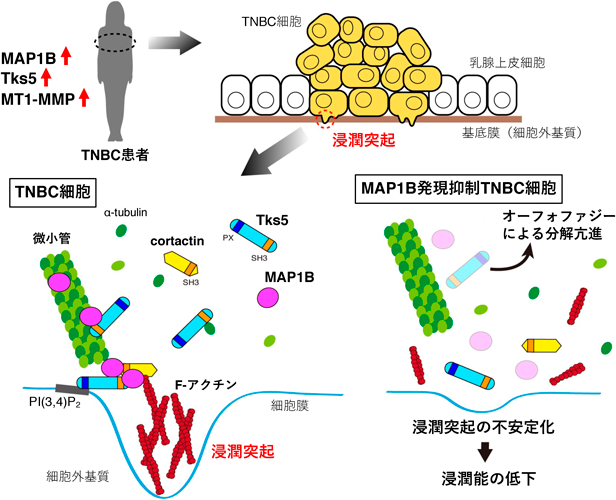
トリプルネガティブ乳がんの浸潤転移における微小管−アクチン結合タンパク質の機能Microtubule/Actin-binding protein MAP1B organizes invadopodia-driven invasion in triple-negative breast cancer cell
東京薬科大学生命科学部感染制御学研究室School of Life Sciences, Tokyo University of Pharmacy and Life Sciences ◇ 〒192–0392 東京都八王子市堀之内1432–1 ◇ 1432–1 Horinouchi, Hachioji, Tokyo 192–0392, Japan