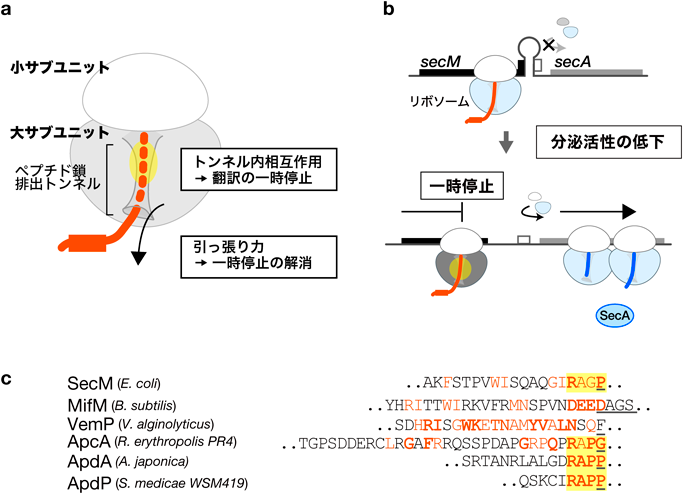
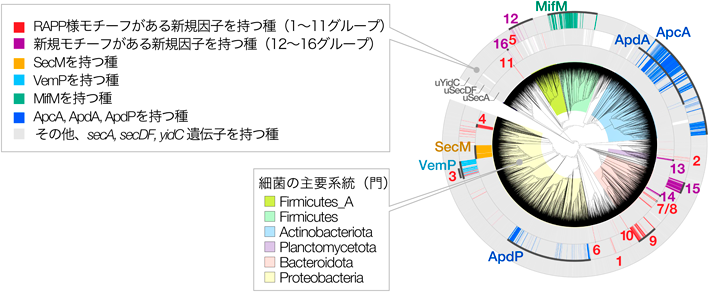
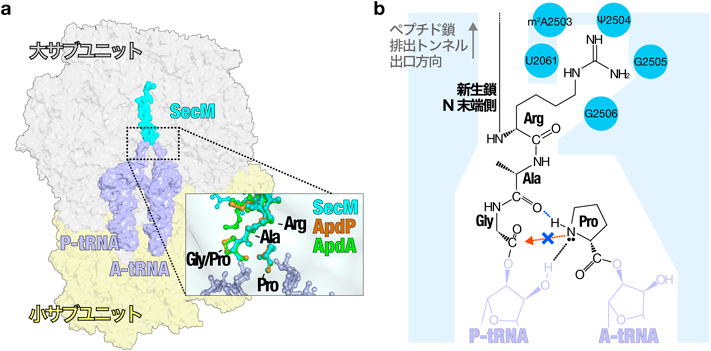
細菌の翻訳アレスト機構の普遍性と多様性Universality and diversity of bacterial translation arrest
1 国立遺伝学研究所National Institute of Genetics ◇ 〒411–8540 静岡県三島市谷田1111 ◇ 1111 Yata, Mishima, Shizuoka 411–8540, Japan
2 京都産業大学Kyoto Sangyo University ◇ 〒603–8555 京都市北区上賀茂本山 ◇ Motoyama, Kamigamo, Kita-ku, Kyoto 603–8555, Japan