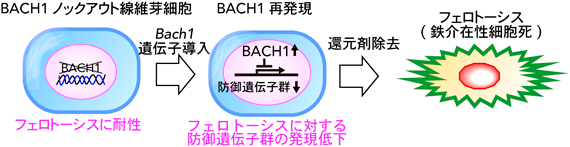
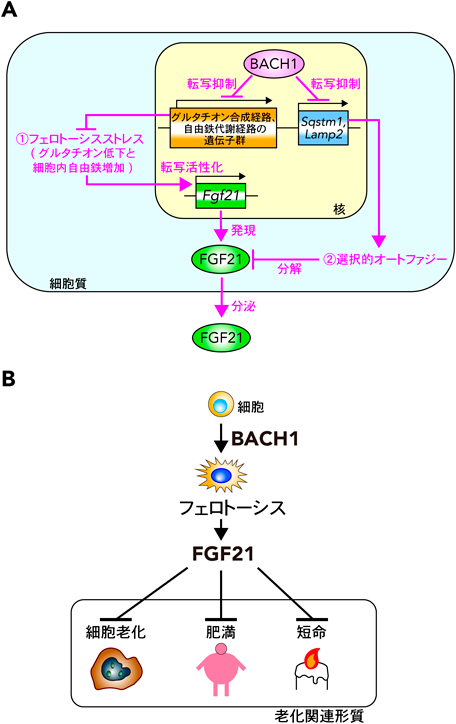
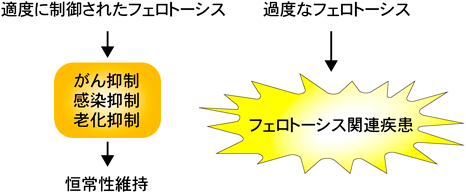
フェロトーシス細胞が分泌する抗老化シグナルThe anti-aging signal secreted from ferroptotic cells
1 東北大学大学院医学系研究科生物化学分野Department of Biochemistry, Tohoku University Graduate School of Medicine ◇ 〒980–8575 宮城県仙台市青葉区星陵町2–1 ◇ 2–1 Seiryo-machi, Aoba-ku, Sendai Miyagi 980–8575, Japan
2 コロンビア大学Irvingがん研究センターInstitute for Cancer Genetics and Herbert Irving Comprehensive Cancer Center, Columbia University ◇ 1130 St. Nicholas Ave. New York, NY 10032, USA ◇ 1130 St. Nicholas Ave. New York, NY 10032, USA