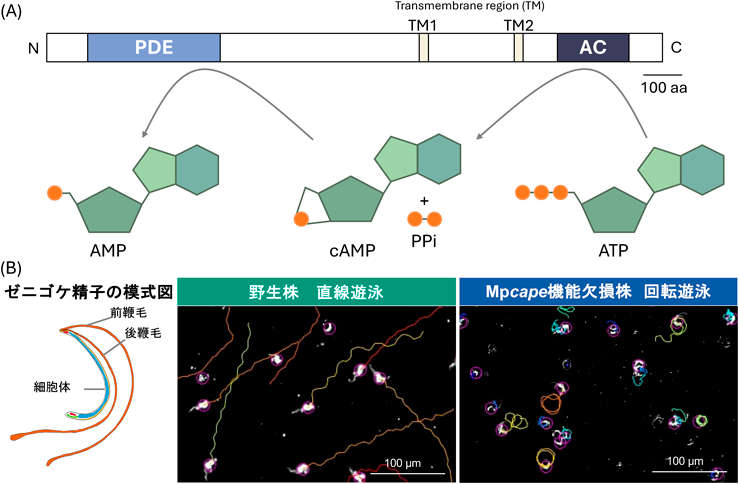
植物におけるcAMP合成・分解酵素の発見と機能Identification and functional roles of cAMP metabolizing enzymes in plants
立命館大学生命科学部生物工学科Department of Biotechnology, College of Life Sciences, Ritsumeikan University ◇ 〒525–8577 滋賀県草津市野路東1–1–1 ◇ 1–1–1 Nojihigashi, Kusatsu, Shiga 525–8577, Japan