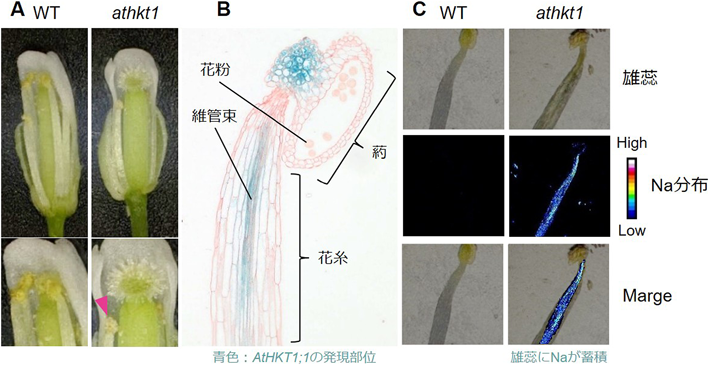
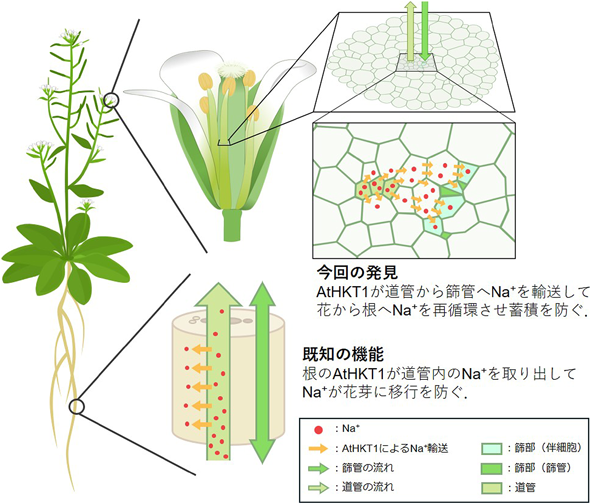
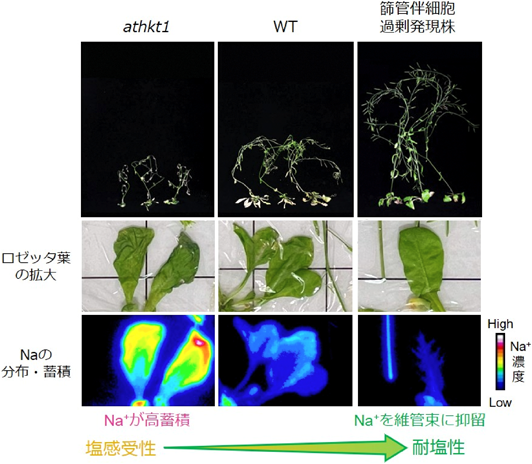
耐塩性を支える植物NaトランスポーターSodium transporters confer salt tolerance in plants
東北大学大学院工学研究科Department of Biomolecular Engineering, Graduate School of Engineering,Tohoku University ◇ 〒980–8579 宮城県仙台市青葉区荒巻字青葉6–6–7 ◇ 6–6–07 Aoba, Aramaki-aza, Aoba-ku, Sendai, Miyagi 980–8579, Japan