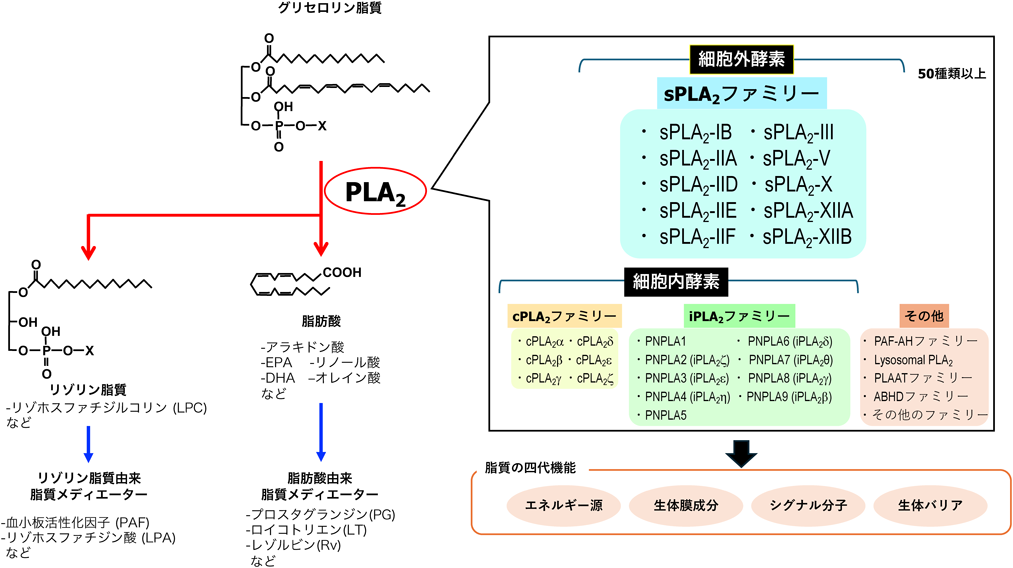
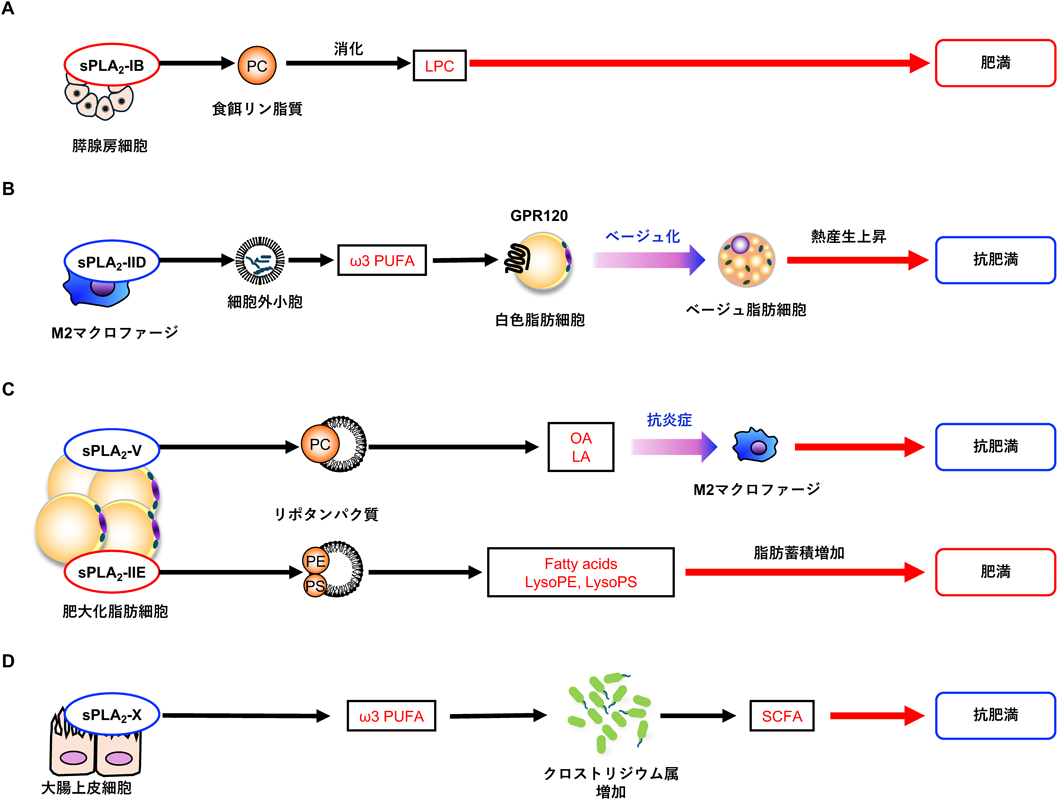
肥満を調節する細胞外リン脂質代謝酵素Secreted phospholipase A2 regulating obesity
1 東京大学大学院医学系研究科疾患生命工学センター健康環境医工学部門Laboratory of Microenvironmental Metabolic Health Sciences Center for Disease Biology and Integrative Medicine Graduate School of Medicine The University of Tokyo ◇ 〒113–8655 東京都文京区本郷7–3–1 ◇ 7–3–1 Hongo, Bunkyo-ku, Tokyo 113–8655, Japan
2 国立研究開発法人日本医療研究開発機構(AMED-CREST)Japan Agency for Medical Research and Development (AMED-CREST) ◇ 〒100–0004 東京都千代田区大手町1丁目7番1号 ◇ 1–7–1 Otemachi, Chiyoda-ku, Tokyo 100–0004, Japan