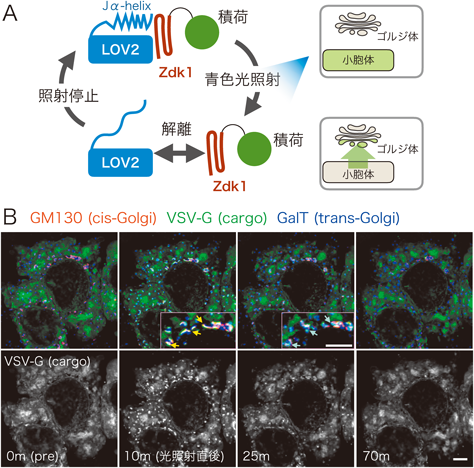
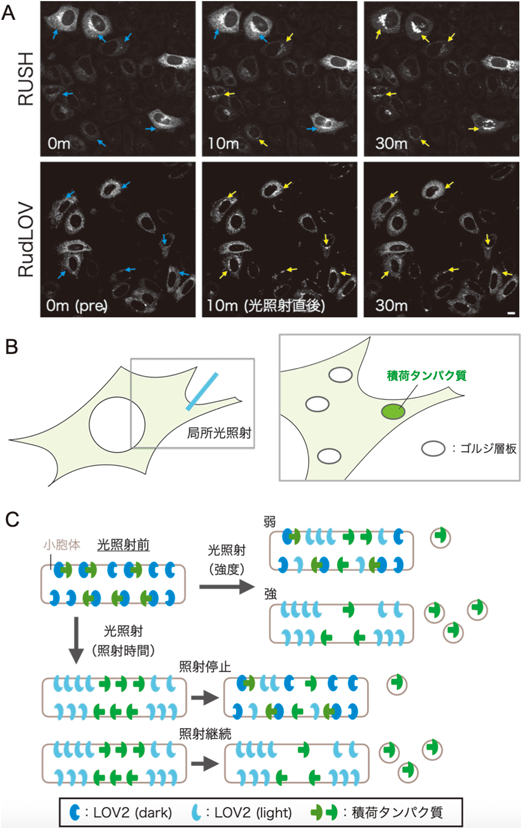
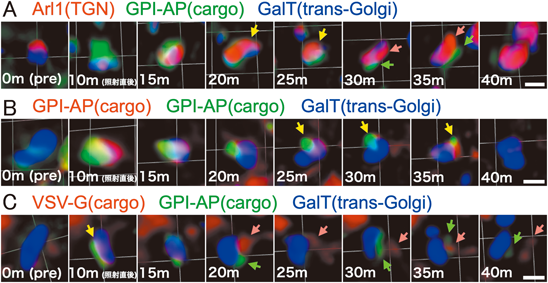
新規輸送開始実験法RudLOV法の開発と積荷輸送の観察Development of a new method for optical synchronized cargo transport, RudLOV, and observation of cargo transport
広島大学大学院統合生命科学研究科Graduate School of Integrated Sciences for Life, Hiroshima University ◇ 〒739–0046 広島県東広島市鏡山1丁目1–7–1 ◇ 1–7–1 Kagamiyama, Higashi-Hiroshima, Hiroshima 739–8528, Japan